Функции, патологии, диагностика и лечение вилочковой железы у детей
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Состояние вилочковой железы и иммунного статуса у новорожденных с внутриутробной инфекцией
Журнал: Российский вестник акушера-гинеколога. 2013;13(4): 27-30
Аксенов А. Н., Бочарова И. И., Башакин Н. Ф., Троицкая М. В., Лебедева Е. А., Обидина А. А., Новикова С. В., Шугинин И. О. Состояние вилочковой железы и иммунного статуса у новорожденных с внутриутробной инфекцией. Российский вестник акушера-гинеколога. 2013;13(4):27-30.
Aksenov A N, Bocharova I I, Bashakin N F, Troitskaia M V, Lebedeva E A, Obidina A A, Novikova S V, Shuginin I O. The thymus and immune status in neonatal infants with intrauterine infection. Russian Bulletin of Obstetrician-Gynecologist. 2013;13(4):27-30. (In Russ.).
Московский областной НИИ акушерства и гинекологии





Проведено обследование 158 доношенных новорожденных из группы высокого инфекционного риска, включающее ультразвуковую тимометрию и состояние иммунного статуса. Показано, что метод ультразвуковой тимометрии является высокоинформативным, доступным, безопасным и может быть применен у новорожденных в раннем неонатальном периоде. Нормативными значениями объема вилочковой железы у доношенных новорожденных в раннем неонатальном периоде следует считать от 1 до 2,5 мл/кг. Предложенные ультразвуковые критерии патологии тимуса в виде увеличения объема более 2,5 мл/кг или его уменьшения менее 1 мл/кг могут быть использованы в качестве ранних диагностических критериев внутриутробной инфекции и нарушений иммунного статуса у новорожденных.
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Московский областной НИИ акушерства и гинекологии
Проблема ранней диагностики внутриутробной инфекции (ВУИ), прогнозирования ее манифестации и осложнений нарушенного иммунного статуса остается актуальной, несмотря на значительное количество существующих бактериологических и иммунологических диагностических тестов. Большинство применяемых для диагностики ВУИ иммунологических методик являются дорогостоящими и трудоемкими, что делает их недоступными для скринингового обследования новорожденных.
Центральным органом иммуногенеза у новорожденных является вилочковая железа (ВЖ). У детей с патологией ВЖ отмечается высокая летальность, особенно в неонатальном периоде, так как на фоне патологии иммунной системы усугубляется течение практически любого заболевания. По данным разных авторов [4, 6], частота иммунодефицитных состояний (ИДС), обусловленных врожденной патологией ВЖ, колеблется от 2-3 до 98 случаев на 1000 вскрытий детей, умерших в периоде новорожденности. Такой разброс, по-видимому, обусловлен тем, что более чем у 90% детей ИДС своевременно не диагностируются.
До недавнего времени ведущим методом исследования состояния ВЖ была рентгенография органов грудной клетки. Сравнение рентгеновских данных с результатами патологоанатомического исследования указывает на их неточность, что может быть обусловлено индивидуальными особенностями строения железы, дистопией органа, глубоким выдохом во время рентгенографии, техническими ошибками. Кроме того, значительная лучевая нагрузка не позволяет широко использовать этот метод у новорожденных (Ж.Н. Бабаева, О.А. Споров, 1987).
В настоящее время для диагностики патологии ВЖ у детей раннего возраста, в том числе новорожденных, используется эхография. Ультразвуковое исследование (УЗИ) по сравнению с рентгенологическим является более чувствительным и специфичным методом для выявления патологии ВЖ в неонатальном периоде [1, 7]. Наиболее важной количественной оценкой размеров ВЖ является отношение ее массы к массе тела ребенка, и в норме оно колеблется от 0,18 до 0,38%. Врожденная стойкая гиперплазия ВЖ диагностируется у новорожденных при увеличении массы, объема, отношения массы железы к массе тела ребенка в 2 раза. Дети с тимомегалией склонны к возникновению и затяжному течению инфекционно-воспалительных заболеваний, различных проявлений аллергии [3]. Врожденная гипоплазия ВЖ характеризуется уменьшением размеров органа в 2 раза ниже по сравнению с нормой, при этом соотношение массы ВЖ к массе тела ребенка не превышает 0,1%. Доказана связь между патологией ВЖ и осложненным течением неонатального периода, поэтому рекомендуется проведение УЗИ ВЖ всем новорожденным с различной патологией. Выявление врожденной тимомегалии и гипоплазии ВЖ требует индивидуального подхода к проведению лечебных и профилактических мероприятий, в том числе иммунокоррекции.
Поскольку основным органом иммунной системы у плода и новорожденного является тимус, то исследования по сопоставлению морфологических особенностей ВЖ и иммунного статуса новорожденных группы высокого инфекционного риска для выявления информативных и доступных критериев ранней диагностики ВУИ являются целесообразными. Работы по изучению состояния ВЖ у новорожденных детей немногочисленны [2, 5, 8] и посвящены, в основном, ее эхографической характеристике у здоровых новорожденных. Анализ результатов УЗИ тимуса в сочетании с комплексной клинической оценкой состояния ребенка и показателями иммунного статуса позволит уточнить место ультразвуковой тимометрии в ранней диагностике ВУИ у новорожденных.
Цель исследования – повышение качества диагностики ВУИ у новорожденных из группы высокого инфекционного риска путем использования ультразвуковой тимометрии в раннем неонатальном периоде.
Материал и методы
Проведено обследование 158 доношенных новорожденных, родившихся у матерей с инфекционно-воспалительными заболеваниями урогенитального тракта. Для выявления клинико-лабораторных корреляций новорожденные были разделены на шесть групп в зависимости от основного клинического диагноза:
1-ю группу составили 29 новорожденных с генерализованными и тяжелыми локализованными формами ВУИ, которые включали сепсис, менингоэнцефалит, пневмонию, гастроэнтероколит; 2-я группа состояла из 19 новорожденных с локализованными инфекционными процессами средней степени тяжести, а именно: везикулопустулез, конъюнктивит, ринит, омфалит, вульвовагинит, локальные формы кандидоза; 3-я группа объединила 16 новорожденных с выявленными при УЗИ морфологическими изменениями в центральной нервной системе (ЦНС) и внутренних органах, что позволило предположить перенесенную ВУИ; 4-ю группу составили 19 новорожденных с гипоксическими повреждениями ЦНС разной степени тяжести; 5-я группа включала 18 новорожденных с задержкой внутриутробного развития (ЗВУР); 6-я группа состояла из 57 клинически здоровых новорожденных.
Всем новорожденным наряду с клиническими микробиологическими, иммунологическими методами исследования, было проведено УЗИ ВЖ с расчетом ее объема на 1 кг массы тела ребенка.
Методика ультразвуковой тимометрии
ВЖ расположена ретростернально в переднем средостении. Ее верхняя часть на 1-1,5 см выступает над ключицами, нижняя достигает третьего-четвертого межреберья, а задняя поверхность прилежит к крупным сосудам (аорта, легочная артерия, нижняя полая вена) и перикарду. Железа состоит из двух соприкасающихся долей, граница между которыми не дифференцируется при УЗИ, но в 3% случаев они могут располагаться отдельно.
При УЗИ ВЖ могут использоваться линейные, конвексные и секторные датчики (в зависимости от размеров акустического окна) с частотой 5,0-10,0 МГц. Плоскости сканирования: поперечная – в месте сочленения рукоятки и тела грудины, продольные – вдоль грудины и парастернально с обеих сторон. Проводят измерения максимального поперечного размера (А), длины (В) и толщины (С) в максимальном продольном срезе ВЖ. При асимметрии долей измерения осуществляются отдельно для каждой доли. Для расчета объема ВЖ используется формула:
V(мл) = А · В · С · 0,526; где А, В, С – линейные размеры ВЖ (в сантиметрах).
В большинстве современных УЗ-сканеров имеются встроенные программы расчета объемов измеряемых объектов, что значительно ускоряет работу.
Масса ВЖ в граммах соответствует суммарному объему в миллилитрах, так как удельная плотность ВЖ равна 1,0.
Результаты и обсуждение
На основании оценки клинических данных и показателей иммунитета с использованием перцентильной шкалы основных иммунологических показателей у обследованных новорожденных были выделены следующие варианты иммунного реагирования в раннем неонатальном периоде.
У новорожденных с тяжелыми формами ВУИ были выявлены два варианта иммунного ответа.

При первом варианте (15 новорожденных) отмечалась активация клеток врожденного и адаптивного иммунитета в сочетании с незрелостью и глубоким нарушением их эффекторных функций в виде значительного повышения числа незрелых клеток врожденного и адаптивного иммунитета, дефицита зрелых иммунокомпетентных клеток, увеличения продукции ИЛ-8 более 50 пг/мл, низкой способности к продукции лимфокинов, что являлось характерным для наиболее тяжелых, генерализованных форм ВУИ с ранней манифестацией, предположительно на фоне позднего антенатального инфицирования, с высоким риском летального исхода. Размеры ВЖ в 60% случаев (у 9 детей) составляли более 2,5 мл/кг, у 3 детей (20%) тимус был менее 1 мл/кг, в 3 случаях размеры ВЖ находились в пределах от 1 до 2,5 мл/кг (см. таблицу).
Второй вариант (14 новорожденных) был характерен для таких форм течения заболевания, которые возникали в результате аспирации и заглатывания околоплодных вод с развитием аспирационных пневмоний, что больше свидетельствовало об интранатальном инфицировании и подтверждалось высокой частотой осложнений в родах, более поздними сроками манифестации ВУИ в раннем неонатальном периоде, отсутствием генерализованных форм инфекции и летальных исходов. Выявленные изменения в иммунограмме характеризовались отсутствием активации иммунитета, дефицитом фагоцитов, зрелых Т- и В-лимфоцитов, преобладанием провоспалительного иммунного ответа, который в связи с нарушениями продукции цитокинов и фагоцитоза был недостаточно эффективным, что привело к манифестации тяжелых форм ВУИ у новорожденных. Объем тимуса у 9 (64,5%) новорожденных составлял от 1 до 2,5 мл/кг, у 4 (28,5%) – более 2,5 мл/кг, у 1 – менее 1 мл/кг.
Иммунный ответ у новорожденных с инфекционно-воспалительными заболеваниями средней степени тяжести (2-я группа) отличался провоспалительной направленностью, которая выражалась в виде повышения уровня IgM, IgG, интерферона в сыворотке крови в сочетании с отсутствием изменений количества и зрелости клеток врожденного и адаптивного иммунитета. Объем ВЖ у 15 (80%) новорожденных составлял от 1 до 2,5 мл/кг, у 3 (15%) – более 2,5 мл/кг, у 1 – менее 1 мл/кг.
Состояние иммунитета у новорожденных с выявленными при УЗИ морфологическими изменениями в ЦНС и внутренних органах (3-я группа) характеризовалось повышением числа зрелых Т- и В-лимфоцитов, клеток с маркером апоптоза, повышением уровня IgG и отсутствием IgM. Объем тимуса у 14 (87,5%) новорожденных составлял от 1 до 2,5 мл/кг, у 2 (12,5%) – менее 1 мл/кг.
По нашему мнению, изменения ЦНС и внутренних органов, выявленные при рождении, в сочетании с показателями иммунитета позволяют предположить наличие раннего внутриутробного инфицирования, преимущественно вирусной этиологии с благоприятным исходом для жизнеспособности плода на фоне этиотропной терапии в антенатальном периоде, но с формированием стойких структурных изменений, преимущественно в ЦНС, к моменту рождения. По-видимому, этот клинико-иммунологический вариант патологии новорожденных следует рассматривать как перенесенную внутриутробную вирусную инфекцию.
У 12 новорожденных с гипоксическими повреждениями ЦНС (4-я группа) без микробной контаминации иммунологически выявлялось повышение числа натуральных киллеров и активированных моноцитов без изменения числа и функциональной активности лимфоцитов. Объем ВЖ составлял от 1 до 2,5 мл/кг. У 7 детей этой группы с выявленной микробной контаминацией иммунный ответ характеризовался моноцитопенией, снижением экспрессии HLADR-антигена, повышением уровня IgM в сыворотке крови, что не исключало манифестацию ВУИ, клинические проявления которой в раннем неонатальном периоде неспецифичны и сходны с симптомами повреждения ЦНС гипоксического характера. У 17 новорожденных объем тимуса находился в пределах от 1 до 2,5 мл/кг, у 2 – менее 1 мл/кг.
Иммунный ответ у новорожденных со ЗВУР (5-я группа) характеризовался снижением количества зрелых Т- и В-лимфоцитов, моноцитов, у 28,5% детей выявлялось повышение уровней интерферона и ИЛ-8 в сыворотке крови. Постнатальные инфекционно-воспалительные заболевания на 1-м месяце жизни были диагностированы у 61% новорожденных. У 13 (72%) новорожденных объем ВЖ составлял от 1 до 2,5 мл/кг, у 5 (28%) тимус был уменьшен в размерах и его объем был менее 1 мл/кг. У 3 новорожденных с гипоплазией тимуса к концу раннего неонатального периода была диагностирована ВУИ вирусной этиологии (у 2 – цитомегаловирусная, у 1 – обусловленная вирусом простого герпеса 2-го типа).
Показатели иммунитета у 34 клинически здоровых новорожденных (6-я группа) без микробной контаминации статистически значимо не отличались от нормативных значений. При лабораторно установленной микробной контаминации у 23 здоровых новорожденных было выявлено увеличение числа зрелых Т- и В- лимфоцитов, основных субпопуляций Т-лимфоцитов, уровня IgG в сыворотке крови, снижение количества нейтрофилов и моноцитов без нарушения продукции лимфокинов. Объем тимуса находился в пределах от 1 до 2,5 мл/кг.
Выводы
1. Проведенные исследования показали четкую взаимосвязь между объемом ВЖ, наличием и степенью тяжести клинических проявлений ВУИ и дефектами иммунитета у новорожденных в раннем неонатальном периоде.
2. Нормативными значениями объема ВЖ у доношенных новорожденных в раннем неонатальном периоде следует считать от 1 до 2,5 мл/кг.
3. Выявленная эхоскопически тимомегалия с объемом ВЖ более 2,5 мл/кг была статистически значима для тяжелых форм ВУИ с нарушениями иммунного ответа в виде: незрелости и активации клеток как врожденного, так и адаптивного иммунитета с глубоким нарушением их эффекторных функций.
4. Уменьшение объема ВЖ менее 1 мл/кг коррелировало с дисфункцией иммунитета в виде дефицита зрелых иммунокомпетентных клеток с диссоциацией их эффекторных функций и недостаточностью провоспалительного ответа, что клинически характеризовалось затяжным течением ВУИ и высокой частотой постнатальных инфекционно-воспалительных заболеваний у новорожденных.
5. Увеличение объема тимуса более 2,5 мл/кг или его уменьшение менее 1 мл/кг у новорожденных в раннем неонатальном периоде следует рассматривать в качестве одного из показаний к проведению им заместительной иммунокоррекции.
6. Метод ультразвуковой тимометрии является высокоинформативным, доступным, безопасным и может быть включен в алгоритм обследования новорожденных группы высокого инфекционного риска.
Тимомегалия
Тимомегалия – гиперплазия тимуса и его гипофункция, сопровождающие ряд заболеваний детского возраста. Незначительная тимомегалия протекает бессимптомно; выраженное увеличение тимуса может проявляться синдром сдавления жизненно важных органов, синдромом лимфопролиферации, иммунными и эндокрино-обменными нарушениями. Диагностика тимомегалии требует участия детского иммунолога, проведения УЗИ вилочковой железы, рентгенографии грудной клетки, исследования показателей Т-звена иммунной системы и гормонального статуса. Детям с тимомегалией рекомендуются общеоздоровительные мероприятия, прием поливитаминов, биостимуляторов; по показаниям – глюкокортикостероидов.
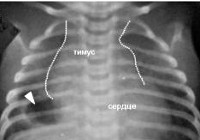
Общие сведения
Тимомегалия – превышение массы и объема вилочковой железы у детей предельных возрастных норм с сохранением нормальной гистологической структуры органа. Тимомегалия обнаруживается примерно у 13-34% детей раннего возраста и 3-12% детей старше 3-х лет. После 5-6 лет количество детей с тимомегалией существенно уменьшается. У мальчиков тимомегалия диагностируется в 1,5-2 раза чаще, чем у девочек. Дети, страдающие тимомегалией, составляют в педиатрии группу риска по развитию аллергических, эндокринных, аутоиммунных и онкологических заболеваний, синдрома внезапной детской смерти, потому нуждаются в особом уходе и дополнительном наблюдении со стороны педиатра и детского аллерголога-иммунолога.

Причины тимомегалии
Вилочковая железа или тимус представляет собой центральный орган иммунной системы и железу внутренней секреции. В тимусе происходит трансформация клеток-предшественников (претимоцитов) в Т-лимфоциты, участвующие в регуляции клеточного и гуморального иммунитета. Кроме этого, вилочковая железа секретирует свыше 20 биологически активных веществ, среди которых гормоны и гормоноподобные вещества, регулирующие обмен веществ, гемопоэз, уровень кальция и сахара в крови, фосфора в скелетных мышцах, рост и половое созревание. Максимальную массу тимус имеет к моменту рождения ребенка (4,4% массы тела); его рост продолжается до 15 лет, после чего орган подвергается постепенной возрастной инволюции – замещению железистой ткани жировой и соединительной.
К развитию тимомегалии могут приводить различные эндогенные и экзогенные факторы, а также их сочетание. Доказана генетическая детерминированность тимомегалии и ее связь с HLA-антигенами B15, B18, В27. Определенную роль в формировании тимомегалии у ребенка играет отягощенный акушерский анамнез матери (аборты и выкидыши в анамнезе, токсикозы беременности, резус-конфликт, поздняя беременность и др.); вредное влияние на плод лекарств, алкоголя, рентгеновского облучения; патология периода новорожденности и раннего возраста (асфиксия, недоношенность, родовые травмы, синдром дыхательных расстройств, конъюгационная желтуха, сепсис новорожденных) и др. Тимомегалия является характерным проявлением лимфатико-гипопластического диатеза.
Классификация тимомегалии
Исследователи выделяют врожденную (первичную) и приобретенную (вторичную) тимомегалию. При врожденной тимомегалии вилочковая железа сформирована правильно, однако увеличена в размерах, что сопровождается снижением ее секреторной функции, гиперплазией лимфоидной ткани и дисфункцией нейро-эндокринной системы.
Приобретенная тимомегалия развивается вследствие первичного поражения других эндокринных желез: гипокортицизма, обусловленного аддисоновой болезнью, травмами, воспалительным или опухолевым поражением коры надпочечников; гипоталамического синдрома при окклюзионной гидроцефалии, васкулитах, опухолях головного мозга и пр.
Кроме этого, увеличение вилочковой железы может носить функциональный характер (например, при ОРВИ, пневмонии и др. заболеваниях); в этих случаях после выздоровления размеры тимуса и иммуногормональные показатели приходят в норму. Органическая тимомегалия связана с непосредственным поражением вилочковой железы.
Симптомы тимомегалии
Незначительное увеличение вилочковой железы может протекать без каких-либо выраженных клинических проявлений. Иногда для обозначения небольшой гиперплазии используется понятие «синдром увеличенной вилочковой железы» (СУВЖ), а термином «тимомегалия» обозначается значительное увеличение органа, сопровождающееся развернутой клинической симптоматикой.
Дети с тимомегалией отличаются характерными фенотипическими чертами: округлыми мягкими формами тела, крупными чертами лица и увеличенными поперечными размерами тела (широким лицом, плечами, грудной клеткой, ладонями и стопами), бледной, слабо пигментированной кожей, светлыми волосами и глазами, слабо развитой мускулатурой, повышенным аппетитом. Чаще чем в популяции у них отмечается нарушение темпов и последовательности прорезывания зубов, позднее начало ходьбы, задержка речевого развития и дислалия.
Из сопутствующих заболеваний при тимомегалии могут встречаться паховые и пупочные грыжи, ВПС (септальные дефекты), перинатальная энцефалопатия, рахит, врожденный вывих бедра, синдактилия, крипторхизм, фимоз, гипоплазия матки и влагалища и др. Дети с тимомегалией склонны к артериальной гипотонии, аритмиям, повышенной потливости, необъяснимому длительному субфебрилитету. Клинически значимая тимомегалии может сопровождаться сдавлением жизненно важных органов (трахеи, сосудистого пучка, ВПВ, блуждающего нерва), развитием синдромов иммунодефицита и лимфопролиферации, эндокрино-обменных нарушений.
При компрессии увеличенным тимусом жизненно важных органов может развиваться синдром верхней полой вены: набухание шейных вен, расширение венозной сети на верхней части туловища, одышка, цианоз. В случае сдавления трахеи возникает кашель, одышка, шумное храпящее дыхание, возбужденное состояние. Раздражение блуждающего нерва сопровождается брадикардией, дисфонией, срыгиваниями или рвотой, коллапсами.
Тимомегалия обычно сочетается с гиперплазией лимфоидной ткани (лимфаденопатией, увеличением аденоидов и миндалин, спленомегалией). В раннем и дошкольном возрасте дети с тимомегалией относятся к группе часто болеющих; у них отмечаются частые эпизоды ОРВИ с сильным коклюшеподобным кашлем и ложным крупом, отиты, пневмонии, выраженные поствакцинальные реакции. Эндокринные сдвиги проявляются ожирением, гипокортицизмом, гипопаратиреозом, сахарным диабетом, дисфункцией щитовидной железы, гиперпигментацией кожных покровов.
Диагностика тимомегалии
Обследование детей с тимомегалией проводится педиатром, детским иммунологом, детским эндокринологом и включает несколько этапов (клинико-анамнестический, инструментальный и лабораторный). При оценке объективного статуса ребенка с тимомегалией обращается внимание на перинатальный анамнез, конституционные данные, перенесенные заболевания.
Основная роль в выявлении тимомегалии принадлежит инструментальному обследованию – рентгенографии грудной клетки, УЗИ вилочковой железы, УЗИ органов брюшной полости и надпочечников. Рентгенодиагностика позволяет определить степень тимомегалии на основании исчисления кардио-тимико-торакального индекса (КТТИ) и вазокардиального индекса (ВКИ). В норме на рентгенограммах в прямой проекции тень вилочковой железы располагается за тенью сердца и сосудистого пучка. При тимомегалии I степени тень тимуса занимает 1/2 половину грудной клетки, II степени – 1/2 – 3/4 грудной клетки, III степени – более 3/4 грудной клетки. УЗИ тимуса позволяет оценить объем и массу органа и составить более четкое представление о степени тимомегалии.
Лабораторные показатели при тимомегалии характеризуются снижением субпопуляции Т-лимфоцитов (CD3, CD4, CD8); резким уменьшением количества зрелых В-клеток, низким уровнем IgG и IgА, повышенным – IgM и IgE; снижением концентрации АКТГ, кортизола, повышением уровня СТГ и ТТГ, некоторым увеличением концентрации паратиреоидного гормона.
Лечение тимомегалии
Вопросы ведения детей с тимомегалией и необходимости проведения корригирующей терапии разработаны недостаточно. Общепринято считать, что при незначительном увеличении тимуса специальных лечебных мероприятий не требуется. Рекомендуется грудное вскармливание, рациональное питание, ограничение стрессов и контактов с инфекционными больными.
Объем медикаментозной терапии определяет иммунолог, наблюдающий ребенка с тимомегалией. Часто болеющим детям каждые 3-4 месяца показан прием адаптогенов и биостимуляторов (женьшеня, пантокрина, элеутерококка, лимонника китайского). С целью иммунокоррекции используется экстракт тимуса крупного рогатого скота. Дважды в год до достижения 5-6-летнего возраста ребенку назначаются курсы индукторов синтеза глюкокортикоидов (аммония глицирризината, этимизола).
При тяжелых заболеваниях, стрессах, а также перед оперативными вмешательствами детям с тимомегалией назначаются глюкокортикоиды (преднизолон, гидрокортизон). В случае развития синдрома тимусо-надпочечниковой недостаточности (апатии, сильной слабости, брадикардии, рвоты, диспепсии, артериальной гипотонии, признаков почечной недостаточности) показано введение преднизолона, инфузионных растворов, сердечных гликозидов, препаратов калия.
При тимомегалии I-II степени профилактическая вакцинация не противопоказана, но проводится на фоне гипосенсибилизирующей терапии и гипоаллергенной диеты. Детям с тимомегалией III степени при благоприятной эпидобстановке дается отвод от прививок на 6 месяцев (за исключением вакцинации против полиомиелита).
Прогноз и профилактика тимомегалии
Обычно тимомегалия у детей сохраняется до 3-6 лет, после чего размеры вилочковой железы приходят норму. Тем не менее, дети с тимомегалией более подвержены инфекционно-воспалительным и аллергическим заболеваниям, риску внезапной смерти от гипофункции коры надпочечников, сдавления увеличенным тимусом органов средостения.
Дети с тимомегалией должны состоять на диспансерном учете у педиатра, детского аллерголога-иммунолога, эндокринолога; проходить ежегодное лабораторно-инструментальное обследование. К возможным мерам по предупреждению тимомегалии можно отнести исключение перинатальных вредностей. Детям с увеличенной вилочковой железой следует избегать стрессов, контактов с инфекционными больными, своевременно проходить профилактические курсы лечения.
УЗИ вилочковой железы у детей: показание к проведению, как делается, что показывает – МЕДСИ
Ультразвуковое исследование (УЗИ) — процедура, безопасная для ребенка любого возраста. Она позволяет провести точную диагностику быстро и безболезненно. При этом не применяется рентгеновское излучение, которое вредно для детского организма. В основе принципа его действия лежит эффект различного отражения звуковых волн высокой частоты от разных типов органов и тканей.
Что из себя представляет вилочковая железа?
Вилочковая железа (тимус) является важной частью организма, отвечающей за выработку Т-лимфоцитов для иммунитета человека. Она размещается в верхней области грудной клетки (в верхнем средостении).
Размеры и масса железы меняются на протяжении всей жизни человека:
- В момент рождения она весит 15 грамм и составляет около 5 см в длину
- К окончанию полового созревания и на протяжении основного периода взрослой жизни ее масса составляет 20–37 грамм, а длина — 7,5–16 см
- К старости (порядка 75-ти лет) ее вес уменьшается до 6 грамм
Вилочковая железа имеет серо-розовый цвет тканей, а в пожилом возрасте — желтоватый.
С какой целью проводят УЗИ тимуса?
Врач назначает УЗИ вилочковой железы для детей в случае, когда имеются жалобы на постоянные болезни ребенка (простуды, ОРЗ и др.) и низкий иммунитет. Это необходимо, чтобы определить причины возникновения регулярных недомоганий.
Ультразвуковое исследование позволяет выявить патологическое увеличение размеров тимуса — тимомегалию. В результате ее появления ослабляется иммунитет, и ребенок начинает регулярно заражаться различными болезнями от других детей и взрослых. В таком случае на фоне обычной простуды может возникнуть аллергия, расстройство ЖКТ, появляется высокая температура.
Показания к проведению
УЗИ тимуса назначается при таких симптомах, как:
- Ребенок регулярно заболевает (до 10-ти раз в год)
- Обычная простуда часто приобретает более тяжелую форму и сопровождается осложнениями (пневмония, бронхит, синусит)
- Температура часто поднимается до 37,5 и держится длительное время
- Обильное срыгивание, слишком частое и тяжелое дыхание
- Появление бронхиальной астмы, аллергических реакций, которые не устраняются даже при более правильной диете
- При общей слабости, хронической утомляемости, болях в груди
- Если сетка сосудов на груди четко отображается
- При нарушении сердечного ритма (аритмия)
- При увеличении лимфоузлов, миндалин или аденоидов
Что может выявить УЗИ?
УЗИ вилочковой железы у детей помогает выявить следующие виды заболеваний и нарушений:
- Тимомегалия
- Патологии развития тимуса
- Аплазия (недоразвитость железы)
- Новообразования (доброкачественные и злокачественные)
- Синдром Бернара-Горнера (аутосомное заболевание)
- Синдром Незелофа (появляется из-за того, что вилочковая железа не справляется со своими функциями)
- Синдром Ди Джорджи (характеризуется низким производством Т-лимфоцитов)
Также ультразвуковое исследование позволит определить такие параметры, как:
- Изменение размера (он должен меняться в пределах возрастных норм)
- Правильность структуры тканей органа
- Контуры (в норме должны быть четкими и однородными)
Как проводится?
Процесс проведения УЗИ вилочковой железы довольно прост:
- Ребенок принимает необходимое для исследования положение тела:
- В возрасте до года он должен находиться на руках у родителей
- От года — он садится или ложится на кушетку
- Если ребенок — подросток, то он должен стоять
- С верхней части тела снимается одежда
- На грудь наносится гель для улучшения проводимости звука
- Врач водит датчиком по верхней части груди
- Изображение отображается на экране, и по нему специалист делает выводы о состоянии органа
Вся процедура занимает порядка 10–15 минут.
Подготовка
Перед проведением ультразвукового исследования вилочковой железы не требуется сложной подготовки:
- Необходимо предупредить врача, если принимаются различные лекарственные препараты
- Следует узнать точный вес ребенка и сообщить его доктору
- Одежду необходимо подобрать такую, которую будет легко снять перед процедурой
- Рекомендуется объяснить ребенку, что за обследование предстоит и как оно будет проходить, чтобы он не нервничал
Расшифровка результатов
Для расшифровки результатов врач должен знать точную массу тела ребенка, поскольку от этого значения зависит определение нормального объема и веса вилочковой железы (их соответствия возрастным нормам).
В норме масса железы составляет 0,3 % от общей массы тела. При превышении данного значения ставится диагноз «тимомегалия». Она бывает трех степеней, а ее значение измеряется особым индексом КТТИ:
- I — при значении индекса КТТИ от 0,33 до 0,37 %
- II — при значении КТТИ от 0,37 до 0,42 %
- III — при значении индекса более 0,42 %
Также на сонограмме (результате УЗИ) могут быть обнаружены и такие изменения железы, как: опухоль, чрезмерное разрастание тканей и др.
Можно ли исследовать тимус другими способами
УЗИ вилочковой железы как методика используется относительно недавно. Ранее для целей выявления нарушений в работе и строении вилочковой железы использовали рентгенологическое исследование. Но такой анализ нельзя проводить часто, в отличие от УЗИ, поскольку рентген-облучение является вредным для детского организма.
Если результаты УЗИ тимуса оказались недостаточно однозначными или контрастными, врач может назначить дополнительные виды обследования:
Тимома
Клеточные элементы мозгового и коркового слоев, равно как и строма, могут стать источником различных опухолей. Эти опухоли, по данным большинства авторов, чаще располагаются в передневерхнем средостении и известны под названием тимом.
Термин «тимома», предложенный Грандхоуммом еще в 1900 г., объединяет все виды опухолей вилочковой железы и применяется и в настоящее время.
Опухоли вилочковой железы – тимомы – встречаются у лиц всех возрастных групп, одинаково часто как у мужчин, так и у женщин, у детей значительно реже (около 8%). Наиболее часто тимомы встречаются у больных миатенией в зрелом и пожилом возрасте. По строению различают: эпителиоидную тимому (эпидермоидную, веретеноклеточную, лимфоэпителиальную, гранулематозную) и лимфоидную тимомы.
Большинство тимом относится к лимфоэпителиомам. В ряде случаев опухоль вилочковой железы состоит из элементов тимуса и жировой ткани – так называемая липотимома, образование которой обычно протекает бессимптомно.
Патогенез (что происходит?) во время Тимомы:
Опухоль обычно небольших размеров, покрыта капсулой, относительно доброкачественная. Однако понятие «доброкачественная тимома» весьма условно, так как в ряде случаев те опухоли, которые при гистологическом исследовании расцениваются как доброкачественные, нередко имеют тенденцию к инфильтративному росту, метастазированию и дают рецидивы после их удаления.
Доброкачественные тимомы длительное время могут протекать бессимптомно, достигая иногда значительных размеров. При этом отмечаются признаки сдавливания органов средостения (ощущение сдавливания, одышка, сердцебиение, набухание шейных вен, цианоз лица). У детей они могут вызвать деформацию грудной клетки – выбухание грудины. Злокачественная тимома составляет около 20-30%. Злокачественные опухоли вилочковой железы характеризуются бурным инфильтративным ростом, ранним и обширным метастазированием. Метастазирует в ближайшие лимфатические узлы и отдаленные органы (реже).
При любом гистологическом типе строения опухоли в толще ее нередко встречаются очаги некроза, кровоизлияния с последующим кистообразованием, фиброзом.
У 10-50% больных с тимомами и задержкой инволюции тимуса выявляются симптомы миастении.
Симптомы Тимомы:
Клиническая картина тимом весьма разнообразна. Около 50% случаев образования опухолей протекает бессимптомно и выявляется во время профилактических рентгенологических исследований или проявляется симптомами сдавливания органов переднего средостения.
При значительном сдавливании появляется чувство стеснения за грудиной, неприятные ощущения и боли, одышка, набухание шейных вен, одутловатость и синюшная окраска лица. Особенно выражены респираторные нарушения у детей вследствие сдавливания относительно узкой податливой трахеи.
Наиболее часто тимомы сочетаются с миастенией, реже – с агаммаглобулинемией, арегенераторной анемией, синдромом Иценко-Кушинга.
В течении болезни можно выделить бессимптомный период и период выраженных клинических проявлений. Длительность бессимптомного периода зависит от локализации и размеров новообразования, его характера (злокачественное, доброкачественное), скорости роста, взаимоотношений с органами и образованиями средостения. Очень часто новообразование длительное время развивается бессимптомно, и его случайно обнаруживают при профилактическом рентгенологическом исследовании грудной клетки.
Клинические признаки новообразований состоят из:
- симптомов сдавливания или прорастания опухоли в соседние органы и ткани;
- общих проявлений заболевания;
- специфических симптомов, характерных для различных новообразований.
Наиболее частыми симптомами являются боли, возникающие вследствие сдавливания или прорастания опухоли в нервные стволы или нервные сплетения, что возможно как при доброкачественных, так и при злокачественных новообразованиях. Боли, как правило, неинтенсивные, локализующиеся на стороне поражения, и нередко иррадиируют в плечо, шею, межлопаточную область. Боли с левосторонней локализацией часто похожи на боли при стенокардии. При возникновении болей в костях следует предполагать наличие метастазов. Сдавливание или прорастание опухолью пограничного симпатического ствола обусловливает возникновение синдрома, характеризующегося опущением верхнего века, расширением зрачка и западением глазного яблока на стороне поражения, нарушением потоотделения, изменением местной температуры и дермографизма. Поражение возвратного гортанного нерва проявляется осиплостью голоса, диафрагмального нерва – высоким стоянием купола диафрагмы. Сдавливание спинного мозга ведет к расстройствам функции спинного мозга.
Проявлением компрессионного синдрома является и сдавливание крупных венозных стволов, и в первую очередь верхней полой вены (синдром верхней полой вены). Он проявляется нарушением оттока венозной крови от головы и верхней половины туловища: у больных появляются шум и тяжесть в голове, усиливающиеся в наклонном положении; боли в груди, одышка, отечность и синюшность лица, верхней половины туловища, набухание вен шеи и грудной клетки. Центральное венозное давление повышается до 300-400 мм вод. ст. При сдавливании трахеи и крупных бронхов возникают кашель и одышка. Сдавливание пищевода может вызвать дисфагию – нарушение прохождения пищи.
На поздних стадиях развития новообразований возникают: общая слабость, повышение температуры тела, потливость, похудание, которые характерны для злокачественных опухолей. У некоторых больных наблюдаются проявления нарушений, связанных с интоксикацией организма продуктами, выделяемыми растущими опухолями. К ним относится артралгический синдром, напоминающий ревматоидный полиартрит; боли и припухлость суставов, отеки мягких тканей конечностей, нарастание частоты сердечных сокращений, нарушение сердечного ритма.
Таким образом, клинические признаки новообразований тимуса весьма многообразны, однако они проявляются в поздних стадиях развития заболевания и не всегда позволяют установить точный этиологический и топографо-анатомический диагноз. Важным для диагностики являются данные рентгенологических и инструментальных методов, особенно для распознавания ранних стадий заболевания.
Диагностика Тимомы:
Синдромы, сопутствующие тимоме, заставляют начать целенаправленное исследование для обнаружения тимомы, поэтому опухоли раньше выявляются и имеют сравнительно небольшие размеры. Бессимптомно развивающиеся опухоли вилочковой железы достигают значительно больших размеров к моменту обнаружения или появления симптомов сдавления органов средостения. Опухоли размером 3 см в диаметре и меньше выявляются с помощью компьютерной томографии. Быстрое увеличение опухоли при динамическом наблюдении, неровные нечеткие контуры указывают на злокачественный ее характер.
Основным методом диагностики новообразований является рентгенологический. Применение комплексного рентгенологического исследования позволяет в большинстве случаев определить локализацию патологического образования – средостение или соседние органы и ткани (легкие, диафрагма, грудная стенка) и распространенность процесса.
К рентгенологическим методам обследования больного с новообразованием тимуса относятся: рентгеноскопия, рентгенография и томография грудной клетки, контрастное исследование пищевода.
Рентгеноскопия дает возможность выявить патологическую тень, составить представление о ее локализации, форме, размерах, подвижности, интенсивности, контурах, установить отсутствие или наличие пульсации ее стенок. В ряде случаев можно судить о связи выявленной тени с расположенными рядом органами.
Для уточнения полученных при рентгеноскопии данных производят рентгенографию. При этом уточняют структуру затемнения,его контуры, отношение новообразования к соседним органам и тканям. Контрастирование пищевода помогает оценить его состояние, определить степень смещения или прорастания опухолью.
При наличии увеличенных лимфатических узлов надключичных областей проводят их биопсию, что позволяет определить их метастатическое поражение или установить системное заболевание. При наличии компрессионного синдрома производят измерение центрального венозного давления.
Больным с новообразованиями выполняют общий и биохимический анализ крови. При подозрении на эхинококкоз показано определение реакции латексагглютинации с эхинококковым антигеном. Изменения морфологического состава периферической крови обнаруживаются, главным образом, при злокачественных опухолях (анемия, лейкоцитоз, лимфопения, повышенная скорость оседания эритроцитов), воспалительных и системных заболеваниях. При сочетании опухоли с аутоиммунными заболеваниями повышается титр аутоантител против различных антигенов.
Рентгенсемиотика опухолей и кист вилочковой железы. Рентгенологическая семиотика. В прямой проекции по правому или левому Контуру срединной тени выявляется неправильной формы полуовальная тень средней или высокой интенсивности. Уровень расположения этой тени различен, но чаще это верхний или средний отдел срединной тени. Структура затемнения однородна, очертания его обычно бугристые, крупноволнистые, реже гладкие.
Как и при других образованиях, расположенных в непосредственной близости к сердцу и магистральным сосудам, тень тимомы обладает передаточной пульсацией. Исследование в боковой проекции позволяет определить, что затемнение располагается спереди и примыкает к тени грудины. Иногда есть необходимость провести послойную томографию. Особенно демонстративна рентгенологическая картина при пневмомедиастинуме.
Четкие очертания опухоли и отграниченность ее от соседних органов и тканей дают основание предположить доброкачественный вариант тимомы. Злокачественный вариант опухоли вилочковой железы проявляется обычно двусторонним расширением срединной тени с нечеткими бугристыми очертаниями и быстрым увеличением на фоне заметного ухудшения общего состояния больных.
Дифференциальная диагностика. От загрудинного зоба тимома отличается отсутствием связи с областью шеи и наличием отчетливо выявляемой верхней границы; тень опухоли не смещается кверху при глотании.
От дермоидов и тератоидов, располагающихся в этом же отделе средостения, тимому отличают бугристые очертания. Для тератодермоидов типично наличие ровных очертаний и правильной овоидной формы, что для тимомы исключение.
Лечение Тимомы:
Основным методом лечения больных с опухолями вилочковой железы является хирургический – удаление вилочковой железы с опухолью. И чем раньше будет выполнено хирургическое вмешательство, тем лучше, так как нередко опухоль имеет инвазивный рост, вовлекая в процесс жизненно важные органы, из-за чего опухоль оказывается нерезектабельной. При операции по поводу тимомы необходимо удалять не только опухоль, но и обязательно – всю вилочковую железу и, если возможно, всю жировую клетчатку переднего средостения.
В противном случае может быть рецидив опухоли и рецидив миастении. Операции выполняются трансстернальным доступом, который позволяет произвести хорошую ревизию и удалить опухоль, вилочковую железу и прилежащую жировую клетчатку переднего средостения. Если при гистологическом исследовании опухоль оказывается злокачественной, после операции больного (после снятия с раны операционных швов) необходимо перевести в специализированное онкологическое учреждение для химио-и лучевого лечения.
Ранний послеоперационный период у больных миастенией с опухолью вилочковой железы протекает тяжелее, чем у больных с гиперплазией железистой ткани.
Чаще наблюдается миастенический криз, требующий многодневной искусственной вентиляции легких, трахеотомии, интенсивной терапии, включая современные методы детоксикации и др.
Лучевая терапия вилочковой железы до операции проводится больным пожилого возраста с сопутствующими заболеваниями, так как риск операции у них слишком высок. В дальнейшем, может быть, некоторым из них при улучшении общего состояния удастся выполнить радикальную операцию. Большинству же в оперативном лечении приходится отказывать.
Определенный лечебный эффект оказывают ингибиторы холинэстеразы: галантамин (по 1 мл 1%-ного водного раствора), прозерин (по 1 мл 0,05%-ного раствора). Глюкокортикоиды дают временный эффект.
К каким докторам следует обращаться если у Вас Тимома:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Тимомы, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Тимус – что это? Роль тимуса на первому году жизни ребенка
Тимус (вилочковая железа) – важный орган иммунной системы детей. Он расположен в верхнем отделе грудной клетки и состоит из двух долей, соединяющихся в передней части трахеи. Железа растет до наступления половой зрелости, достигая массы 30–40 грамм, затем постепенно уменьшается (обратное развитие).
Она играет доминирующую роль в иммунной, эндокринной системе. Тимус продуцирует тимозин, тимопоэтин, стимулирующие выработку антител, а также производит Т-лимфоциты – белые клетки крови, уничтожающие аномальные клетки с чужеродными антигенами. Другая функция вилочковой железы – предотвращение патологического роста клеток и предупреждение рака. Следует отметить, что тимус играет ведущую роль в иммунитете ребенка до трех лет.

Роль тимуса в жизни ребёнка
До рождения и в детстве тимус ответственен за производство плюс созревание Т-лимфоцитов, защищающих организм от определенных угроз, включая вирусы, бактерии. Тимус является крупнейшим лимфоидным органом у новорожденных, так как активнее других тканей продуцирует лимфоциты. Железа выступает «первой скрипкой» в развитии и улучшении иммунной системы ребенка.
Тимус производит и секретирует тимозин – гормон, необходимый для выработки Т-клеток. После «созревания» в железе они поступают в кровь и мигрируют в лимфоузлы и селезенку, где помогают иммунной системе бороться с болезнью.
В некоторых случаях функции вилочковой железы снижены, что ослабляет иммунную систему, увеличивая склонность к инфекциям и аллергии. Ребенок страдает затяжными ОРВИ, патология легко переходит в хроническую. Недостаток Т-лимфоцитов в организме может привести к иммунодефицитным заболеваниям, характеризующимися сильной потливостью, отечностью и/или болезненностью горла, припухлостью лимфатических узлов, депрессией.
Недоедание и дефицит белка в раннем возрасте обусловливает медленный или ограниченный рост тимуса, «подрывая» тем самым нормальное функционирование лимфоцитов. Вот почему важно сбалансированное питание с достаточным количеством белка.
Доктора данного направления
Патология тимуса
Основные виды патологии тимуса:
- Аплазия – отсутствие или недоразвитие вилочковой железы
- Гипо- и дисплазия – недоразвитие тимуса
- Акцидентальная инволюция – уменьшение вилочковой железы, под влиянием гормонального дисбаланса, стресса, инфекции
- Атрофия – уменьшение, замещение железистой ткани соединительной, прекращение функционирования
- Тимомегалия – увеличение массы и объема паренхимы вилочковой железы выше возрастной нормы при сохранении ее нормального строения
- Гиперплазия – увеличение железистой ткани, с нарушением выработки иммунных клеток и функционирования тимуса.
- Тимома – опухоль вилочковой железы.
- Киста тимуса – жидкостное образование вилочковой железы.
- Патология тимуса (вилочковой железы) может вызывать: развитие ряда иммунодефицитных синдромов, аутоиммунных заболеваний и некоторых эндокринных нарушений.
Увеличение тимуса у детей
Отклонение в размере тимуса в большую сторону и снижение его функции обозначают термином «синдром увеличенной вилочковой железы» (СУВЖ) у детей. Проблему увеличенного тимуса чаще рассматривают в свете дифференциальной диагностики с плевритом, перикардитом, опухолями средостения, другими патологиями.
Ошибочно считают, что увеличенный тимус у детей грудного или раннего возраста является физиологическим состоянием. Особенности протекания инфекционных заболеваний у маленьких пациентов с СУВЖ заставляют классифицировать синдром, как патологию. Дети с СУВЖ имеют большую вероятность развития дисбаланса нейроэндокринной плюс иммунной систем. Поэтому пациенты с выявленным увеличением тимуса требуют полного обследования и диспансерного наблюдения у эндокринолога, иммунолога.
Симптомы заболевания или нарушения развития вилочкой железы
Для того, что бы вовремя выявить патологию тимуса, родителям стоит обратить внимание на отклонения, имеющие различную степень выраженности, которые могут свидетельствовать о заболевании или нарушении развития вилочковой железы:
- Частая заболеваемость ребенка простудными заболеваниями.
- Затяжное течение различных заболеваний, с частыми осложнениями.
- Увеличение лимфоидной ткани – лимфатических узлов, миндалин, аденоидов, ткани на задней поверхности глотки.
- Бледность и/или мраморный рисунок на коже ребёнка.
- Большой вес ребёнка при рождении.
- Ребёнок быстро теряет и быстро набирает вес.
- Кашель вне простудного заболевания, который усиливается в положении ребёнка горизонтально.
- Потливость, субфебрильная температура длительное время вне простудных заболеваний.
- Гипергидроз, холодные конечности.
- Видимая венозная сеточка на груди малыша.
- Цианоз (посинение) носогубного треугольника при нагрузках (плач, бег)
- Частые срыгивания, икоты, отрыжки
- Одышка
- Нарушение сердечного ритма
При возникновении подозрений на патологию тимуса, врач может назначить дополнительные методы обследования:
- УЗИ вилочковой железы,
- КТ,
- МРТ,
- рентген,
- общий анализ крови,
- иммунограмму,
- биохимический анализ крови,
- кровь на гормоны.
Тимическая недостаточность поддается иммунокорекции, которая индивидуально подбирается врачом аллергологом-иммунологом. Стоит обратить внимание, что своевременная диагностика патологии вилочковой железы особенно актуальна на первом году жизни ребенка, когда ребенку начинают проводить вакцинацию.
Для получения подробных консультаций о роли тимуса в жизни ребёнка на первом году жизни обращайтесь к педиатрам медицинских центров «Президент-Мед»
В КЛИНИКАХ «ПРЕЗИДЕНТ-МЕД» ВЫ МОЖЕТЕ
- пройти обследование и лечение по более чем 30 медицинским специализациям, реабилитацию после инсультов, операций, травм, (более 5000 видов анализов и лабораторных исследований), (УЗИ, эндоскопия: гастроскопия), ЭКГ, установка и расшифровка СМАД и Холтер-ЭКГ и другие,
- пройти медицинскую комиссию за один день, пройти профосмотр (как для организаций, так и для частных лиц), – справки в ГИБДД и для допуска к занятиям спортом, для приобретения оружия, в санаторий,
- при наличии показаний – оформить лист временной нетрудоспособности,
- оформить и получить другие виды медицинской документации,
- сделать любые инъекции, одного дня или дневного стационара.
Смотрите так же по теме:

Автор: Лаврова Нина Авенировна
Окончила Ярославский государственный медицинский институт по специальности «Лечебное дело»
Медицинский опыт работы – 25 лет
ЗАБОЛЕВАНИЯ ВИЛОЧКОВОЙ ЖЕЛЕЗЫ И ИХ ЛЕЧЕНИЕ
II кафедра клинической хирургии (заведующий – профессор Тимофей Павлович Макаренко) Центрального института усовершенствования врачей на базе Центральной клинической больницы № 1МПС.
Публикация посвящается памяти Василия Дмитриевича Стоногина (1933-2005)
Заболевания вилочковой железы изучаются врачами различных специальностей: невропатологами, эндокринологами, иммунологами, гемато¬логами, хирургами, патогистологами и др. Проблема миастении является относительно изученной; в последние годы установлено участие вилочковой железы в таком жизненно важном процессе, как выработка (регулировка) иммунитета.
Опухоли и кисты вилочковой железы, миастения и некоторые аутоиммунные заболевания требуют хирургического лечения. Значительный вклад в этот сложный раздел внесли отечественные и зарубежные хирурги (А. Н. Бакулев и Р. С. Колесникова; В. Р. Брайцев; Б. К. Осипов; Б. В. Петровский; М. И. Кузин и соавт.; С. А. Гаджиев и В. Васильев; Viets, и др.).
С 1966 по 1973 год мы наблюдали 105 больных с различными заболеваниями переднего средостения, из них 66 с различными заболеваниями вилочковой железы. Эти больные были разделены на следующие клинические группы: 1-я – 30 больных с гиперплазией вилочковой железы и явлениями миастении; 2-я – 23 больных с опухолями вилочковой железы (тимомами), из них с доброкачественными 15, в том числе с явлениями миастении 9; со злокачественными 8, в том числе с явлениями миастении 5; 3-я – 4 больных с кистами вилочковой железы, все без миастении; 4-я – 3 больных с тератоидными образованиями; 13-я – 2 больных – лимфогранулематоз с изолированным поражением вилочковой железы; 6-я – 4 больных с апластической анемией на фоне аутоиммунной агрессии вилочковой железы.
Из 66 больных 65 были оперированы: 62 произведена радикальная и 3 эксплоративная операция.
С явлениями миастении под нашим наблюдением было 44 больных, из которых 43 (13 мужчин и 30 женщин) оперированы; возраст оперированных был от 14 до 55 лет, причем возраст большинства (25 больных) – от 15 до 30 лет. Среди больных с опухолями вилочковой железы преобладали 30-40-летние (13 больных).
Миастения – сложное нейроэндокринное заболевание, основным проявлением которого является слабость и особенно быстрая, патологическая мышечная утомляемость после физической нагрузки. Наряду с этим, согласно исследованиям ряда авторов (М. И. Кузин и соавт., и др.), при ми¬астении нарушается функция многих органов и систем (сердечно-сосудистой, дыхательной, пищеварительной, обмена веществ и т. д.).
Клиника миастении хорошо известна, однако правильный диагноз больному с миастенией нередко ставят после продолжительного наблюдения. У 32 из 44 наших больных правильный диагноз был поставлен только через 6-8 месяцев после появления первых признаков заболевания. Это объяс¬няется малой выраженностью клинической картины миастении в начальной стадии и плохой осведомленностью практических врачей, к которым впервые обращаются за помощью больные миастенией (невропатологи, окулисты, отоларингологи, терапевты).
При выраженной генерализованной форме миастении диагноз не труден. В начальной стадии и в случаях, когда миастения носит локализован¬ный характер (бульбарная, глазная, скелетно-мышечная, глоточно-лицевая), у наших больных предполагались самые разнообразные диагнозы, вплоть до подозрения на симуляцию. Считаем необходимым подчеркнуть особую важность прозериновой пробы, имеющей дифференциально-диагностическое значение. У больных миастенией внутримышечная инъекция 1-2 мл 0,05% раствора прозерина устраняет мышечную слабость и быструю утомляемость, в то время как при миопатиях и мышечной слабости, вызванных другими причинами, инъекция прозерина не дает эффекта. Имеют значение динамометрия, эргометрия и электромиография.
Общепризнано, что лечение миастении должно проводиться комплексно с участием 3-4 специалистов: невропатолога, терапевта-эндокринолога, анестезиолога-реаниматолога и хирурга. На основании большого клинического материала (сотни оперированных и наблюдаемых в отдаленном периоде) авторы подчеркивают преимущество оперативного лечения миастении перед консервативным (М. И. Кузин; А. С. Гаджиев и соавт., и др.). Результаты оперативного лечения лучше, если операцию производят впервые 2-2,5 года от начала заболевания. В более поздние сроки операция оказывается менее эффективной. Отсюда вытекает особая важность ранней диагностики миастении.
Из 43 оперированных нами больных в первый год заболевания миастенией поступили лишь 12, в сроки от 1 года до 3 лет – 23 и после 3 лет – 8 больных. Следовательно, больные поступали в клинику для оперативного лечения поздно.
Специальным методом исследования вилочковой железы является рентгеноконтрастный – пневмомедиастинография, которая позволяет судить о степени увеличения вилочковой железы, её структуре – отдель¬ный узел с четко ограниченными контурами или опухоль с инфильтрирую¬щим ростом и т. д.
Наличие у больного выраженной клинической картины прогрессирующей миастении является показанием к операции, так как все консервативные методы лечения, включая и рентгенотерапию, дают лишь временное улучшение.
У больных миастенией необходима специальная предоперационная подготовка, цель которой – снижение проявлений миастении путем индивидуального подбора дозы лекарственных препаратов. Дозировки препаратов подбирают строго индивидуально, с таким расчетом, чтобы в течение суток не наблюдалось периодов миастенического истощения, не наступало миастенического криза. Предоперационная подготовка, являясь симптоматической терапией, оказывает некоторое лечебное действие, что имеет положительное значение для предстоящей операции. Однако не у всех больных предоперационная подготовка, несмотря на ее комплексность и интенсивность, оказывается эффективной.
Вопрос о необходимости предоперационной рентгенотерапии нельзя считать окончательно решенным. Только 5 из наших больных перед операцией получали рентгеновское облучение, причем каких-либо улучшений в течении послеоперационного периода мы у них не отметили. У больных, оперированных по поводу злокачественной тимомы с явлениями миастении, предоперационное облучение играет важную роль в ближайшем исходе операции и в какой-то степени влияет на сроки наступления рецидива заболевания (М. И. Кузин и соавт.).
Большинство операций по поводу миастении нами выполнено из переднего доступа путем полной срединной продольной стернотомии. Наиболее ответственным моментом операции является отделение железы от левой плечеголовной вены. Ранение этого сосуда опасно из-за массивного кровотечения и возможной воздушной эмболии. В одном случае произошло ранение этой вены, закончившееся благополучно (был наложен боковой сосудистый шов). При операции следует избегать наложения зажимов на железистую ткань, раздавливания её.
У 3 наших больных было сочетание миастении и загрудинного зоба. Произведены тимэктомия и субтотальная струмэктомия.
У 26 больных во время операции была повреждена медиастинальная плевра, в том числе у 8 больных с обеих сторон. Осложнений, связанных с операционным пневмотораксом, не было. Если во время операции плевра не повреждена, переднее средостение дренируется одной резиновой трубкой, конец которой выводят в нижний угол раны или через отдельный прокол ниже мечевидного отростка и соединяют с отсосом. Вслед за тимэктомией трахеостома (превентивно) была наложена 5 больным.
Если сама операция тимэктомии по сравнению с другими торакальными операциями не представляет особой сложности, то течение послеоперационного периода у ряда больных сопровождается осложнениями, на 1-м месте среди которых стоит миастенический криз. Поэтому операции по поводу миастении возможны только в тех учреждениях, где можно обеспечить круглосуточное наблюдение анестезиолога-реаниматолога, а также многодневную аппаратную вентиляцию лёгких.
Вопрос о назначении антихолинэстеразных препаратов в послеоперационном периоде окончательно не решен. С целью уменьшения гиперсекреции бронхов лучше назначать прозерин с небольшими дозами атропина.
Тяжелый миастенический криз с расстройством дыхания, сердечной деятельности, глотания и т. д. наблюдали в первые дни после операции у 26 больных. Вывести из криза консервативными мероприятиями удалось 7 больных; 19 больным была наложена трахеостома с переводом их на аппаратное дыхание, длительность которого составляла от 3 до 40 суток. Через трахеостому систематически круглосуточно аспирируют слизь из трахеобронхиального дерева. Питание больных, находящихся на аппаратном дыхании, осуществляется через зонд. Помимо медикаментозного лече¬ния, применения кислорода, использования дыхательной гимнастики, в последние годы всем больным миастенией в послеоперационном периоде проводится лечебный массаж всего тела, повторяемый несколько раз в день.
Трахеостомическую трубку удаляют после того, как у больного стойко восстанавливается самостоятельное дыхание.
Из 43 оперированных по поводу миастении в первые дни после операции умерли 3 больных. Это относится к периоду, когда в клинике только осваивались эти операции. Все больные оперированы в тяжелом состоянии. Отдаленные результаты прослежены у 26 больных: выздоровление наступило у 17 и улучшение (больные принимают антихолинэстеразные препараты) – у 8 больных; состояние осталось без изменений у 3 больных. Двое оперированных умерли от рецидива злокачественной тимомы (один – с явлениями миастении через 3 года, другой – с инфарктом миокарда).
Доброкачественные опухоли вилочковой железы (тимомы) представля¬ют собой узлы округленной формы с плотной капсулой. При гистологическом исследовании в этих опухолях наряду с соединительнотканными клетками обнаруживаются фибробласты и концентрически расположенные вытянутые эпителиальные клетки, напоминающие тельца Гассаля. Эти опухоли по строению напоминают склерозирующую ангиому, еще их называют ретикулярной перителиомой (Pope и Osgood). Особое место занимают липотимомы. Одни авторы относят их к доброкачественным опухолям, другие – к злокачественным (Andrus и Foot). Опухоли эти нередко достигают боль¬ших размеров и состоят из жировой дольчатой ткани, содержащей скопления тимоцитов и гассалевых телец. Если в опухоли преобладает жировая ткань, её рекомендуют называть липотимомой, если преобладают элементы вилочковой железы – тимолипомой.
Среди наших больных мы наблюдали 3 (2 мужчин и 1 женщину, все старше 40 лет) с липотимомой. У них опухоль была небольших размеров, с ровными четкими границами; опухоль была расценена нами как доброкачественная. Заболевание сопровождалось умеренно выраженными явлениями миастении. Один из этих больных поступил с жалобами на слабость и быструю утомляемость; при дальнейшем обследовании у него была выявлена тяжелая гипопластическая анемия. Больной оперирован; в ближайшем послеоперационном периоде отмечены благоприятные результаты.
Из 15 наших больных с доброкачественными тимомами у 9 (4 мужчин и 5 женщин) были явления миастении, у остальных опухоль ничем себя не проявляла и была выявлена случайно.
Злокачественные тимомы – плотные, различных размеров бугристые опухоли, нередко прорастающие капсулу. У больных с этими новообразованиями из-за быстрого роста опухоли, прорастания соседних органов или сдавления их рано развивается синдром медиастинальной компрессии. Больные жалуются на боли за грудиной, чувство давления в грудной клетке и др. Нередко злокачественные тимомы протекают с явлениями миастении, отмеченной нами у 5 из 8 больных. Злокачественная тимома может протекать и совершенно бессимптомно. Приводим пример.
Больной М., 19 лет, поступил 17.III.1966 года. Жалоб нет. После окончания средней школы при прохождении медицинского обследования для поступления в учебное заведение у него рентгенологически было выявлено опухолевое образование в переднем средостении. Признаков миастении нет. Пневмомедиастинография: в переднем средостении со всех сторон окутанное газом образование продолговатой формы размером 15*5 см, с участками просветления в центре; заключение: опухоль вилочковой железы, возможно, с участками распада. Произведена тимэктомия. Гистологически: злокачественная тимома ретинулоклеточного типа. Проведена послеоперационная рентгенотерапия. Осмотрен через 4 года после операции:, жалоб нет, состояние хорошее, признаков рецидива нет.
Дифференциальный диагноз доброкачественных и злокачественных тимом нередко бывает трудным. Злокачественная тимома по рентгенологическим признакам напоминает лимфогранулематоз и лимфосаркому. В отличие от этих образований тимома располагается непосредственно за грудиной, обычно бывает овально-сплющенной или конусовидной формы. Всякая тимома, протекает она с явлениями миастении или без них, подлежит удалению, В литературе имеются указания, что каждую тимому следует рассматривать как потенциально злокачественную опухоль (Б. В. Петровский; Seybold и соавт., и др.).
Кисты вилочковой железы встречаются довольно редко. Обычно это тонкостенные образования различных размеров, расположенные в толще железы, выполненные желтоватой или коричневатой жидкостью. Из-за эла¬стичности этих образований признаков сдавления окружающих органов не наблюдается. Клиническая картина кист, если они протекают без миастении, бедна. Как правило их обнаруживают случайно, при профилактическом осмотре. Все наши 4 больных (3 женщины и 1 мужчина) были старше 40 лет (41 год – 48 лет). Ни у одного больного не было признаков миастении, хотя описаны сочетания кисты вилочковой железы и миастении. Все были оперированы (тимэктомия) с благоприятным результатом.
У 3 оперированных нами больных опухоль переднего средостения по гистологическому строению была тератомой. Учитывая тесную связь образования с остатками вилочковой железы и наличие в самом образовании ткани вилочковой железы, мы расценили опухоль как тератому вилочковой железы. У 2 больных на основании признаков (появление в мокроте сальных масс, волос у одной больной, а также обнаружение органоидных включений на рентгенограмме у другой) диагноз был поставлен до операции, у третьей больной – лишь во время операции. Из 3 оперированных больных у 2 при¬шлось удалить не только тератоидное образование, но и долю лёгкого из-за вовлечения последнего в процесс (прорыв нагноившейся тератомы в верхнедолевой бронх). Высокая степень злокачественного превращения тератоидных образований, возможность нагноения и другие осложнения убеждают в необходимости раннего и радикального хирургического удаления этих новообразований.
Вопрос о возможности изолированного поражения вилочковой железы лимфогранулематозом представляется спорным. Мы наблюдали 2 больных, у которых до операции был установлен диагноз “опухоль вилочковой железы”. После операции, при гистологическом исследовании препаратов, диагноз был изменен: изолированное поражение лимфогранулематозом вилочковой железы. Принимая во внимание указания о возможности изолированного поражения вилочковой железы на ранних стадиях заболевания (С. А. Гаджиев и В. В. Васильев), оба эти наблюдения мы отнесли к патологии вилочковой железы. После операции за больными ведётся наблюдение в течение 5 лет. Признаков рецидива и генерализации процесса нет.
Заболевание, заключающееся в сочетании патологии вилочковой желе¬зы и гипопластической анемии, которая возникает вследствие избирательного поражения костного мозга без изменения продукции лейкоцитов и тромбоцитов, впервые описано Кацнельсоном в 1922 году. Позже было предположено, что вилочковая железа влияет на гемопоэтическую функцию костного мозга, регуляцию состава белковых фракций, состояние лимфоидной системы и т. д. (Soutter и соавт.). С тех пор опубликованы данные некоторых авторов об отдельных операциях на вилочковой железе при различных болезнях крови (А. Н. Бакулев, 1958; Chaemers и Boheimer, и др.). К настоящему времени нами произведены 4 операции тимэктомии у больных гипопластической анемией. О результатах этих операций говорить пока рано, так как после них прошел небольшой срок. Ближайшие результаты удовлетворительные у 3 больных.
- В вилочковой железе возникает ряд патологических процессов, которые требуют оперативного лечения.
- Оперативное лечение по поводу миастении оправдано как при наличии рентгенологически и клинически определяемой опухоли, так и лишь при гиперплазии вилочковой железы.
- Операцию рекомендуется производить в ближайшее время после установления диагноза. Лучевое лечение целесообразно проводить после удаления злокачественной опухоли или если произвести радикальную операцию невозможно.
1) Бакулев А. Н., Колесникова Р. С. Хирургическое лечение опухолей и кист средостения. М., 1967.
2) Брайцев В. Р. Врожденные дизонтогенетические образования средостения и легких. М., 1960.
3) Гаджиев С. А., Догель Л. В., Ваневский В. Л. Диагностика и хирургическое лечение миастении. Л., 1971.
4) Гаджиев С. А., Васильев В. Мед газета, 1973, №15.
5) Кузин М. И. Клин мед, 1969, № 11, с. 6.
6) Кузин М. И., Успенский Л. В., Волков Б. П. Вести, хир., 1972, №7, с.48.
7) Осипов Б. К. Хирургические заболевания легких и средостения. М., 1961.
8) Петровский Б. В. Хирургия средостения. М., 1960.
9) Andгus W., Fооt N., J. thorac. Surg., 1937, v. 6. p. 648.
10) Chaemers G., Boheimer K., Brit. med. J., 1954, v.2, p.1514.
11) Pope R., О s g о о d R., Am. J. Path., 1953, v. 20, p. 85.
12) S е у b о 1 d W., D о n a 1 d М. С., J. thorac. Surg. Clagett C. et al., 1950, v. 20, p.195.
13) Soutter G., Sommers Sh. R e 1 m о n Ch. et al. Ann. Surg., 1957, v. 146, p. 426.
14) Viets H., Brit. med. J., 1950, v. 1, p.139.
Данные об авторах:
| 1) Виктор Львович Маневич – профессор, доктор медицинских наук, 2-я кафедра клинической хирургии ЦОЛИУв. |  |
| 2) Василий Дмитриевич Стоногин – доцент 2-й кафедры хирургии ЦОЛИУв, заведующий учебной частью кафедры, кандидат медицинских наук. E-mail: svas70@mail.ru |  |
Восстановление текста, компьютерная графика – Сергей Васильевич Стоногин.
Любое копирование материала запрещено без письменного разрешения авторов и редактора.


