Действие инсулина на организм

Как показывает мировая статистика, от сахарного диабета страдает более 20% населения нашей планеты. Причем у большинства из этих людей был диагностирован инсулинозависимый диабет, вылечить который не представляется возможным. Но это не говорит о том, что больной не может вести привычный образ жизни.
Все, что для этого нужно, обеспечить свой организм инсулином. С этой целью применяются специальные инъекции, постановка которых осуществляется строго по схеме, выписанной врачом. Но каков механизм действия инсулина? И как он помогает диабетикам?
Роль инсулина в человеческом организме
Инсулин представляет собой особый гормон, который принимает участие в углеводном обмене. Именно он занимается расщеплением глюкозы и обеспечивает насыщение клеток организма необходимой энергией. Продуцированием этого гормона занимается поджелудочная железа. При нарушении целостности или функционирования клеток этого органа инсулин вырабатывается в маленьком количестве, в результате чего организм начинает испытывать в нем дефицит, что проявляется повышением уровня сахара в крови.
При этом нарушается работа почек и печени, в организме начинают скапливаться токсичные вещества, негативно влияющие на все внутренние органы и системы. И в первую очередь от этого страдает сосудистая система. Под воздействием сахара и токсичных веществ снижается тонус стенок сосудов, они становятся хрупкими и ломкими, на фоне чего риски развития инсульта и инфаркта миокарда увеличиваются в несколько раз.
Повышенное содержание сахара в крови оказывает влияние и на регенерационные процессы в организме. Это особенно заметно по состоянию кожных покровов. Любые порезы и раны заживают очень долго, часто подвергаются инфицированию и перерастают в язвы. А это тоже является опасным, так как при нагноении язв вероятность развития гангрены также возрастает.
Механизм действия
Говоря о том, как действует инсулин в организме, следует отметить, что работает он непосредственно через белок-рецептор. Представляет он собой сложный интегральный белок клеточной мембраны, который состоит из 2 субъединиц. В медицине их отмечают как a и b. Каждая из этих субъединиц имеет свою полипептидную цепочку.
Действие инсулина происходит следующим образом: сначала он вступает в связь с а-субъединицей, таким образом изменяя ее конформацию. После этого в процесс вовлекается b-субъединица, которая запускает разветвленную цепь реакций по активации ферментов, необходимых для расщепления глюкозы и ее усвоения в клетках.
Следует отметить, что несмотря на то, что действие инсулина в организме изучается учеными уже на протяжении многих столетий, его биохимические свойства еще до конца не изучены. Однако уже стало известно, что во всем этом процессе принимают участие вторичные «посредники», в роли которых выступают диацилглицеролы и инозитолтрифосваты. Именно они обеспечивают активизацию протеинкиназы С с фосфорилирующим действием и имеют связь с внутриклеточным обменом веществ.
Данные посредники обеспечивают усиленное поступление глюкозы в клетки организма, тем самым насыщая их энергией. Сначала комплекс инсулин-рецептора погружается в цитозоль, а далее разрушается в лизосомах, после чего возникают деградационные процессы – часть инсулина разрушается, а другая его часть направляется к мембранам клеток и снова встраивается в них.
Инсулин – это гормон, который оказывает прямое воздействие на обменные процессы во всем организме. Многие его эффекты наблюдаются, благодаря его активному действию на ряд ферментов. Он единственный в своем роде, который способствует снижению уровня сахара в крови. Происходит это за счет:
- усиления поглощения клеточными мембранами глюкозы;
- активизации ферментов гликолиза;
- повышения активности продуцирования гликогена;
- снижения синтеза глюконеогенеза, отвечающего за образование в клетках печени глюкозы.
Инсулин является единственным гормоном, который усиливает усвоение клетками аминокислот, необходимых для нормального их функционирования, а также поставку в них ионов калия, магния и фосфата. Кроме этого, инсулин способствует усилению продуцирования жирных кислот за счет преобразования глюкозы в триглицериды. Если же в организме наблюдается дефицит инсулина, то это приводит к мобилизации жиров и их отложению в тканях внутренних органов.
Антикатаболическое действие инсулина на организм обуславливается уменьшением процесса гидролиза белков, за счет чего снижается их деградация (из-за того, что при диабете у больных наблюдается дефицит инсулина, деградация белков увеличивается, в результате чего наблюдается снижение мышечного тонуса и возникает слабость).
Помимо этого, инсулин обеспечивает уменьшение липолиза, за счет чего снижается концентрация жирных кислот в крови и риски возникновения холестериновой болезни, тромбофлебита и т.д. становятся намного меньше.
Действие на углеводный обмен
Как уже стало понятно, инсулин – это гормон, который принимает участие практически во всех процессах, происходящих в организме. Но так как речь идет непосредственно о сахарном диабете, необходимо более детально рассмотреть действие инсулина на углеводный обмен.
В том случае, если в организме наблюдается дефицит этого гормона, то это влечет за собой нарушение процесса проникновения глюкозы сквозь клетки мышечных тканей, в результате чего наблюдается снижение энергетических запасов. Когда уровень инсулина повышается до нормальных значений, этот процесс восстанавливается, причем естественным путем.
Однако при повышенной физической активности мембраны клеток повышают свою проницаемость и поглощают намного больше глюкозы, чем обычно. И происходит это даже в том случае, если уровень сахара в крови является очень низким. Но риски развития гипогликемической комы в данном случае возрастают в несколько раз.
Инсулиновый рецептор играет немаловажную роль в процессе гомеостаза глюкозы. Если он нарушается, это приводит к дегенеративным изменениям в клетках, что провоцирует развитие многих заболеваний, среди которых находится не только сахарный диабет, но и рак.
Рассматривая действие инсулина, нельзя не сказать о его воздействии на печень. Именно в этом органе организм откладывает излишки глюкозы как бы прозапас, высвобождая ее только тогда, когда уровень сахара в крови снижается до критических отметок.
И еще один важный момент: инсулин, как уже говорилось выше, участвует в процессе гликолиза, активируя синтез определенных ферментов, без которых расщепление и усвоение клетками глюкозы является невозможным.
Действие на белковый обмен
Инсулин играет немаловажную роль не только в углеводном обмене, но и в белковом. Именно он обеспечивает расщепление белков, поступающих вместе с пищей, на аминокислоты, которые активизируют в организме синтез собственных белков. При дефиците инсулина этот процесс нарушается, что приводит к различным осложнениям. Помимо этого, инсулин обеспечивает ускорение транскрипции ДНК, стимулируя образование РНК.
Действие на жировой обмен
Инсулин принимает также активное участие в липогенезе – синтезе жирных кислот. Их формирование происходит в процессе распада углеводов. А жирные кислоты являются также очень важными для организма, так как без них происходит нарушение жирового обмена, что сопровождается развитием ожирения и отложением жировых клеток во внутренних органах.
Инъекции инсулина
При развитии сахарного диабета действовать нужно незамедлительно. Как правило, сначала у людей диагностируется СД2, и только при несоблюдении диет и правил приема лекарственных препаратов развивается СД1, при котором без инсулиновых инъекций просто не обойтись.
На сегодняшний день выделяются следующие типы инсулиносодержащих препаратов:
- Быстрого действия . Действовать начинают уже спустя 5 минут после подкожного введения и достигают своего максимального пика через 1 час. Но,такие препараты обладают одним недостатком – действуют они недолго, и их введение необходимо осуществлять перед каждым приемом пищи либо при наступлении гипогликемической комы.
- Короткого действия . Эффективность наблюдается спустя 30 минут после введения. Применяются такие инъекции также перед едой. Однако его действие длится намного дольше, чем у инсулина быстрого действия.
- Среднего действия . Такие препараты применяются в комплексе с инсулинами быстрого или короткого действия. Эффективность после их приема наблюдается в течение нескольких часов.
- Длительного действия . Препараты гипогликемического действия, эффективность которых наблюдается на протяжении суток. Однако применять такие препараты также нужно с инсулинами короткого и быстрого действия. Применяются они несколько раз в день до употребления пищи через равные промежутки времени.
Какой именно препарат будет прописан больному, зависит от его индивидуальных особенностей и тяжести протекания болезни. Чтобы правильно подобрать средство, врачам необходимо более детально изучить молекулярные свойства крови. Для этого обязательно делается биохимия венозной крови и крови из пальца.
По результатам обследования врач сможет подобрать не только препарат, но и его дозировку, которая будет наиболее эффективной и безопасной для пациента. Так как неправильно подобранная дозировка инсулина может привести к гипогликемии и возникновению серьезных осложнений. Поэтому заниматься самолечением ни в коем случае нельзя. Применение инъекций инсулина должно происходить под строгим контролем врача.
Инсулин – самый молодой гормон
Строение
Инсулин представляет собой белок, состоящий из двух пептидных цепей А (21 аминокислота) и В (30 аминокислот), связанных между собой дисульфидными мостиками. Всего в зрелом инсулине человека присутствует 51 аминокислота и его молекулярная масса равна 5,7 кДа.
Синтез
Инсулин синтезируется в β-клетках поджелудочной железы в виде препроинсулина, на N-конце которого находится концевая сигнальная последовательность из 23 аминокислот, служащая проводником всей молекулы в полость эндоплазматической сети. Здесь концевая последовательность сразу отщепляется и проинсулин транспортируется в аппарат Гольджи.
На данном этапе в молекуле проинсулина присутствуют А-цепь, В-цепь и С-пептид (англ. connecting – связующий). В аппарате Гольджи проинсулин упаковывается в секреторные гранулы вместе с ферментами, необходимыми для “созревания” гормона . По мере перемещения гранул к плазматической мембране образуются дисульфидные мостики, вырезается связующий С-пептид (31 аминокислота) и формируется готовая молекула инсулина. В готовых гранулах инсулин находится в кристаллическом состоянии в виде гексамера, образуемого с участием двух ионов Zn 2+ .
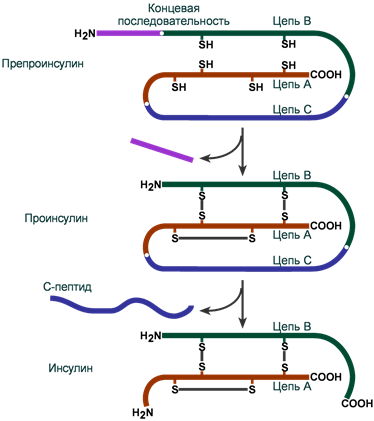
Схема синтеза инсулина
Регуляция синтеза и секреции
Секреция инсулина происходит постоянно, и около 50% инсулина, высвобождаемого из β-клеток, никак не связано с приемом пищи или иными влияниями. В течение суток поджелудочная железа выделяет примерно 1/5 от запасов имеющегося в ней инсулина.
Главным стимулятором секреции инсулина является повышение концентрации глюкозы в крови выше 5,5 ммоль/л, максимума секреция достигает при 17-28 ммоль/л. Особенностью этой стимуляции является двухфазное усиление секреции инсулина:
- первая фаза длится 5-10 минут и концентрация гормона может 10-кратно возрастать, после чего его количество понижается,
- вторая фаза начинается примерно через 15 минут от начала гипергликемии и продолжается на протяжении всего ее периода, приводя к увеличению уровня гормона в 15-25 раз.
Чем дольше в крови сохраняется высокая концентрация глюкозы, тем большее число β-клеток подключается к секреции инсулина.
Индукция синтеза инсулина происходит от момента проникновения глюкозы в клетку до трансляции инсулиновой мРНК. Она регулируется повышением транскрипции гена инсулина, повышением стабильности инсулиновой мРНК и увеличением трансляции инсулиновой мРНК.
Активация секреции инсулина
1. После проникновения глюкозы в β-клетки (через ГлюТ-1 и ГлюТ-2) она фосфорилируется гексокиназой IV (глюкокиназа, обладает низким сродством к глюкозе),
2. Далее глюкоза аэробно окисляется, при этом скорость окисления глюкозы линейно зависит от ее количества,
3. В результате нарабатывается АТФ, количество которого также прямо зависит от концентрации глюкозы в крови,
4. Накопление АТФ стимулирует закрытие ионных K + -каналов, что приводит к деполяризации мембраны,
5. Деполяризация мембраны приводит к открытию потенциал-зависимых Ca 2+ -каналов и притоку ионов Ca 2+ в клетку,
6. Поступающие ионы Ca 2+ активируют фосфолипазу C и запускают кальций-фосфолипидный механизм проведения сигнала с образованием ДАГ и инозитол-трифосфата (ИФ3),
7. Появление ИФ3 в цитозоле открывает Ca 2+ -каналы в эндоплазматической сети, что ускоряет накопление ионов Ca 2+ в цитозоле,
8. Резкое увеличение концентрации в клетке ионов Ca 2+ приводит к перемещению секреторных гранул к плазматической мембране, их слиянию с ней и экзоцитозу кристаллов зрелого инсулина наружу,
9. Далее происходит распад кристаллов, отделение ионов Zn 2+ и выход молекул активного инсулина в кровоток.
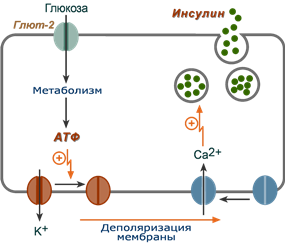
Схема внутриклеточной регуляции синтеза инсулина при участии глюкозы
Описанный ведущий механизм может корректироваться в ту или иную сторону под действием ряда других факторов, таких как аминокислоты, жирные кислоты, гормоны ЖКТ и другие гормоны, нервная регуляция .
Из аминокислот на секрецию гормона наиболее значительно влияют лизин и аргинин. Но сами по себе они почти не стимулируют секрецию, их эффект зависит от наличия гипергликемии, т.е. аминокислоты только потенциируют действие глюкозы.
Свободные жирные кислоты также являются факторами, стимулирующими секрецию инсулина, но тоже только в присутствии глюкозы. При гипогликемии они оказывают обратный эффект, подавляя экспрессию гена инсулина.
Логичной является положительная чувствительность секреции инсулина к действию гормонов желудочно-кишечного тракта – инкретинов (энтероглюкагона и глюкозозависимого инсулинотропного полипептида), холецистокинина, секретина, гастрина, желудочного ингибирующего полипептида.
Клинически важным и в какой-то мере опасным является усиление секреции инсулина при длительном воздействии соматотропного гормона, АКТГ и глюкокортикоидов, эстрогенов, прогестинов. При этом возрастает риск истощения β-клеток, уменьшение синтеза инсулина и возникновение инсулинзависимого сахарного диабета. Такое может наблюдаться при использовании указанных гормонов в терапии или при патологиях, связанных с их гиперфункцией.
Нервная регуляция β-клеток поджелудочной железы включает адренергическую и холинергическую регуляцию. Любые стрессы (эмоциональные и/или физические нагрузки, гипоксия, переохлаждение, травмы, ожоги) повышают активность симпатической нервной системы и подавляют секрецию инсулина за счет активации α2-адренорецепторов. С другой стороны, стимуляция β2-адренорецепторов приводит к усилению секреции.
Также выделение инсулина повышается n.vagus, в свою очередь находящегося под контролем гипоталамуса, чувствительного к концентрации глюкозы крови.
Мишени
Рецепторы инсулина находятся практически на всех клетках организма, кроме нервных, но в разном количестве. Нервные клетки не имеют рецепторов к инсулину, т.к. последний просто не проникает через гематоэнцефалический барьер.
Механизм действия
После связывания инсулина с рецептором активируется ферментативный домен рецептора. Так как он обладает тирозинкиназной активностью, то фосфорилирует внутриклеточные белки – субстраты инсулинового рецептора. Дальнейшее развитие событий обусловлено двумя направлениями: MAP-киназный путь и ФИ-3-киназный механизмы действия (подробно).
При активации фосфатидилинозитол-3-киназного механизма результатом являются быстрые эффекты – активация ГлюТ-4 и поступление глюкозы в клетку, изменение активности “метаболических” ферментов – ТАГ-липазы, гликогенсинтазы, гликогенфосфорилазы, киназы гликогенфосфорилазы, ацетил-SКоА-карбоксилазы и других.
При реализации MAP-киназного механизма (англ. MAP – mitogen-activated protein) регулируются медленные эффекты – пролиферация и дифференцировка клеток, процессы апоптоза и антиапоптоза.
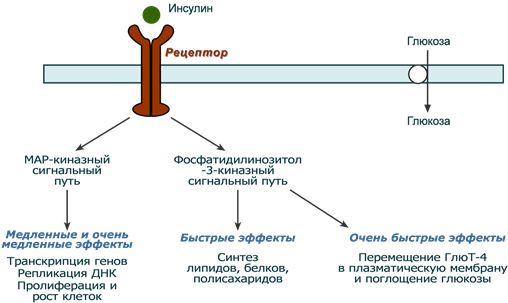
Два механизма действия инсулина
Скорость эффектов действия инсулина
Биологические эффекты инсулина подразделяются по скорости развития:
Очень быстрые эффекты (секунды)
Эти эффекты связаны с изменением трансмембранных транспортов :
1. Активации Na + /K + -АТФазы , что вызывает выход ионов Na + и вход в клетку ионов K + , что ведет к гиперполяризации мембран чувствительных к инсулину клеток (кроме гепатоцитов).
2. Активация Na + /H + -обменника на цитоплазматической мембране многих клеток и выход из клетки ионов H + в обмен на ионы Na + . Такое влияние имеет значение в патогенезе артериальной гипертензии при сахарном диабете 2 типа.
3. Угнетение мембранной Ca 2+ -АТФазы приводит к задержке ионов Ca 2+ в цитозоле клетки.
4. Выход на мембрану миоцитов и адипоцитов переносчиков глюкозы ГлюТ-4 и увеличение в 20-50 раз объема транспорта глюкозы в клетку.
Быстрые эффекты (минуты)
Быстрые эффекты заключаются в изменении скоростей фосфорилирования и дефосфорилирования метаболических ферментов и регуляторных белков.
Печень
- торможение эффектов адреналина и глюкагона (фосфодиэстераза),
- ускорение гликогеногенеза (гликогенсинтаза),
- активация гликолиза (фосфофруктокиназа, пируваткиназа),
- превращение пирувата в ацетил-SКоА (ПВК-дегидрогеназа),
- усиление синтеза жирных кислот (ацетил-SКоА-карбоксилаза),
- формирование ЛПОНП,
- повышение синтеза холестерина (ГМГ-SКоА-редуктаза),
Мышцы
- торможение эффектов адреналина (фосфодиэстераза),
- стимулирует транспорт глюкозы в клетки (активация ГлюТ-4),
- стимуляция гликогеногенеза (гликогенсинтаза),
- активация гликолиза (фосфофруктокиназа, пируваткиназа),
- превращение пирувата в ацетил-SКоА (ПВК-дегидрогеназа),
- усиливает транспорт нейтральных аминокислот в мышцы,
- стимулирует трансляцию (рибосомальный синтез белков).
Жировая ткань
- стимулирует транспорт глюкозы в клетки (активация Глют-4),
- активирует запасание жирных кислот в тканях (липопротеинлипаза),
- активация гликолиза (фосфофруктокиназа, пируваткиназа),
- усиление синтеза жирных кислот (активация ацетил-SКоА-карбоксилазы),
- создание возможности для запасания ТАГ (инактивация гормон-чувствительной-липазы).
Медленные эффекты (минуты-часы)
Медленные эффекты заключаются в изменении скорости транскрипции генов белков, отвечающих за обмен веществ, за рост и деление клеток, например:
1. Индукция синтеза ферментов в печени
- глюкокиназы и пируваткиназы ( гликолиз ),
- АТФ-цитрат-лиазы, ацетил-SКоА-карбоксилазы, синтазы жирных кислот, цитозольной малатдегидрогеназы ( синтез жирных кислот ),
- глюкозо-6-фосфатдегидрогеназы ( пентозофосфатный путь ),
2. Индукция в адипоцитах синтеза глицеральдегидфосфат-дегидрогеназы и синтазы жирных кислот.
3. Репрессия синтеза мРНК, например, для ФЕП-карбоксикиназы ( глюконеогенез ).
4. Обеспечивает процессы трансляции, повышая фосфорилирование по серину рибосомального белка S6.
Очень медленные эффекты (часы-сутки)
Очень медленные эффекты реализуют митогенез и размножение клеток. Например, к этим эффектам относится
1. Повышение в печени синтеза соматомедина, зависимого от гормона роста.
2. Увеличение роста и пролиферации клеток в синергизме с соматомединами.
3. Переход клетки из G1-фазы в S-фазу клеточного цикла.
Инактивация инсулина
Удаление инсулина из циркуляции происходит после его связывания с рецептором и последующей интернализации (эндоцитоза) гормон-рецепторного комплекса, в основном в печени и мышцах. После поглощения комплекс разрушается и белковые молекулы лизируются до свободных аминокислот. В печени захватывается и разрушается до 50% инсулина при первом прохождении крови, оттекающей от поджелудочной железы. В почках инсулин фильтруется в первичную мочу и, после реабсорбции в проксимальных канальцах, разрушается.
Патология
Гипофункция
Инсулинзависимый и инсулиннезависимый сахарный диабет. Для диагностики этих патологий в клинике активно используют нагрузочные пробы и определение концентрации инсулина и С-пептида.
ВЛИЯНИЕ ИНСУЛИНА НА ОБМЕН ВЕЩЕСТВ
Инсулин оказывает влияние на все виды обмена веществ, способствует анаболическим процессам, увеличивает синтез гликогена, жиров и белков, тормозя эффекты многочисленных контринсулярных гормонов (глюкагона, катехоламинов, глюкокортикоидов и соматотропина).
Все эффекты инсулина подразделяются на 4 группы:
1. очень быстрые (через несколько секунд) – гиперполяризация мембран клеток (за исключением гепатоцитов), повышение проницаемости для глюкозы, активация Na + К + -АТФазы, входа К + и откачивания Na + , подавление Са 2+ – насоса и задержка Са 2+ ;
2. быстрые эффекты (в течение нескольких минут) – активация и торможение различных ферментов, подавляющих катаболизм и усиливающих анаболические процессы;
3. медленные процессы (в течение нескольких часов) – повышение поглощения аминокислот, изменение синтеза РНК и белков-ферментов;
4. очень медленные эффекты (то часов до суток) – активация митогенеза и размножения клеток.
Инсулин оказывает влияние практически на все органы и ткани, однако его главными мишенями служат печень, мышечная и жировая ткань.
Важнейшим эффектом инсулина в организме является увеличение в транспорта глюкозы через мембраны мышечных и жировых клеток путем облегченной диффузии по градиенту концентрации с помощью чувствительных к гормону мембранных белковых переносчиков, называемых ГЛЮТ. В мембранах разных видов клеток выявлены 6 типов ГЛЮТ, но только ГЛЮТ-4 – является инсулинзависимым и находится на мембранах клеток скелетных мышц, миокарда, жировой ткани.
Инсулин влияет на все виды обмена веществ и оказывает следующие эффекты:
– усиливает транспорт глюкозы через клеточную мембрану и ее утилизацию тканями, снижает уровень глюкозы крови
– подавляет распад и стимулирует синтез гликогена
– активирует процессы гликолиза
– угнетает липолиз, что приводит к снижению поступления свободных жирных кислот в кровоток
– препятствует образованию кетоновых тел в организме
– стимулирует синтез триглицеридов и жирных кислот из глюкозы
– повышает проницаемость мембран для аминокислот
– усиливает синтез иРНК
– стимулирует синтез и подавляет распад белка
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ ИНСУЛИНОТЕРАПИИ
1. Сахарный диабет I типа.
2. Резистентность к синтетическим пероральным сахароснижающим средствам при сахарном диабете II типа.
3. Декомпенсация сахарного диабета, вызванная различными факторами (острые сопутствующие заболевания, травмы, инфекции).
4. Гипергликемические комы.
5. Тяжелые поражения печени и почек при сахарном диабете II типа, когда невозможно применить синтетические пероральные сахароснижающие средства.
6. Плохое заживление ран.
7. Выраженное истощение.
ПОБОЧНЫЕ ЭФФЕКТЫ ИНСУЛИНА.
1. Гипогликемические реакции.
2. Липодистрофии в месте введения.
4. Местные и системные аллергические реакции.
ПРОТИВОПОКАЗАНИЯ.
1. Заболевания, протекающие с гипогликемией.
2. Амилоидоз почек.
3. Язва желудка и двенадцатиперстной кишки.
4. Декомпенсированные пороки сердца.
ПРОИЗВОДНЫЕ СУЛЬФОНИЛМОЧЕВИНЫ
I поколение II поколение
Бутамид Глибенкламид (Манинил, Даонил)
Толбутамид Глипизид (Антидиаб, Глибенез)
Хлорпропамид Гликлазид (Диабетон)
Гликвидон (Глюренорм)
Глимепирид (Амарил)
МЕГЛИТИНИДЫ
Репаглинид –произв. бензойной кислоты
Натеглинид –произв. D-фенилаланина
МЕХАНИЗМ ДЕЙСТВИЯ
– стимулируют β-клетки поджелудочной железы и повышают выработку эндогенного инсулина.
– снижают активность инсулиназы.
– тормозят связывание инсулина с антителами и белками плазмы крови.
– снижают активность фосфорилазы и тормозят гликогенолиз.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Сахарный диабет II типа (при невозможности компенсации гипергликемии диетой).
ПОБОЧНЫЕ ЭФФЕКТЫ
1. Гипогликемические реакции.
2. Увеличение массы тела.
3. Повышение чувствительности к алкоголю.
5. Тошнота, рвота.
6. При длительном применении – нарушение функции печени и почек.
7. Нарушение кроветворения: агранулоцитоз, тромбопения, гемолитическая анемия.
8. Аллергические реакции.
9. Фотосенсибилизация (фотодерматоз).
ПРОТИВОПОКАЗАНИЯ
1. Сахарный диабет I типа и все диабетические комы.
2. Выраженные нарушения функции печени и/или почек.
3. Беременность, лактация.
4. Повышенная чувствительность к производным сульфонилмочевины.
БИГУАНИДЫ
Буформин (Адебит, Глибутид)
Метформин (Сиофор, Глюкофаг)
МЕХАНИЗМ ДЕЙСТВИЯ
Тормозят инактивацию эндогенного инсулина, снижают всасывание углеводов в кишечнике, повышают потребление глюкозы клетками без образования гликогена и стимулируют анаэробный гликолиз.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Сахарный диабет II типа (особенно в сочетании с ожирением).
ПОБОЧНЫЕ ЭФФЕКТЫ
2. Диспепсические явления.
3. Металлический привкус во рту.
5. Мегалобластическая анемия (редко).
6. Лактоацидоз (буформин).
ПРОТИВОПОКАЗАНИЯ
1. Сахарный диабет I типа и все диабетические комы.
2. Нарушения функции почек.
3. Любые состояния, сопровождающиеся гипоксией.
5. Наличие лактоацидоза в анамнезе.
6. Хронический алкоголизм.
7. Операции и травмы.
8. Заболевания печени или повышение активности печеночных ферментов в 2 и более раза по сравнению с нормой.
9. Период повышенных физических нагрузок.
10 Беременность, лактация.
ПРОИЗВОДНЫЕ ТИАЗОЛИДИНДИОНА
Розиглитазон
Пиоглитазон (актос)
МЕХАНИЗМ ДЕЙСТВИЯ
Повышают чувствительность тканей к инсулину. Взаимодействуют со специфическими ядерными рецепторами, что транскрипцию некоторых инсулинчувствительных генов и в итоге снижается резистентность к инсулину. Повышают захват тканями глюкозы, жирных кислот, усиливают липогенез, угнетают глюконеогенез.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Сахарный диабет II типа, на фоне недостаточности продукции эндогенного инсулина, а также при развитии инсулинорезистентности.
ПОБОЧНЫЕ ЭФФЕКТЫ
1. Гипогликемические реакции.
4. Аллергические реакции.
ПРОТИВОПОКАЗАНИЯ
1. Диабетические комы.
2. Выраженные нарушения функции печени и почек.
3. Беременность, лактация.
Акарбоза (Глюкобай)
МЕХАНИЗМ ДЕЙСТВИЯ
– угнетают интестинальные α-гликозидазы, что приводит к замедлению усвоения углеводов и снижению поглощения глюкозы из сахаридов
– снижают суточные колебания содержания глюкозы в крови
– усиливают действие диабетической диеты
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Сахарный диабет II типа (при невозможности компенсации гипергликемии диетой).
ПОБОЧНЫЕ ЭФФЕКТЫ
2. Боли в эпигастральной области.
4. Аллергические реакции (редко).
ПРОТИВОПОКАЗАНИЯ
1. Хронические заболевания кишечника, протекающие с выраженными нарушениями пищеварения и абсорбции (неспецифический язвенный колит).
2. Грыжи больших размеров.
3. Сужение и язвы кишечника.
4. Беременность и лактация.
ИНКРЕТИНОМИМЕТИКИ
Инкретины –это гормоны, которые секретируются некоторыми типами клеток тонкого кишечника в ответ на прием пищи и стимулируют секрецию инсулина.
Выделяют 2 гормона.
1.Глюкозозависимый инсулинотропный пептид (ГИП)
2. Глюкогонподобный полипептид (ГПП-1)
При экзогенном введении инкретинов на фоне сахарного диабета 2 типа только ГПП-1 проявлял достаточный инсулинотропный эффект, в связи с чем подходил для создания препаратов на его основе.
Созданные препараты можно разделить на 2 группы:
1. Вещества, имитирующие действие ГПП-1 – аналоги ГПП-1
2. Вещества, пролонгирующие действие эндогенного ГПП-1 вследствие блокады дипептидилпептидазы-4 (ДПП-4) – вермента, разрушающего ГПП-1– Ингибиторы ДПП-4
ИНКРЕТИНОМИМЕТИКИ
1.Аналоги глюкогонподобного полипептида-1 (ГПП-1)
МЕХАНИЗМ ДЕЙСТВИЯ
Стимулирует рецепторы к глюкагонподобному полипептиду-1 и вызывает следующие эффекты:
1.Улучшают функцию β-клеток поджелудочной железы, усиливают глюкозозависимую секрецию инсулина. Секреция инсулина прекращается по мере того, как снижается концентрация глюкозы в крови (т.е. снижается риск развития гипогликемии).
2. Восстанавливают или значительно усиливают как 1-ю так и 2-ю фазу инсулинового ответа.
3. Подавляют избыточную секрецию глюкагона, но не нарушают нормального глюкагонового ответа на гипогликемию.
4. Уменьшают чувство голода
2. Ингибиторы дипептидилпептидазы -4 (ДПП-4)
Ситаглиптин (Янувия)
Вилдаглиптин (Галвус)
Саксаглиптин
МЕХАНИЗМ ДЕЙСТВИЯ
Подавляя действие фермента ДПП-4, увеличивают уровень и продолжительность жизни эндогенных глюкозозависимого инсулинотропного пептида (ГИП) и ГПП-1, способствуя усилению их физиологического инсулинотропного действия.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Сахарный диабет II типа
– монотерапия: в качестве дополнения к диете и физическим нагрузкам;
– комбинированная терапия в сочетании с другими сахароснижающими средствами.
ПОБОЧНЫЕ ЭФФЕКТЫ
1. Тошнота, рвота, диарея
2. Снижение аппетита
3. Боли в эпигастральной области
6. Головная боль
ПРОТИВОПОКАЗАНИЯ
1. Сахарный диабет I типа и диабетические комы
2. Беременность, лактация
3.Нарушение функции печени
4. Сердечная недостаточность.
5. Воспалительные заболевания кишечника
6. Детский и подростковый возраст до 18 лет.
7. Повышенная чувствительность к препаратам.
ЭСТРОГЕННЫЕ ПРЕПАРАТЫ
1. Эстрогенные препараты стероидного строения:
ЭСТРАДИОЛ (дерместрил, климара, прогинова)
2. Эстрогенные препараты нестероидного строения:
ДИЭТИЛСТИЛЬБЭСТРОЛ
СИГЕТИН
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Патологические состояния, связанные с недостаточной функцией яичников:
1. Первичная и вторичная аменорея.
2. Гипоплазия половых органов и вторичных половых признаков.
3. Климактерические и посткастрационные расстройства.
5. Слабость родовой деятельности.
6. Профилактика и лечение остеопороза у женщин в период менопаузы.
7. Гипертрофия и рак предстательной железы у мужчин (синтетические препараты нестероидной структуры).
8. Пероральная и имплантируемая контрацепция.
АНТИЭСТРОГЕННЫЕ ПРЕПАРАТЫ
МЕХАНИЗМ ДЕЙСТВИЯ
1. Блокируют эстрогеновые рецепторы и устраняют действие эстрогенов.
2. Блокируя эстрогеновые рецепторы в гипоталамусе и гипофизе, нарушают систему обратной связи, что приводит к усилению выработки гонадотропных гормонов и, как следствие, увеличению размеров яичников и повышению их функции.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
1. Ановуляторная дисфункция яичников и связанное с ней бесплодие.
2. Дисфункциональное маточное кровотечение.
3. Дисгонадотропные формы аменореи.
4. Андрогенная недостаточность.
6. Задержка полового и физического развития у подростков мужского пола.
Последнее изменение этой страницы: 2016-04-26; Нарушение авторского права страницы
Механизм действия инсулина
Инсулин является гормоном, имеющим пептидную природу и образующимся в клетках поджелудочной железы. Он влияет на обменные процессы, происходящие в организме и охватывающие почти все ткани. Одна из его ключевых функций заключается в уменьшении в крови концентрации глюкозы, поэтому недостаток этого гормона часто провоцирует развитие такой патологии, как сахарный диабет. При абсолютной нехватке инсулина у пациента развивается заболевание 1 типа, а при относительной недостаточности гормона возникает диабет 2 типа.
Инсулин: состав гормона
Образующийся в поджелудочной железе гормон является предшественником инсулина. В процессе нескольких последовательных друг за другом химических реакций он преобразуется в активную форму гормона, которая способна выполнять предназначенные для нее функции в организме.
Каждая молекула инсулина имеет в своем составе 2 полипептидные цепи, связанные дисульфидными мостиками (С-пептидом):
- А-цепь. Она включает в себя 21 аминокислотный остаток.
- В-цепь. В ее состав входит 30 аминокислотных остатков.
 Инсулин отличается высокой скоростью оказываемого действия, поэтому в течение часа с момента выработки синтезируется. Стимулом для производства гормона является поступление пищи с большим количеством углеводов, в результате чего происходит скачок в крови значения глюкозы.
Инсулин отличается высокой скоростью оказываемого действия, поэтому в течение часа с момента выработки синтезируется. Стимулом для производства гормона является поступление пищи с большим количеством углеводов, в результате чего происходит скачок в крови значения глюкозы.
Инсулин у каждого биологического вида имеет структурные отличия, поэтому его роль в регулировании углеводного обмена тоже разная. Наиболее схожим с человеческим гормоном считается инсулин свиньи, отличающийся от него лишь 1 аминокислотным остатком. Инсулин быка отличается от гормона человека тремя такими остатками.
Как регулируется значение глюкозы в крови?
Оптимальная концентрация сахара поддерживается благодаря выполнению всеми системами организма своих функций. Тем не менее, главная роль в таком процессе принадлежит действию гормонов.
На концентрацию глюкозы воздействуют 2 группы гормонов:
- Инсулин (естественный гипергликемический гормон) – снижает ее уровень.
- Гормоны гипергликемической группы (например, гормон роста, глюкагон, адреналин) – увеличивают ее уровень.
В тот момент, когда значение глюкозы становится ниже физиологического уровня, выработка инсулина замедляется. В случае критического падения сахара в крови, начинается высвобождение гормонов гипергликемической группы, которые направляют глюкозу из клеточных запасов. Для подавления дальнейшего выделения в кровь инсулина активизируются гормоны стресса и адреналин.
На выработку, действие инсулина или утрату восприимчивости клеточных мембран к этому гормону могут оказать влияние следующие факторы:
- Нарушение процесса созревания инсулина, а также его рецептора;
- Возникновение измененных молекул, а также нарушение их биологических функций;
- Присутствие в организме антител к действию гормона, что приводит к потере связи между гормоном и его рецептором;
- Деградация рецепторов гормона;
- Нарушение процесса эндоцитоза гормона с рецептором.
Любое препятствие на пути поступления сигнала от инсулина в клетку способно полностью или частично нарушить его влияние на весь процесс метаболизма. Важно понимать, что в таком состоянии организма высокая концентрация гормона не может исправить ситуацию.
Влияние инсулина и его роль
Инсулин выполняет важные функции в организме и оказывает многогранное действие на обменные процессы.
Воздействие гормона в зависимости от оказанного эффекта принято делить на 3 основные группы:
- Анаболическое;
- Метаболическое;
- Антикатаболическое.
Метаболическое воздействие проявляется следующим образом:
- Усиливается поглощение клетками поступающих в организм веществ. Глюкоза является одним из важных компонентов, поэтому ее усвоение позволяет регулировать в крови уровень сахара.
- Повышается объем синтеза такого полисахарида, как гликоген.
- Снижается интенсивность гликогенеза (уменьшается формирование глюкозы в печени из различных веществ).
Анаболическое действие гормона призвано усилить биосинтез белковых компонентов и репликацию ДНК (дезоксирибонуклеи́новой кислоты). Инсулин под влиянием этого свойства помогает превратить глюкозу в такие органические соединения, как триглицериды. Это позволяет создать условия, необходимые для скопления жиров в момент недостатка гормона.
Антикатаболическое влияние охватывает 2 направления:
- Понижает степень гидролиза белков (деградации);
- Сокращает проникновение жирных кислот в кровяные клетки;
- Под воздействием инсулина в крови сохраняется нормальный уровень сахара
Эффект от воздействия инсулина проявляется через специальный рецептор и возникает спустя разное по продолжительности время:
- Через короткий период (минуту или даже секунды), когда выполняются функции транспортировки, ингибирование ферментов, синтез рибонуклеиновой кислоты, фосфорилирование белков;
- Спустя длительное время (до нескольких часов) в случае синтеза ДНК, белка и процесса клеточного роста.
Как действует гормон?
Инсулин участвует практически во всех процессах обмена, но основное его действие касается метаболизма углеводов. Влияние на эти вещества, оказываемое гормоном, связано во многом с усилением скорости доставки через клеточные мембраны излишек глюкозы. В результате этого активизируются инсулиновые рецепторы, и приводится в действие внутриклеточный механизм, способный влиять напрямую на усвоение клетками глюкозы. Механизм действия инсулина основан на урегулировании численности мембранных белков, доставляющих эти вещества.
Транспортировка глюкозы тканям полностью зависит от инсулина. Эти ткани имеют огромное значение для человеческого организма и отвечают за такие важные функции, как дыхание, движение, кровообращение и формирование запаса энергии, выделенной из поступившей пищи.
Рецепторы гормона, расположенные в клеточной мембране, имеют следующий состав:
- Альфа-субъединицы (2 штуки). Они расположены вне клетки.
- Бета-субъединицы (2 штуки). Они пересекают клеточную мембрану, затем переходят в цитоплазму.
Эти составляющие образованы двумя полипептидными цепочками, соединены между собой дисульфидными связями и характеризуются тирозинкиназной активностью.
После связи рецептора с инсулином происходят такие события, как:
- Конформация рецептора подлежит изменению, затрагивая сначала только а-субъединицу. В результате такого взаимодействия появляется тирозинкиназная активность у второй субъединицы (бета), запускается цепь реакций для усиления действия ферментов.
- Рецепторы в процессе соединения между собой формируют микроагрегаты или пятна.
- Происходит интернализация рецепторов, в результате чего появляется соответствующий сигнал.
Если инсулин содержится в плазме в больших количествах, то численность рецепторов сокращается, а чувствительность клеток к гормону падает. Снижение регуляции числа рецепторов объясняется их потерей в период проникновения инсулина в клеточную мембрану. В результате такого нарушения возникает ожирение или развивается такое заболевание, как сахарный диабет (чаще всего 2 типа).
Виды гормона и продолжительность его действия
Кроме естественного инсулина, вырабатываемого поджелудочной железой, некоторым людям приходится применять гормон в форме лекарственного препарата. Средство поступает в клетки путем выполнения соответствующих подкожных инъекций.
Продолжительность действия такого инсулина делится на 3 категории:
- Начальный период, когда инсулин попадает в кровь пациента. В это время гормон имеет сахароснижающий эффект.
- Пик. В этот период достигается максимальная точка снижения глюкозы.
- Длительность. Этот промежуток длится дольше, чем предыдущие периоды. За это время уменьшается содержание в крови сахара.
В зависимости от продолжительности эффекта от инсулина, применяемый в медицине гормон может быть следующих видов:
- Базальный. Он действует целые сутки, поэтому в день достаточно одной инъекции. У базального гормона отсутствует пик действия, он не понижает сахар на какое-то время, а позволяет поддерживать фоновое значение глюкозы в течение всего дня.
- Болюсный. Гормон является более оперативным средством воздействия на значение в крови глюкозы. Попадая в кровь, он сразу производит необходимый эффект. Пик действия болюсного гормона приходится как раз на приемы пищи. Он используется пациентами диабета первого типа, чтобы скорректировать уровень сахара с помощью соответствующей дозы инъекции.
Дозировка инсулина не должна рассчитываться пациентами с диабетом самостоятельно. Если количество единиц гормона значительно превысит норму, то может случиться даже летальный исход. Спасти жизнь можно будет только в случае пребывания пациента в ясном сознании. Для этого нужно сделать инъекцию глюкозы еще до наступления диабетической комы.
Инъекции гормона: распространенные ошибки
Эндокринологам часто приходится слышать во время практики жалобы от пациентов на неэффективность инъекций инсулина. Сахар в крови может и не снизиться, если в процессе введения гормона была нарушена техника.
Спровоцировать это могут следующие факторы:
- Использование просроченного инсулина, когда уже истек срок годности.
- Нарушение основных правил транспортировки и условий хранения препарата.
- Смешивание разных типов гормона в 1 флаконе.
- Попадание воздуха в подготовленный для инъекции шприц.
- Нанесение спирта на участок для инъекции, что приводит к разрушению инсулина.
- Применение поврежденного шприца или иглы во время инъекции.
- Быстрое извлечение иглы сразу после введения гормона, что могло привести к потере части лекарства. В результате в организм инсулин поступил в недостаточном количестве. Такая ошибка может стать причиной гипергликемии (резкому подъему сахара). В противном случае, когда инсулина поступило больше, чем требовалось для нейтрализации глюкозы, наступает гипогликемия (падение сахара). Оба состояния опасны для пациентов, страдающих диабетом.
Инсулин: роль в обмене углеводов

Для организма важны все вещества, поступающие из кишечника с пищей. Они участвуют в обмене веществ и выполняют определенные функции. Метаболизм углеводов контролируется рядом гормонов, основным из которых является инсулин. Это белковое соединение, которое синтезируют бета-клетки в поджелудочной железе. Влияние инсулина распространяется на большинство клеток организма. Он контролирует поступление в них глюкозы, которая доставляется в организм с питанием, а затем перерабатывается в энергию для жизнедеятельности. Ведущая роль этого гормона — контроль за постоянным уровнем сахара в крови. При недостатке глюкозы организм «голодает», но и избыточное ее количество также опасно для здоровья.
Поддержание сахара в крови

Основная функция инсулина в организме — «открывать» клетки для проникновения внутрь них глюкозы, что позволяет им полноценно работать, синтезировать энергию и усваивать необходимые для функционирования нутриенты. Инсулин выделяется из бета-клеток под действием сигналов, поступающих из тканей. Углеводы, поступающие с привычным питанием, расщепляются до простых соединений и всасываются в кишечнике, таким образом повышается сахар в крови. Для нормального функционирования тела необходимо поддержание строго заданного уровня сахара в крови, колеблющегося в физиологических пределах от 3.3 до 5.5 ммоль/л натощак и несколько выше после еды. Именно инсулин является тем физиологическим регулятором, который поддерживает сахар в крови на оптимальном уровне, переводя поступающие углеводы из плазмы внутрь клеток. Как только уровень глюкозы в плазме снижается до нормы, активное действие инсулина блокируется. При сильно выраженном снижении сахара в крови, например, когда питание длительно не поступает, включается в работу другой гормон (глюкагон), он «достает» глюкозу из резервных фондов — гликогена печени.
Нормальный обмен веществ и патологии
Если организм здоров, обмен веществ не нарушен, на фоне полноценного и рационального питания уровень глюкозы плазмы колеблется в пределах физиологических норм, что никак не влияет на здоровье и самочувствие. За счет активной работы поджелудочной железы, стимулирующейся физиологическими импульсами, количество выделяемого инсулина строго соответствует уровню углеводов плазмы. Клеткам и тканям поступает сигнал: можно израсходовать строго определенное количество глюкозы, часть ее оставить в плазме, а избыток запасти в виде гликогена в печени. Это позволяет поддерживать оптимальный обмен веществ, и организм не страдает от голода и избытка веса. Данный механизм регуляции уровня глюкозы за счет выработки инсулина кране важен для здорового обмена веществ и профилактики патологий. Избыток глюкозы крайне негативно влияет на многие органы и ткани. Особенно сильно от гипергликемии (это избыток глюкозы плазмы) страдают мелкие сосуды и почки, печень и нервы, а также головной мозг. Данное состояние можно наблюдать на примере болезни, связанной с расстройством обмена веществ — сахарного диабета. Основу его составляет проблема с выработкой инсулина или чувствительностью к нему тканей, из-за чего формируется хроническое повышение глюкозы крови (гипергликемия).
Инсулин
Ткани организма по чувствительности к инсулину делятся на два типа:
1. инсулинзависимые – соединительная, жировая, мышцы; в меньшей степени чувствительна к инсулину ткань печени;
2. инсулиннезависимые – нервная ткань, эритроциты, эпителий кишечника, почечные канальцы, семенники.
Метаболические эффекты инсулина разнообразны – регуляция обмена углеводов, липидов и белков. В норме инсулин выделяется в кровь после приема пищи и ускоряет анаболические процессы: синтез белков и веществ, являющихся резервом энергии (гликоген, липиды). Это единственный гормон, снижающий концентрацию глюкозы в крови.
Влияние инсулина на углеводный обмен:
1. увеличивает проницаемость клеточных мембран для глюкозы;
2. индуцирует синтез глюкокиназы, тем самым ускоряет фосфорилирование глюкозы в клетке;
3. повышает активность и количество ключевых ферментов гликолиза (фосфофруктокиназы, пируваткиназы)
4. стимулирует синтез гликогена за счет активации гликогенсинтазы и уменьшает распад гликогена;
5. ингибирует глюконеогенез, подавляя синтез ключевых ферментов глюконеогенеза;
6. повышает активность пентозофосфатного пути.
Общий результат стимуляции этих процессов – снижение концентрации глюкозы в крови. Около 50% глюкозы используется в процессе гликолиза, 30–40 % превращается в липиды и около 10 % накапливается в форме гликогена.
Влияние инсулина на метаболизм липидов:
1. ингибирует липолиз (распад триацилглицеролов) в жировой ткани и печени;
2. стимулирует синтез триацилглицеролов в жировой ткани;
3. активирует синтез жирных кислот;
4. в печени ингибирует синтез кетоновых тел.
Влияние инсулина на метаболизм белков:
1. стимулирует транспорт аминокислот в клетки мышц, печени;
2. активирует синтез белков в печени, мышцах, сердце и уменьшает их распад;
3. стимулирует пролиферацию и число клеток в культуре и, вероятно, может участвовать в регуляции роста in vivo.
Гипофункция поджелудочной железы
При недостаточной секреции инсулина развивается сахарный диабет. Выделяют два типа сахарного диабета: инсулинзависимый (тип I) и инсулиннезависимый (тип II).
Инсулинзависимый сахарный диабет (у 10% больных) – заболевание, вызываемое разрушением ?-клеток островков Лангерганса. Характеризуется абсолютным дефицитом инсулина.
Инсулиннезависимый сахарный диабет (у 90% больных) развивается чаще всего у тучных людей. Основная причина – снижение чувствительности рецепторов к инсулину, повышенная скорость катаболизма инсулина, нарушение регуляции секреции гормона. При этом уровень инсулина в крови – в норме. Факторы риска развития заболевания – генетическая предрасположенность, ожирение, гиподинамия, стресс.
Симптомы сахарного диабета: гипергликемия – повышение концентрации глюкозы в крови; глюкозурия – выведение глюкозы с мочой; кетонемия – повышение в крови концентрации кетоновых тел; кетонурия – выведение кетоновых тел с мочой; полиурия – возрастает суточный диурез (в среднем до 3–4 л).
Накопление кетоновых тел снижает буферную емкость крови, что приводит к ацидозу. Активируются катаболические процессы: распад белков, липидов, гликогена; повышается концентрация в крови аминокислот, жирных кислот, липопротеинов.
Гиперфункция поджелудочной железы
Инсулинома – опухоль ?-клеток островков Лангерганса, сопровождается повышенной выработкой инсулина, выраженной гипогликемией, судорогами, потерей сознания. При крайней степени гипогликемии может наступить смертельный исход. Устранить гиперинсулинизм можно введением глюкозы и гормонами, повышающими уровень глюкозы (глюкагон, адреналин).
Инсулин: образование, секреция и действие
Инсулин (от лат. insula — остров) — это гормон пептидной природы, образуется в бета-клетках островков Лангерганса поджелудочной железы. Оказывает многогранное влияние на обмен практически во всех тканях. Основное действие инсулина заключается в снижении концентрации глюкозы в крови.

Инсулин увеличивает проницаемость плазматических мембран для глюкозы, активирует ключевые ферменты гликолиза, стимулирует образование в печени и мышцах из глюкозы гликогена, усиливает синтез жиров и белков. Кроме того, инсулин подавляет активность ферментов, расщепляющих гликоген и жиры. То есть, помимо анаболического действия, инсулин обладает также и антикатаболическим эффектом.
Нарушение секреции инсулина вследствие деструкции бета-клеток — абсолютная недостаточность инсулина — является ключевым звеном патогенеза сахарного диабета 1-го типа. Нарушение действия инсулина на ткани — относительная инсулиновая недостаточность — имеет важное место в развитии сахарного диабета 2-го типа.
Образование и секреция инсулина
Главным стимулом к синтезу и выделению инсулина служит повышение концентрации глюкозы в крови.
Синтез инсулина в клетке
Синтез и выделение инсулина представляют собой сложный процесс, включающий несколько этапов. Первоначально образуется неактивный предшественник гормона, который после ряда химических превращений в процессе созревания превращается в активную форму.
Ген, кодирующий первичную структуру предшественника инсулина, локализуется в коротком плече 11 хромосомы.
На рибосомах шероховатой эндоплазматической сети синтезируется пептид-предшественник — т.н. препроинсулин. Он представляет собой полипептидную цепь, построенную из 110 аминокислотных остатков и включает в себя расположенные последовательно: L-пептид, B-пептид, C-пептид и A-пептид.
Почти сразу после синтеза в ЭПР от этой молекулы отщепляется сигнальный (L) пептид — последовательность из 24 аминокислот, которые необходимы для прохождения синтезируемой молекулы через гидрофобную липидную мембрану ЭПР. Образуется проинсулин, который транспортируется в комплекс Гольджи, далее в цистернах которого происходит так называемое созревание инсулина.
Созревание является наиболее длительным этапом образования инсулина. В процессе созревания из молекулы проинсулина с помощью специфических эндопептидаз вырезается C-пептид — фрагмент из 31 аминокислоты, соединяющий B-цепь и A-цепь. То есть молекула проинсулина разделяется на инсулин и биологически инертный пептидный остаток.
В секреторных гранулах инсулин, соединяясь с ионами цинка, образует кристаллические гексамерные агрегаты.
Регуляция образования и секреции инсулина
Главным стимулятором освобождения инсулина является повышение уровня глюкозы в крови. Дополнительно образование инсулина и его выделение стимулируется во время приёма пищи, причём не только глюкозы или углеводов. Секрецию инсулина усиливают аминокислоты, особенно лейцин и аргинин, некоторые гормоны гастроэнтеропанкреатической системы: холецистокинин, ГИП, ГПП-1, а также такие гормоны, как глюкагон, АКТГ, СТГ, эстрогены и др., препараты сульфонилмочевины. Также секрецию инсулина усиливает повышение уровня калия или кальция, свободных жирных кислот в плазме крови.
Понижается секреция инсулина под влиянием соматостатина.
Бета-клетки также находятся под влиянием автономной нервной системы:
-
- Парасимпатическая часть (холинергические окончания блуждающего нерва) стимулирует выделение инсулина;
-
- Симпатическая часть (активация ?2-адренорецепторов) подавляет выделение инсулина.
Причём синтез инсулина заново стимулируется глюкозой и холинергическими нервными сигналами.
Действие инсулина
Так или иначе инсулин затрагивает все виды обмена веществ во всём организме. Однако в первую очередь действие инсулина касается именно обмена углеводов. Основное влияние инсулина на углеводный обмен связано с усилением транспорта глюкозы через клеточные мембраны. Активация инсулинового рецептора запускает внутриклеточный механизм, который напрямую влияет на поступление глюкозы в клетку путём регуляции количества и работы мембранных белков, переносящих глюкозу в клетку.
В наибольшей степени от инсулина зависит транспорт глюкозы в двух типах тканей: мышечная ткань (миоциты) и жировая ткань (адипоциты) — это т.н. инсулинозависимые ткани. Составляя вместе почти 2/3 всей клеточной массы человеческого тела, они выполняют в организме такие важные функции как движение, дыхание, кровообращение и т. п., осуществляют запасание выделенной из пищи энергии.
Механизм действия
Подобно другим гормонам своё действие инсулин осуществляет через белок-рецептор.
Инсулиновый рецептор представляет собой сложный интегральный белок клеточной мембраны, построенный из 2 субъединиц (a и b), причём каждая из них образована двумя полипептидными цепочками.
Инсулин с высокой специфичностью связывается и распознаётся а-субъединицей рецептора, которая при присоединении гормона изменяет свою конформацию. Это приводит к появлению тирозинкиназной активности у субъединицы b, что запускает разветвлённую цепь реакций по активации ферментов, которая начинается с самофосфорилирования рецептора.
Весь комплекс биохимических последствий взаимодействия инсулина и рецептора ещё до конца не вполне ясен, однако известно, что на промежуточном этапе происходит образование вторичных посредников: диацилглицеролов и инозитолтрифосфата, одним из эффектов которых является активация фермента — протеинкиназы С, с фосфорилирующим (и активирующим) действием которой на ферменты и связаны изменения во внутриклеточном обмене веществ.
Усиление поступления глюкозы в клетку связано с активирующим действием посредников инсулина на включение в клеточную мембрану цитоплазматических везикул, содержащих белок-переносчик глюкозы GluT 4.
Комплекс инсулин — рецептор после образования погружается в цитозоль и в дальнейшем разрушается в лизосомах. Причём деградации подвергается лишь остаток инсулина, а освобождённый рецептор транспортируется обратно к мембране и снова встраивается в неё.
Физиологические эффекты инсулина
Инсулин оказывает на обмен веществ и энергии сложное и многогранное действие. Многие из эффектов инсулина реализуются через его способность действовать на активность ряда ферментов.
Инсулин — это единственный гормон, снижающий содержание глюкозы в крови, это реализуется через:
-
- усиление поглощения клетками глюкозы и других веществ;
-
- увеличение интенсивности синтеза гликогена — инсулин форсирует запасание глюкозы клетками печени и мышц путём полимеризации её в гликоген;
-
- уменьшение интенсивности глюконеогенеза — снижается образование в печени глюкозы из различных веществ;
-
- усиливает поглощение клетками аминокислот (особенно лейцина и валина);
-
- усиливает транспорт в клетку ионов калия, а также магния и фосфата;
-
- усиливает репликацию ДНК и биосинтез белка;
-
- усиливает синтез жирных кислот и последующую их этерификацию — в жировой ткани и в печени инсулин способствует превращению глюкозы в триглицериды; при недостатке инсулина происходит обратное — мобилизация жиров;
-
- подавляет гидролиз белков — уменьшает деградацию белков;
-
- уменьшает липолиз — снижает поступление жирных кислот в кровь.
Регуляция уровня глюкозы в крови
Поддержание оптимальной концентрации глюкозы в крови — результат действия множества факторов, сочетание слаженной работы почти всех систем организма. Однако главная роль в поддержании динамического равновесия между процессами образования и утилизации глюкозы принадлежит гормональной регуляции.
В среднем уровень глюкозы в крови здорового человека колеблется от 2,7 до 8,3 ммоль/л, однако сразу после приёма пищи концентрация резко возрастает на короткое время.
Две группы гормонов противоположно влияют на концентрацию глюкозы в крови:
-
- Единственный гипогликемический гормон — инсулин;
-
- Гипергликемические гормоны (такие как глюкагон, гормон роста и адреналин), которые повышают содержание глюкозы в крови.
Когда уровень глюкозы опускается ниже нормального физиологического значения, высвобождение инсулина из B-клеток замедляется (но в норме никогда не останавливается). Если же уровень глюкозы падает до опасного уровня, высвобождаются так называемые контринсулярные (гипергилкемические) гормоны (наиболее известный — глюкагон ?-клеток панкреатических островков), которые вызывают высвобождение глюкозы из клеточных запасов в кровь. Адреналин и другие гормоны стресса сильно подавляют выделение инсулина в кровь.
Точность и эффективность работы этого сложного механизма является непременным условием нормальной работы всего организма, здоровья. Длительное повышенное содержание глюкозы в крови (гипергликемия) является главным симптомом и повреждающим фактором сахарного диабета. Гипогликемия — понижение содержания глюкозы в крови — часто имеет ещё более серьёзные последствия. Так, экстремальное падение уровня глюкозы может быть чревато развитием гипогликемической комы и смертью.
Гипергликемия
Гипергликемия — увеличение уровня сахара в крови.
В состоянии гипергликемии увеличивается поступление глюкозы как в печень, так и в перефирические ткани. Как только уровень глюкозы зашкаливает, поджелудочная железа начинает вырабатывать инсулин.
Гипогликемия
Гипогликемия — патологическое состояние, характеризующееся снижением уровня глюкозы периферической крови ниже нормы (обычно, 3,3 ммоль/л). Развивается вследствие передозировки сахароснижающих препаратов, избыточной секреции инсулина в организме. Гипогликемия может привести к развитию гипогликемической комы и привести к гибели человека.
Источники:
http://biokhimija.ru/gormony/insulin.html
http://infopedia.su/5xd14.html
http://diabet-med.su/mexanizm-dejstviya-insulina.html
http://medaboutme.ru/zdorove/publikacii/stati/sovety_vracha/insulin_rol_v_obmene_uglevodov/
http://bio.wikireading.ru/7806
http://www.shealth.ru/insulin.html
http://endokrinplus.ru/analizy-saharnyj-diabet


