Токсоплазмоз
Токсоплазмоз – это паразитарное заболевание, характеризующееся поражением нервной системы, глаз, скелетной мускулатуры и мышцы сердца, а также увеличением лимфоузлов, печени и селезенки. Склонно к хроническому течению.
Распространенность токсоплазмоза в мире невероятно высока, в основном за счет стран Африки, а также Латинской и Южной Америки, в которых инфицированность населения доходит до 90%. Показатели в Европе и Северной Америке ниже – 25-50% населения.
Что провоцирует / Причины Токсоплазмоза:
Возбудитель токсоплазмоза Toxoplasma gondii относится к типу простейших (Protozoa), классу споровиков (Sporozoa), отряду кокцидий (Coccidia). Токсоплазмы подвижны и имеют форму дуги, арки или напоминают дольку апельсина. Встречаются также овальные и округлые формы. Тип движения у токсоплазмы скользящий.
Патогенез (что происходит?) во время Токсоплазмоза:
Жизненный цикл токсоплазмы включает стадии полового и бесполого размножения. Токсоплазмоз распространен во многих странах. Человек заражается от домашних животных, чаще всего от кошек, которые являются окончательным хозяином паразита. В их организме происходит половое размножение возбудителя. Больные токсоплазмозом животные выделяют паразитов с мочой, слюной, молоком. Человек является промежуточным хозяином. Заражение происходит алиментарным (наиболее часто), капельным, через поврежденные кожу и слизистые оболочки, трансмиссивным (при укусе членистоногих) путем. Возможно, внутриутробное заражение при проникновении паразита от матери к плоду через плаценту. Токсоплазмой инфицированы от 50 до 80% взрослого населения.
Пути заражения токсоплазмозом
Заражение человека происходит при употреблении мясных продуктов и яиц, не прошедших достаточную термическую обработку. Не исключена возможность заражения при попадании возбудителя на слизистые оболочки и поврежденные кожные покровы, трансмиссивным и др. путём. Наблюдается и внутриутробное заражение.
Факторы, которые могут способствовать появлению в организме паразита и повышают риск возникновения токсоплазмоза:
• Дотрагиваться грязными руками до рта после контакта с землей, после уборки кошачьего туалета, или любого другого контакта с кошачьими экскрементами.
• Принимать в пищу сырое или не до конца приготовленное мясо, особенно свинину, мясо ягненка или оленину.
• Прикасаться ко рту после контакта с сырым или непрожаренным/непроваренным мясом.
• Пересадка органов или переливание крови (очень редко).
• Если женщина беременна, и она заразилась токсоплазмозом, инфекция может от нее передаться ребенку, что может привести к серьезным последствиям.
В организме человека токсоплазмы размножаются в кишечнике, распространяются лимфогенным и гематогенным путем. Фаза лимфогенного заноса (увеличиваются и воспаляются лимфатические узлы) сменяется гематогенной диссиминацией. Стадия нахождения паразита в крови короткая (несколько дней). Попадая во внутренние органы, токсоплазмы вызывают в них воспалительные явления. Особенно часто поражаются нервная система, сетчатка, печень, миокард. В этих органах токсоплазмы находятся внутриклеточно и экстрацеллюлярно. Скопления паразитов называются псевдоцистами. Токсоплазмы способны образовывать цисты в тканях, вызывая состояние латентной инфекции. Активизация паразита происходит при неблагоприятных для макроорганизма условиях и снижении его иммунологической реактивности. В патогенезе токсоплазмозного поражения нервной системы имеют значение очаговые воспалительные явления (некротизирующий энцефалит), дисциркуляторные нарушения, связанные с васкулитом, обструкция ликворных путей, приводящая к гидро- и микроцефалии.
Наиболее грубые морфологические изменения нервной системы наблюдаются у детей. При макроскопическом исследовании выявляется расширение желудочков с перивентрикулярной зоной некроза. Обнаруживаются рубцы, замещающие участки некроза, облитерация межжелудочкового отверстия и латеральной апертуры IV желудочка. Гидроцефалия может быть выражена, приводя к истончению и деформации вещества полушарий.
Морфологические проявления токсоплазмоза мозга у взрослых многообразны. При микроскопическом исследовании наиболее характерны рассеянные по всему головному и спинному мозгу милиарные гранулемы, состоящие из больших эпителиоидных клеток, лимфоцитов, моноцитов, иногда эозинофилов. Гранулемы содержат многочисленных паразитов, окружены зоной отека с некротическими очажками, обусловленными васкулитом. Типично для токсоплазмоза обызвествление мелких очагов. При наличии токсоплазм в субарахноидальном пространстве возникает серозно-продуктивный лептоменингит.
У большинства зараженных нет клинических проявлений заболевания. У части больных наблюдается вялотекущие хронические формы и крайне редко – острые, с тяжелым течением заболевания. При внутриутробном заражении в первые месяцы беременности часто происходит выкидыш и гибель плода. Не исключается возможность внутриутробных уродств плода и рождения детей с дефектами развития. Если заражение произошло в поздние сроки беременности, рождается ребенок с генерализованным токсоплазмозом.
Симптомы Токсоплазмоза:
Токсоплазмозом заболевают лица любого возраста, однако наиболее часто – дети. Выделяют приобретенный и врожденный токсоплазмоз.
Приобретенный токсоплазмоз. Инкубационный период – от 3 до 14 дней. Продромальный период с общим недомоганием, мышечными и суставными болями – обычно несколько недель, иногда месяцев. Острая стадия заболевания проявляется повышением температуры, ознобом, лимфоаденопатией. Появляется генерализованная макулопапулезная сыпь, отсутствующая только на подошвах, ладонях, волосистой части головы. Наряду с общими признаками инфекционного заболевания имеется клиническая картина поражения различных органов: миокардит, пневмония, очаговый некротический нефрит, гепатит. Поражение нервной системы проявляется менингитом, энцефалитом, менингоэнцефалитом, энцефаломиелитом. Редко наблюдаются радикулоневритическая и малосимптомная формы (последняя может быть обнаружена лишь с помощью серологических реакций).
Наиболее типичной формой токсоплазмоза является менингоэнцефалит, в клинической картине которого имеются общемозговые и менингеальные симптомы, парезы конечностей, тонико-клонические судороги, глазодвигательные (диплопия) и координаторные нарушения. Иногда развиваются одиночные или множественные токсоплазмозные абсцессы в головном мозге. Характерны расстройства сознания, летаргия, утрата памяти и ориентировки в пространстве. В крови обнаруживаются лейкоцитоз со сдвигом формулы влево, увеличение СОЭ, в цереброспинальной жидкости – лимфоцитарный плеоцитоз, умеренное увеличение содержания белка.
Выделяют острую, хроническую и латентную формы с подразделением последней на первично-латентную, без клинических проявлений, и вторично-латентную, возникающую после острой формы или рецидива хронической.
Острый токсоплазмоз характеризуется внезапным началом, лихорадкой, явлениями общей интоксикации. У больных отмечаются лимфаденопатия, макулопапулезная сыпь, увеличиваются печень, селезенка. Могут развиться признаки энцефалита, менингоэнцефалита и миокардита.
В зависимости от преобладающего синдрома выделяют энцефалитическую, тифоподобную и смешанную формы острого токсоплазмоза.
После стихания процесса острый токсоплазмоз переходит во вторично-хроническую или, реже, вторично-латентную формы.
Хронический токсоплазмоз может развиться как первично-хроническое, так и вторично-хроническое заболевание. Он характеризуется торпидным, длительным течением, при котором наблюдаются периоды обострения и ремиссии. Основные клинические симптомы – интоксикация, субфебрилитет, миалгии, артралгии. У больных отмечаются раздражительность, снижение памяти, невротические реакции. Частым симптомом является генерализованная лимфаденопатия. Вследствие мезаденита возникают ноющие боли и вздутие живота, запор, тошнота. К числу важных симптомов заболевания относятся специфический миозит (в толще мышц иногда можно прощупать уплотнения и даже кальцификаты) и миокардит. У многих больных обнаруживают признаки вегето-сосудистой дистонии, эндокринные нарушения (расстройства менструального цикла, импотенция, вторичная надпочечниковая недостаточность и др.). Нередко встречается поражение глаз в форме хориоретинита, ретинита, увеита. В периферической крови – лейкопения, нейтропения, относительный лимфоцитоз, тенденция к эозинофилии. СОЭ в пределах нормы.
Однако преобладающей формой течения приобретенного заболевания является латентный токсоплазмоз. Он чаще имеет первично-латентный и, значительно реже, вторично-латентный характер. Латентный токсоплазмоз диагностируется только при серологическом исследовании. Латентная и хроническая формы болезни могут переходить в тяжелое генерализованное течение, что встречается при ВИЧ-инфекции и других состояниях, приводящих к иммунодефициту. Наиболее часто у больных ВИЧ/СПИДом встречаются менингоэнцефалит и абсцессы мозга, вызванные токсоплазмами. В диагностике большое значение имеет компьютерная томография. В процесс также вовлекаются легкие, сердце, миокард и другие органы. Токсоплазмоз – одна из причин гибели больных ВИЧ/СПИДом.
Врожденный токсоплазмоз. При заболевании матери токсоплазмозом в первой половине беременности плод, как правило, погибает вследствие несовместимых с жизнью пороков развития. При инфицировании матери во второй половине беременности ребенок рождается с тяжелым поражением мозга. Острая стадия заболевания протекает внутриутробно, рождается ребенок с активно текущим менингоэнцефалитом или его последствиями. Неврологические проявления менингоэнцефалита разнообразны: полиморфные эпилептические припадки, клонико-тонические судороги, спастические парезы, тремор, миоклонии, парезы глазных и мимических мышц, нистагм, контрактуры мышц, менингеальные явления. Иногда имеются симптомы поражения спинного мозга.
Для врожденного токсоплазмоза характерна триада признаков: гидроцефалия, хориоретинит и интрацеребральные кальцификаты. При гидроцефалии увеличиваются размеры головы, кости черепа истончаются, роднички напряжены. Гидроцефалии обычно сопутствует микрофтальмия. Если гидроцефалия развивается до рождения ребенка, то в родах приходится прибегать к краниотомии. Однако во многих случаях увеличение объема головы не обнаруживается и гидроцефалия выявляется только при пневмоэнцефалографии. Хориоретинит часто бывает двусторонним, фокальным, включающим макулярную область. Возможны также ирит, увеит, катаракта, первичная или вторичная атрофия зрительных нервов. Интрацеребральные кальцификаты диаметром 1-3 см располагаются в коре и базальных ганглиях и выявляются на краниограммах КТ и МРТ головного мозга.
Дети с врожденным токсоплазмозом отстают в умственном развитии вплоть до олигофрении. У них наблюдаются также разнообразные психотические состояния (депрессия, психомоторное возбуждение, галлюцинации, кататония). Иногда у детей с врожденным токсоплазмозом обнаруживаются желтуха, увеличенные печень и селезенка. Температура обычно остается нормальной. Ликворное давление при люмбальной пункции обычно нормальное. Отмечается высокое содержание белка и умеренный мононуклеарный плеоцитоз, иногда ксантохромия.
Осложнения врожденного токсоплазмоза – следствие поражения мозга и глаз, ведущего к истощению, параличам, умственной отсталости, слепоте. Присоединение вторичной инфекции обусловливает развитие гнойного менингоэнцефалита и пиоцефалии. Смерть наступает от прогрессирующего поражения головного мозга.
Течение токсоплазмоза
Ранее считалось, что врожденный токсоплазмоз приводит к смерти в течении первых лет жизни ребенка. В настоящее время возможны стабилизация инфекции и даже полное выздоровление с остаточными явлениями, выраженность которых зависит от степени поражения центральной нервной системы (кальцификаты, хореоретинит, эпилептический синдром, отставание в умственном развитии и др.). У взрослых наряду с острым течением часто отмечается подострое или даже хроническое развитие заболевания. Нередко приобретенный токсоплазмоз, особенно у взрослых, протекает без выраженных в той или иной степени клинических симптомов (инаппарантная форма).
Диагностика Токсоплазмоза:
Диагноз токсоплазмоза устанавливают на основании комплекса показателей, которые включают клинические данные и результаты лабораторного подтверждения. Относительное значение имеют эпидемиологические предпосылки, такие как контакт с кошками, условия общения с ними, особенности пищевых привычек (употребление сырого, полусырого мяса, проба сырого фарша, немытых овощей, фруктов), соблюдение личных гигиенических навыков, профессия и др.
Чрезвычайное многообразие клинических проявлений, отсутствие симптомов, характерных только для токсоплазмоза, затрудняет клиническую диагностику и позволяет в определенных случаях только предположить диагноз, который формируется при проведении полноценной дифференциальной диагностики и при анализе результатов лабораторного исследования.
Методы лабораторной диагностики токсоплазмоза делят на две группы: паразитологические и иммунологические.
Паразитологические методы основаны на возможности обнаружения возбудителя или выделении его при заражении восприимчивых животных – биопроба.
К ним относится прямая микроскопия мазков – отпечатков пораженных органов (миндалины, биоптат лимфоузлов, головного мозга, внутренние органы погибших эмбрионов или плодов) или мазков из осадка спинномозговой жидкости, крови, окрашенных по Романовскому – Гимзе. Можно исследовать гистологические препараты этих органов.
К сожалению, технические сложности обнаружения post mortum, а также редкие случаи обнаружения токсоплазм в крови, спинномозговой жидкости затрудняют использование этих методов.
Биологическая проба на белых мышах, хомяках, зараженных исследуемым материалом и проведением последующих 5-6 слепых пассажей, требует особых условий содержания животных, лабораторий со специальным режимом работы и применяется только в научных целях.
В широкой практике используют преимущественно иммунологические методы, которые включают серологические реакции и внутрикожную пробу. Эти методы, достаточно специфичные и чувствительные, определяют, прежде всего, состояние инфицированности, а серореакции – и заболеваемости. Эти понятия неоднозначны, ибо заболеваемость во много раз ниже инфицированности.
Из методов серологической диагностики используют реакцию связывания комплемента (РСК), реакцию непрямой иммунофлюоресценции (РНИФ) и иммуноферментный анализ (ИФА). Диагноз подтверждается достоверным нарастанием титра антител – динамикой титров в парных сывороротках, взятых с интервалом 2-4 недели.
РСК становится положительной со 2-й недели после заражения и наибольших титров – 1:16 – 1:320 достигает через 2-4 месяца. Через 1-3 года может стать отрицательной или сохраниться в низких титрах (1:5, 1:10), которые не имеют самостоятельного значения.
РНИФ становится положительной с 1-й недели инфекции и максимальных показателей (1:1280 – 1:5000) достигает на 2- 4 месяце. В низких титрах 1:10 – 1: 40 может сохраняться 15-20 лет.
ИФА в соответствии с ориентацией на международный стандарт ВОЗ является наиболее объективным методом. О положительной реакции свидетельствуют оптические показатели более 1,5, в иммуноферметных единицах – больше 60; в международных – больше 125, в титрах антител – 1:1600 и больше.
Диагностика врожденного токсоплазмоза у ребенка начинается с акушерского анамнеза матери, эпиданамнеза и показателей серологических реакций. Обязательны консультации специалистов для дифференциации с герпетической, цитомегаловирусной, листериозной, хламидийной инфекциями, а также рентгенография черепа и обследование в медикогенетическом центре.
Следует напомнить, что 20 – 30% женщин имеют антитела – это здоровые носители антител. Они не требуют лечения. 70 – 80%, показавших отрицательные серореакции, составляют группу риска и нуждаются в повторном обследовании.
На протяжении первого года жизни ребенка необходимо проводить параллельные серологические обследования матери и ребенка в динамике.
Положительные реакции у матери и ребенка в первые три месяца жизни ребенка не дают оснований для постановки диагноза «токсоплазмоз» ребенку, т. к. специфические антитела в составе IgG передаются ребенку трансплацентарно. Для подтверждения диагноза врожденного токсоплазмоза у новорожденного применяют тест Ремингтона вариант РИФ с определением IgM, которые не проходят через плаценту. Их обнаружение свидетельствует об инфицированности плода.
Лечение Токсоплазмоза:
При остром токсоплазмозе используются химиотерапевтические препараты.
Делагил (по 0,5г 2 раза в сутки) в сочетании с сульфаниламидами (по 0,5г 2 раза в сутки) в течение 10 дней. Фансидар назначается в количестве 5 таблеток на курс: по 1 табл. через 2 дня или в виде внутримышечных инъекций по 1 ампуле в 2,5 мг один раз в 2 дня в количестве 5 инъекций. Проводится один или два курса лечения.
Из антибиотиков назначаются: линкомицина гидрохлорид (по 0,5г 2 раза в сутки); метациклина гидрохлорид (по 0,3г 2 раза в сутки) в течение 5-7 дней в сочетании с сульфаниламидами; ровамицин.
Лечение хронического токсоплазмоза во много раз труднее, чем острого, так как химиопрепараты не оказывает значительного эффекта. Главное место занимает гипосенсибилизирующая и иммуномодулирующая терапия. В комплекс лечения включают витамины, десенсибилизирующие средства, лидазу, церебролизин и пр.
Имеются данные о положительном действии левамизола в терапии хронического токсоплазмоза. Левамизол назначается по 150 мг 3 дня подряд с перерывами 1 нед между циклами, всего 2 – 3 цикла.
Профилактика Токсоплазмоза:
Профилактика инфицирования токсоплазмами заключается в употреблении в пищу только хорошо термически обработанного мяса и мясопродуктов, чисто вымытых овощей, фруктов и ягод. В процессе приготовления пищи запрещается пробовать на вкус сырой мясной фарш. Необходимо тщательно мыть руки после обработки сырых мясопродуктов, работе в саду, огороде, детям после игры на детской площадке и, особенно, в песочнице. Следует тщательно соблюдать санитарно-гигиенические правила содержания в квартире домашних животных, не забывая мыть руки после контактов с ними.
При наступлении беременности каждая женщина должна быть обследована на токсоплазмоз в женской консультации. При выявлении у беременной клинических проявлений токсоплазмоза, а также обнаружение антител к токсоплазмам класса IgM, следует решить вопрос о необходимости лечения или прерывания беременности.
К каким докторам следует обращаться если у Вас Токсоплазмоз:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Токсоплазмоза, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Токсоплазмоз
Токсоплазмоз – заболевание, которое в терминах паразитологии относится к группе протозойных паразитозов. Эта группа болезней характеризуется рядом специфических особенностей, поскольку весьма своеобразны их возбудители, составляющие подцарство простейших (protozoa). Более подробные сведения об этой группе патогенов представлены в статьях «Болезни, вызываемые простейшими» и «Простейшие. Амебиаз».
Возбудитель
Заболевание токсоплазмоз вызывается единственным (насколько сегодня известно) представителем рода токсоплазмы – простейшим Toxoplasma Gondii. Назван этот микроорганизм именем североафриканского горного грызуна гонди (другой вариант названия – гунди), у которого он был впервые обнаружен в 1908 году. Морфологически токсоплазма представляет собой округлую или, чаще, продолговатую клетку, формой напоминающую банан либо дольку апельсина. Это один из самых мелких представителей протозойного подцарства: длина составляет 8-10 мкм, поперечный габарит 2-4 мкм. Тем не менее, по всем признакам (см.выше) это именно простейшее, а не бактерия. Наряду с двумястами плазмодиями, из которых как минимум пять вызывают малярию, токсоплазма входит в класс споровиков (Sporozoa).
Токсоплазма является внутриклеточным паразитом и в качестве промежуточного хозяина может колонизировать около 300 видов теплокровных животных, включая человека, и не менее 60 видов птиц. Однако окончательным хозяином является семейство кошачьих, в том числе обычная домашняя кошка. Не будь этой особенности, – и едва ли стоило бы размещать данную статью на сайте Лахта Клиники. Дело в том, что организм «промежуточного хозяина» используется возбудителем для паразитирования в тканевых формах и размножения простым бесполым делением, тогда как «окончательный хозяин» означает организм, в котором токсоплазма размножается половым путем и образует т.н. ооцисты (яйцецисты) – ту самую форму, которая устойчива как ко внешним, так и к внутренним средам, и может годами пребывать в зрелом жизнестойком состоянии, чтобы однажды активизироваться в организме нового или «хронического» хозяина. В том числе и человека.
На сегодняшний день общая распространенность носительства токсоплазмы в мире оценивается в пределах 40-70%; иногда приводятся и более высокие проценты. Однако статистика обнаруживает выраженную региональную зависимость, что отчасти обусловлено неравномерностью распределения самой токсоплазмы в земной экосистеме (в Южной Корее, например, ее почти совсем нет, а в Южной Америке очень много – в некоторых областях заражено до 90% населения). Частота встречаемости в России оценивается на уровне 20%, то есть каждый пятый из нас является, как минимум, носителем.
В течение активного, острого периода течения токсоплазмоза (2-3 недели) больная кошка с фекалиями выделяет порядка двух миллиардов цист.
Жизнеспособность их сохраняется, в зависимости от условий, до двух и более лет.
Заражение
Присутствие токсоплазмы в организме домашней кошки можно считать доказанным, если в ее рационе хотя бы эпизодически случается сырое мясо, если она имеет возможность охотиться на мышей и если бывает на улице. Любая песочница, к которой имеют доступ коты, – инфицирована. Человек заражается через мясо, недостаточно обработанное термически; в некоторых странах (например, во Франции), где в блюдах национальной кухни присутствует «мясо с кровью», частота выявляемости антител к токсоплазме значительно выше. Возможно заражение через немытые овощи и фрукты, грязные руки, а также, в единичных случаях, через поврежденную кожу (раньше это представлялось сомнительным, в настоящее время сомнений не вызывает).
Кроме того, возможно внутриутробное трансплацентарное заражение от первично инфицированной матери. Обратим на это особое внимание.
Патогенез
Проникнув в кишечник промежуточного хозяина, – например, человека, – циста благодаря пищеварительным ферментам избавляется от защитной оболочки и высвобождает активную форму токсоплазмы, т.н. спорозоиты. В свою очередь, спорозоиты представлены двумя разными типами – тахизоитами и брадизоитами (напомним, «тахи-» и «бради-» переводится как «быстро» и «медленно», соотв.), которые гематогенным путем разносятся в различные участки организма, где стремятся внедриться в клетки хозяина. Во внутриклеточном пространстве брадизоиты, которые с трудом или вообще не идентифицируются иммунной системой, медленно размножаются, воспроизводя активные формы. Тахизоиты делятся гораздо быстрее (напомним, обе формы в промежуточном хозяине размножаются «бактериальным» агамогенезом и увеличивают свою популяцию стремительно – по тому же экспоненциальному закону, что и бактерии). Когда растущая плотная колония тахизоитов (псевдоциста) внутри клетки достигает критического объема, клетка погибает, тахизоиты оказываются в межклеточном пространстве (здесь их могут обнаружить и уничтожить иммунные факторы), и те из них, кто успел внедриться в следующую клетку, начинают цикл заново. Таким образом, в процессе постоянного самовоспроизведения внутриклеточно-паразитарные формы токсоплазмы, во-первых, быстро увеличивают свою численность, во-вторых, последовательно убивают колонизированные ими ткани. Кроме того, в организме могут оставаться целостные цисты, по какой-либо причине не активизировавшиеся в кишечнике, а также образовываться новые, – если паразитоз из-за слабости иммунной системы, неспособной к полной эрадикации, приобрел хронический характер и вошел в «бесконечный цикл» рецидивов и ремиссий.
Опасность для человека, симптоматика
Крайне важно отметить: доля инфицированных токсоплазмой людей, у которых развивается клинически значимый токсоплазмоз, очень мала – по разным оценкам, она варьирует от долей процента до нескольких процентов. Животные и птицы болеют токсоплазмозом гораздо чаще (см. ниже). Человек же практически всегда переносит токсоплазменную инвазию бессимптомно, поскольку иммунная система мгновенно распознает этот микроорганизм как враждебный – и реагирует настолько мощно, что инфицированный обычно даже не узнаёт о том, что был чем-то заражен. Кроме того, исключена опасность заразиться от инфицированного, даже если он переживает острый период токсоплазмоза (как правило, не подозревая об этом).
Таким образом, нет никаких оснований создавать лепрозории для носителей, повсеместно истреблять диких кошек и избавляться от кошек домашних, а ребенка выпускать на улицу лишь в скафандре высшей эпидемиологической защиты. Можно сказать, что мы, взрослые люди, если и были когда-то инфицированы, то эта проблема давным-давно решена, причем раз и навсегда: к токсоплазме вырабатывается устойчивый пожизненный иммунитет, и даже если человек попадает в незначительный процент переболевших в клинически значимой степени (лихорадка, легкое общее недомогание, мышечные боли, лимфаденопатия, спленогепатомегалия), то это уже не повторяется ни при каких обстоятельствах.
Иными словами, токсоплазма распространена широко, однако токсоплазмозом как болезнью почти никто из людей не болеет. И на этом, опять же, можно было бы поставить точку, если бы не слово «почти» и связанные с ним три «но».
Почти никто – это ведь не значит «абсолютно никто», особенно в пересчете на статистические масштабы. В какой-то, пусть даже малой, доле случаев острый период токсоплазмоза протекает отнюдь не бессимптомно и не в легкой гриппоподобной форме, а с весьма тяжелыми воспалительными осложнениями, такими как хориоретинит (поражаются сетчатка и сосуды глаз), пневмония (воспаление легких), энцефалит (воспаление головного мозга), эндокардит (воспаление внутрисердечной оболочки). Шансы вытянуть несчастливый билет в этой лотерее, повторим, статистически очень малы, но они не равны нулю, и в этом заключается первое «но».
Второе «но» состоит в том, что токсоплазма очень опасна для людей с выраженным иммунодефицитом. Ослабление иммунитета в силу «обычных» причин (переохлаждение, переутомление, стрессы, гиповитаминоз, перенесенная операция и мн.др.) является прямым фактором риска развития ОРВИ и многих других инфекций, но к токсоплазмозу это отношения не имеет. Речь идет именно о глубоком, выраженном иммунодефиците. В первую очередь это, конечно, ВИЧ/СПИД, но не только. Есть определенный процент лиц, вынужденных принимать онкологическую химиотерапию или иммуносупрессоры (напр., при аутоиммунных заболеваниях, после трансплантации органов и т.д.). Для всех этих категорий людей «почуявшая слабину» токсоплазма смертельно опасна: если при здоровом или даже ослабленном иммунитете ее быстро и безжалостно уничтожает наша природная защита, то в отсутствие или при глубокой недостаточности такой защиты токсоплазма столь же быстро и безжалостно пожирает мозговые, легочные, сердечные ткани, приводя к их массовому некрозу и, в итоге, к летальному исходу.
Наконец, третье «но», – главный мотив публикации данного материала: токсоплазмоз и беременность. Вопросы на эту тему сегодня звучат постоянно, и некоторым женщинам в период гестации действительно приходится сталкиваться с проблемой, которая, наверное, правильного решения не имеет вообще – ни рационального, ни эмоционального, ни интуитивного. Поэтому всё, что здесь можно сделать – это еще на этапе планирования беременности как можно лучше изучить вопрос и по возможности отчетливо представлять себе, в каком случае токсоплазма опасна, и насколько она опасна, и чем именно, и какие существуют способы предотвратить беду.
Как показано выше, токсоплазма способна проникать через плаценту в организм плода. Единственный вариант и единственное стечение обстоятельств, при которых это представляет реальную угрозу, – первичное инфицирование токсоплазмой в период беременности, т.е. первое в жизни заражение женщины, у которой ранее не было иммунитета к возбудителю. В этом случае действуют следующие статистические риски и клинические закономерности.
Чем больше срок беременности, тем выше проницаемость плаценты и вероятность инфицирования плода: в зависимости от триместра, этот риск оценивается как 15%, 25% и 70%.
Если внутриутробное заражение все же произошло, то тяжесть последствий для плода тем больше, чем меньше срок беременности. Вероятности того, что внутриутробный токсоплазмоз в дальнейшем ничем себя не проявит, – не существует. Надеяться на то, что произойдет уникальное чудо и последствий удастся избежать, к несчастью, не приходится даже в том случае, когда инвазия сразу же диагностирована и подвергнута интенсивному квалифицированному лечению. На практике внутриутробный токсоплазмоз означает смерть плода со спонтанным абортом, рождение с гидро- либо микроцефалией, или же развитие, в дальнейшем, тяжелейших поражений центральной нервной, зрительной и других систем организма. Интеллектуальная недостаточность характеризуется глубокой степенью выраженности.
В подобной ситуации, – когда происходит первичное заражение беременной женщины, – приходится ставить вопрос об искусственном прерывании беременности.
На последующие беременности вышеописанные риски не распространяется: речь, повторим, идет лишь о ситуациях, когда первичная инвазия токсоплазмы приходится на гестационный период.
Частота врожденного токсоплазмоза на сегодняшний день варьирует в пределах от 1:1000 до 1:10000 новорожденных.
Диагностика
Стандартом диагностики токсоплазмоза, в том числе на этапе внутриутробного развития, является серологическое исследование: реакция непрямой флюоресценции или ИФА (иммуноферментный анализ). Дополнительно назначают УЗИ и другие исследования по показаниям.
Лечение
Не лишне повторить снова и снова: абсолютное большинство случаев приобретенного (не внутриутробного) токсоплазмоза лечения не требует, поскольку иммунная система справляется с вторжением паразита и на будущее вырабатывает антитела к нему. Однако и на случай осложненного течения в арсенале современной паразитологии есть медикаментозные средства, эффективные в отношении токсоплазмы, напр., пириметамин, сульфадиазин, клиндамицин и т.д. При поражении сетчатки глаза и центральной нервной системы может быть целесообразным назначение глюкокортикоидных гормонов. Пациенты, инфицированные вирусом иммунодефицита, противорецидивную терапию получают пожизненно.
При врожденной инфекции, даже если в перинатальном периоде она протекает бессимптомно (что является, увы, лишь вопросом времени), назначают продолжительную терапию указанными выше средствами с добавлением фолиевой кислоты. Пытаются справиться и с внутриутробным заражением (например, применяют природный антибиотик спирамицин).
Разумеется, любое лечение токсоплазмоза должно назначаться исключительно врачом и осуществляться под его постоянным наблюдением и лабораторным контролем.
Терапия врожденного и хронического токсоплазмоза малоэффективна или не эффективна вообще.
Профилактика
Учитывая вышесказанное, женщине при планировании или наступлении беременности чрезвычайно важно пройти все назначенные обследования, ни в коем случае не игнорируя какие бы то ни было анализы и процедуры. Если обнаружено отсутствие иммунитета к токсоплазме, или же имеет место выраженный иммунодефицит, необходимо принимать все меры предосторожности, особенно при наличии в доме кошки: животное не должно гулять на улице и питаться сырым мясом. Санитарную обработку туалетного лотка следует производить регулярно, и лучше бы к нему не прикасаться человеку, для которого токсоплазма представляет опасность. Кошку желательно обследовать в ветеринарной клинике и, если выявлен паразитоз, качественно пролечить. Возможно, наилучшим решением является, – как бы тяжело это ни было для большинства семей, – расстаться с домашним питомцем, по крайней мере временно, на период вынашивания беременности.
Овощи и фрукты необходимо тщательно отмывать; любые мясные продукты должны проходить достаточную термическую обработку, а столы и доски, на которых разделывается мясо, – очищаться с применением моющих средств. Все гигиенические процедуры, особенно после любого контакта с землей, овощами, фруктами, ягодами и т.д., лица из группы риска должны выполнять сразу же, с мылом, самым тщательным образом.
В заключение отметим, что мир простейших микроорганизмов по-прежнему находится в фокусе напряженного внимания исследователей, – в том числе фармакологов, – однако многие вопросы остаются неясными. Это касается и токсоплазмы, которое свое название получила отнюдь не случайно: вырабатываемый ею токсин необычен и может оказаться гораздо опасней, чем принято считать в настоящее время. Известно и доказано, в частности, что это вещество каким-то образом искажает баланс нейромедиаторов и, если концентрация его в организме высока, влияет на поведение носителя (например, определенные виды птиц именно по этой причине, а не из-за токсоплазмоза как такового, поставлены под угрозу вымирания). Кроме того, изучается серьезно обоснованная гипотеза о том, что токсоплазма играет патогенетическую роль в возникновении и развитии душевных болезней человека, – прежде всего, исследуется возможная связь между токсоплазмой и шизофренией. Для психиатрии такие исследования чрезвычайно важны, поскольку шизофрения, – эта «жестокая королева» психических заболеваний, – как тяжелый хронический эндогенный процесс за последние сто лет досконально изучена в клинических проявлениях, однако до сих пор совершенно непонятна в триггерных и патогенетических механизмах, и ежегодно наносит колоссальный социальный, психологический и экономический ущерб в масштабах всей цивилизации.
Врожденный токсоплазмоз
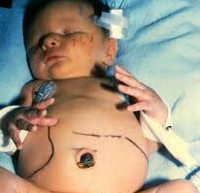
Врожденный токсоплазмоз – это паразитарная патология, которая возникает при трансплацентарном инфицировании ребенка Toxoplasma gondii. У большинства детей протекает бессимптомно. Возможные проявления заболевания: интоксикационный синдром, пятнисто-папулезная сыпь, лимфаденопатия, желтуха, гепатоспленомегалия, отеки нижних конечностей. Часто провоцирует развитие патологий органа зрения, слуха, ЦНС; реже – миокарда, легких и печени. Антенатальная диагностика базируется на проведении биопсии, постнатальная – на совокупности анамнестических и клинико-лабораторных данных (ИФА, ПЦР). Этиотропное лечение врожденного токсоплазмоза проводится при помощи схем на основе препаратов пириметамина и сульфадимезина или спирамицина.
МКБ-10
Общие сведения
Врожденный токсоплазмоз – заболевание в педиатрии и неонатологии, возникающее в результате трансплацентарного заражения плода на фоне острой формы токсоплазменной инфекции у матери. Впервые Toxoplasma gondii была описана французами К. Николь и Л. Монсо в 1908 году. В 1939 г. американцы Э. Вольф, Д. Кауэн и Б. Пэйдж подтвердили трансплацентарный механизм передачи возбудителя. Промежуточными хозяевами могут выступать более 400 видов животных. Согласно статистическим данным ВОЗ, число инфицированных токсоплазмой людей в мире составляет порядка 1,5 млрд. человек, в России – около 30% всего населения. Частота врожденной формы 1,5:1000 новорожденных. Даже на фоне лечения средний показатель смертности у детей до 5 лет составляет 12%, осложнения возникают почти у 90%.

Причины врожденного токсоплазмоза
Врожденный токсоплазмоз развивается только при инфицировании матери Toxoplasma gondii во время вынашивания ребенка. Механизм заражения беременной женщины – фекально-оральный. Наиболее распространенные причины: контакт с животными из семейства кошачьих и употребление термически необработанной пищи. Инвазивная форма возбудителя – ооциста – формируется в кишечнике животных и выделяется с калом, после чего может на протяжении 12 и больше месяцев сохранять контагиозность в условиях внешней среды. В крайне редких случаях этиологическим фактором может стать трансплантация контаминированных органов или переливание крови. Заражение плода T. gondii происходит трансплацентарным путем. После рождения ребенка развивается интенсивный гемолиз, возникают геморрагии на слизистых оболочках, расширение камер сердца, пневмония или интерстициальный отек легких, некроз печени и селезенки, увеличение лимфоузлов, воспаление и отек тканей головного мозга, некробиоз сетчатки. При гистологическом исследовании непосредственно пораженных тканей определяется некроз, гранулематозная или диффузная пролиферация ретикулоцитов, инфильтрация плазмоцитами и лимфоцитами, перифокально – множество токсоплазм. Впоследствии на месте некротизированных участков формируется фиброз, переходящий в кальциноз.
Классификация врожденного токсоплазмоза
В зависимости от периода инфицирования плода врожденный токсоплазмоз может протекать в трех формах:
- Хроническая форма. Заражение происходит в I-II триместрах беременности. Риск передачи возбудителя – 13-18%. При такой форме могут развиваться атрофия головного мозга, гидроцефалия, деформация желудочков мозга, анофтальмия, колобома, атрофия сетчатки, врожденные пороки сердца и других органов и систем.
- Подострая форма. Инфицирование – III триместр. Риск заражения ребенка – 75-85%. Проявления могут включать в себя энцефалит, менингоэнцефалит, очаговый некроз сетчатки, увеит.
- Острая форма. Токсоплазма попадает в организм ребенка непосредственно перед родами. Возможные симптомы: гипертермия, пятнисто-папулезная сыпь, интенсивная желтуха, гепатоспленомегалия, анемия, миокардит, пневмония.
Симптомы врожденного токсоплазмоза
Врожденный токсоплазмоз может проявляться в различные периоды жизни ребенка – от первых дней до нескольких месяцев. Специфических симптомов данное заболевание не имеет. Зачастую присутствующая клиника нечеткая и имитирует другие врожденные патологии. Наиболее вероятные проявления врожденного токсоплазмоза: ухудшение общего состояния, пятнисто-папулезная сыпь различной локализации, генерализованная лимфаденопатия, увеличение печени и селезенки, желтуха, отеки нижних конечностей, субфебрильное повышение температуры тела. Тяжесть симптомов зависит от степени инфицирования токсоплазмами, триместра беременности, в котором произошло инфицирование, и иммунных сил матери. Примерно 70-90% детей не имеют каких-либо проявлений в ранние периоды жизни, но почти у всех спустя некоторое время возникают осложнения. Классический врожденный токсоплазмоз проявляется триадой Сэбина – обструктивная гидроцефалия, хориоретинит и массивное внутричерепное обызвествление. Наблюдается данный комплекс не более чем у 3% детей. Помимо триады, часто возникают миокардит, миозит, гепатит и пневмония. Клинические проявления напрямую зависят от присутствующих патологических изменений. Вероятность развития поздних осложнений на фоне латентного врожденного токсоплазмоза составляет порядка 90%. Период возникновения может быть разным – от нескольких месяцев до нескольких лет. Наиболее часто наблюдается поражение глаз, органа слуха и ЦНС. Самое распространенное осложнение – ретинит (примерно 85% случаев). К другим последствиям перенесенного врожденного токсоплазмоза относят олигофрению, гидроцефалию, повышение внутричерепного давления, острый и хронический энцефалит, эпилепсию, полную глухоту и/или слепоту, микрофтальм, увеит, хроническую гипертермию, редко – шизофрению.
Диагностика врожденного токсоплазмоза
Диагностика врожденного токсоплазмоза может проводиться в антенатальном и постнатальном периоде. Антенатальное исследование подразумевает использование инвазивных методов с дальнейшими лабораторными анализами. Абсолютное показание к их проведению – острый токсоплазмоз матери в сумме с нарушениями развития плода по результатам акушерского УЗИ. Выбор методики исследования зависит от срока беременности. При гестации от 10 недель проводится биопсия хориона, от 16 недель – амниоцентез, от 18 – кордоцентез. Для верификации инфекции полученный материал исследуют при помощи ПЦР. Постнатальная диагностика включает в себя сбор анамнестических данных и проведение клинического и лабораторного исследования. Данная мера является обязательной для всех детей, входящих в группу риска внутриутробного инфицирования. Неспецифическая диагностика и ее результаты зависят от присутствующих симптомов и синдромов. Список исследований может включать в себя ОАК (анемия, тромбоцитопения, лейкоцитоз); рентгенографию ОГК (признаки инфильтрации легких); нейросонографию и КТ головного мозга; биохимическое исследование крови с измерением АЛТ и АСТ, определением СРБ, уровня билирубина и его фракций (все показатели выше нормы); офтальмоскопию (некроз сетчатки); спинномозговую пункцию (признаки воспаления). Специфические методы подразумевают серодиагностику биологических жидкостей методом ИФА, при котором наблюдается возрастание титра антител IgG в 4 и больше раз и высокий уровень IgM на протяжении 10-14 суток. При необходимости проводится ПЦР с целью идентификации ДНК токсоплазмы.
Лечение врожденного токсоплазмоза
Лечение новорожденного с выраженной клинической картиной врожденного токсоплазмоза проводится только в условиях стационара, в отделении патологии новорожденных. Соблюдение специфического режима и рациона не требуется, их коррекция проводится в соответствии с состоянием ребенка. При наличии отягощенного анамнеза матери этиотропную терапию начинают с момента постановки предварительного диагноза. В других случаях перед началом лечения требуется проведения лабораторных методов исследования. Используемые схемы: пириметамин и сульфадимезин на 1-1,5 месяца; спирамицин или другие макролиды на 4-6 недель. В некоторых случаях применяют системные глюкокортикостероиды – преднизолон. Симптоматическое лечение зависит от присутствующих симптомов и синдромов, выявленных педиатром или неонатологом. При стойком повышении внутричерепного давления или развитии гидроцефалии показано хирургическое лечение. При необходимости дальнейшее лечение может проводиться амбулаторно под контролем педиатра, инфекциониста и других специалистов. В таких же условиях проводится терапия субклинической и латентной формы врожденного токсоплазмоза. Решение об отказе от приема препаратов принимается на основе клинико-лабораторных показателей, находящихся в пределах возрастной нормы, и заключения всех лечащих врачей.
Прогноз и профилактика врожденного токсоплазмоза
Прогноз при врожденном токсоплазмозе зависит от триместра, в котором произошло инфицирование плода и тяжести клинических проявлений. При развитии патологии в I триместре может наблюдаться самопроизвольное прерывание беременности и выкидыш или дальнейшее развитие тяжелых форм заболевания, однако аномалии органов при этом не возникают. При адекватной и своевременной терапии прогноз для жизни благоприятный, для выздоровления – сомнительный. Неспецифическая профилактика врожденного токсоплазмоза включает в себя ограничение контакта домашних животных с беременной женщиной, соблюдение гигиенических норм, прием в пищу только термически обработанных продуктов, тщательное мытье овощей и фруктов. При наличии факторов, указывающих на возможное инфицирование матери, проводится специфическая диагностика, направленная на идентификацию T. gondii. При подтверждении диагноза показано немедленное проведение этиотропной терапии. Специфической профилактики врожденного токсоплазмоза не разработано.
Токсоплазмоз – симптомы и лечение
Что такое токсоплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Токсоплазмоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое простейшими внутриклеточными паразитами — токсоплазмами, которые попадая в организм человека могут при условиях иммунодефицита поражать нервную ткань, среды глаза, сердечно-сосудистую и ретикулоэндотелиальную системы, вызывая поражение организма той или иной степени тяжести. Болезнь относится к группе TORCH-комплекса, т. е. вызывает врождённую патологию.
Этиология
- 1908 год: французские учёные Ch. Nicolle и L. Manceaux выявили у грызунов микроорганизм, получивший родовое название Toxoplasma (в пер. с франц. taxon — дуга, plasmon — форма) и видовое — gondii (по названию грызунов).
- 1923 год: чешский офтальмолог I. Yanku установил роль токсоплазмы в патологии человека, описав симптомы врождённого токсоплазмоза у погибшего ребёнка и выделив паразита из сетчатки глаза.
- 1938-1939 год: американские исследователи доказали возможность передачи инфекции от матери к плоду через плаценту и прижизненно выделили паразитов от больного ребёнка.
Таксономия:
Вид — Toxoplasma gondii
Токсоплазмы обитают в мире в трёх формах:
- трофозоиты (тахизоиты);
- цисты (брадизоиты);
- ооцисты.
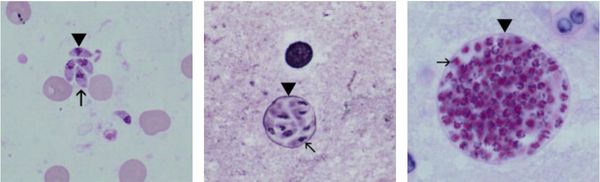
Трофозоиты достигают 4-7 мкм в длину и 2-4 мкм в ширину. Их тело по форме напоминает полумесяц с заострённым передним и закруглённым задним концами, состоит из пелликулы (покровной ткани) и различных органелл. Такие паразиты обитают во всех клетках млекопитающих кроме эритроцитов, размножаются путём деления. Могут создавать движение, активно проникая в клетки хозяина через клеточную мембрану или посредством фагоцитоза (захвата и переваривания клетки). Обнаруживаются в тканях в острой стадии инфекции. Их скопление внутри одной клетки называют псевдоцистой. Трофозоиты неустойчивы вне клетки и во внешней среде, быстро погибают при высушивании, прогревании и применении дезинфицирующих средств. Хорошо окрашиваются по Романовскому. Чувствительны к различным химиопрепаратам (сульфаниламидам, некоторым макролидам и другим).
Цисты размерами до 100 мкм отличаются плотной оболочкой, через которую не могут проникнуть антитела или лекарственные препараты. Внутри оболочки сосредоточено 3000-5000 паразитов, со временем они увеличиваются. Цисты формируются в организме хозяина (в основном в скелетных мышцах, миокарде и ЦНС) и живут там десятки лет. Чрезвычайно устойчивы к воздействиям внешних факторов. При адекватной иммунной системе могут пожизненно находиться в состоянии функционального покоя и не приносить никакого вреда организму человека.
Ооцисты играют основную роль в передаче инфекции. Они представляют собой овальные образования 10-12 мкм в диаметре. Их развитие и формирование длится 3-24 дня и проходит в слизистой оболочке тонкой кишки кошек. Затем в течение 7-20 дней паразиты выделяются с испражнениями, после этого срока новые фекалии кошки уже не заразны. За сутки с испражнениях животного выделяется до 10 миллионов ооцист. Спустя 2-3 дня при температуре 24 °C происходит споруляция ооцист — образование спор. При благоприятных условиях микроорганизмы сохраняются во внешней среде до года и дольше.
Существует множество штаммов токсоплазм, одни из которых отличаются высокой вирулентностью, а другие относительно маловирулентны. [1] [2] [7] [9]
Эпидемиология
Учитывая большое количество латентных форм, заболевание не поддаётся общему исчислению — им может быть заражено не менее 1,5 миллиардов человек. Только ежегодно регистрируется около 200 тысяч случаев внутриутробного инфицирования.
Распространение возбудителя повсеместное — токсоплазма обнаружена на всех материках. После заражения паразиты способны пожизненно сохранятся в организме большинства животных и птиц. Количество случаев приобретённого токсоплазмоза в разных странах колеблется: от 85 % во Франции и Мадагаскаре до 15 % в США и Англии.
- Фекально-оральный:
- водный и пищевой путь — при недостаточной термической обработке, чаще при употреблении сырого мяса и фарша;
- контактно-бытовой путь — при несоблюдении санитарных норм в повседневной жизни, например, при общении с кошками.
- Вертикальный путь (от матери к плоду) — преимущественно при первичном заражении матери во время беременности, часто у ВИЧ-инфицированных в стадии СПИДа.
- Артифициальный путь — при пересадке органов, в которых расположены цисты, пациенту с плохим иммунитету.
- Аэрогенный путь — при попадании инфицированной ооцистами пыли в рот человека.
- Контактный путь — при повреждении целостности кожных покровов. Встречается крайне редко, в основном у работников лабораторий и скотобоен, отмечен лишь в некоторых источниках, явного практического значения не имеет.
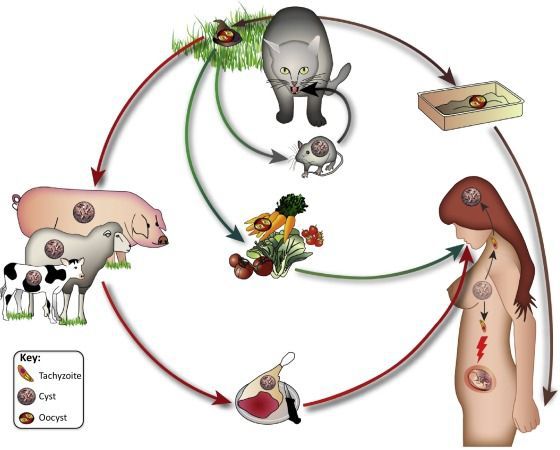
От человека к человеку заболевание не предаётся (кроме случаев каннибализма). Нельзя заразиться посредством укуса насекомых и при половом контакте.
Инфицирование токсоплазмой вызывает устойчивый пожизненный иммунитет к повторному заражению, однако известны случаи рецидива первичной инфекции при заражении другим высоковирулентным штаммом (у беременных, заразившихся при употреблении сырого мяса с другого континента). [1] [3] [5] [8] [9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы токсоплазмоза
Инкубационный период при манифестных формах (явных проявлениях болезни) длится от двух недель до двух месяцев.
Специфичных симптомов, характерных именно для токсоплазмоза, не существует.
В большинстве случаев приобретённого токсоплазмоза заболевание протекает бессимптомно или со стёртой клиникой, напоминающей нетяжёлое ОРЗ: кратковременная лихорадка, слабость, недомогание, повышение температуры до 38,0 °C, увеличение периферических лимфоузлов, небольшое увеличение печени и селезёнки.
Доказано, что токсоплазма может оказывать влияние на психику человека. Это выражается в учащении рискованных действий, снижении концентрации внимания, повышенной нервозности, у лиц с тяжёлым острым или длительным хроническим активным течением повышен риск развития шизофрении.
Иногда заболевание проявляется изолированной глазной формой — длительно текущие увеиты, иридоциклиты и хориоретиниты. Как правило, эти нарушения являются поздними проявлениями нераспознанного ранее врождённого процесса.
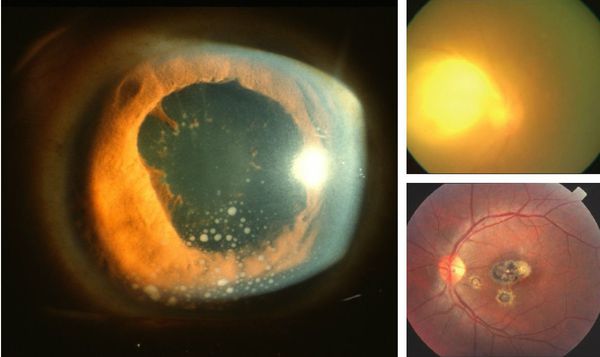
У людей с выраженным иммунодефицитом (ВИЧ, пересадка органов с последующей цитостатической терапией) возможно развитие генерализованного процесса с поражением нескольких органов (головного мозга, сердца, печени, почек, лёгких), нередко очень тяжёлого течения, проявляющегося в виде синдрома полиорганной недостаточности.
Токсоплазмоз у беременных может протекать в различных клинических вариантах и представляет опасность не столько для самой беременной (исключая тяжело протекающие патологии у беременных со СПИДом), сколько для плода.
При первичном заражении беременной токсоплазмозом имеет значение срок гестации:
- При инфицировании в первом триместре передача возбудителя плоду происходит лишь в 4 % случаев (к 13 неделе — в 6 %), но заканчивается, как правило, гибелью плода и выкидышем на ранних сроках. Если первичная инфекция у матери в первом триместре доказано, но выкидыш до 13 недели беременности не произошёл, то крайне высока вероятность, что внутриутробной передачи не было и ребёнок будет здоров.
- При инфицировании во втором триместре (особенно на 24-26 неделях) риск внутриутробной передачи резко возрастает и достигает 30-40 %, причём сопровождается развитием тяжёлых проявлений заболевания — одновременное увеличение селезёнки и печени, воспаление сосудистой оболочки и сетчатки глаза, поражения ЦНС в виде гидроцефалии, кальцификация, сыпь, миокардит, пневмония и другие.
- При заражении матери в третьем триместре передача инфекции ребёнку происходит с частотой до 90 %, однако проявления заболевания являются латентными или субклиническими и могут появиться спустя годы после рождения (отставание в развитии, нарушения зрения). [1][2][4][9]
Патогенез токсоплазмоза
Входные ворота токсоплазмоза — ротовая полость, оттуда ооцисты попадают в кишечник человека. Далее при развитии паразита (делении его клеток) образуются трофозоиты, которые мигрируют в различные органы и ткани (преимущественно в ЦНС и мышечную). В клетках они формируют псевдоцисты — большое количество размножающихся паразитов.
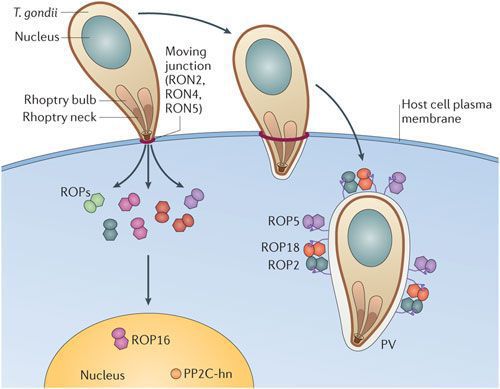
По мере развития и размножения токсоплазм поражённые клетки разрушаются, происходит заражение новых здоровых клеток, и при попадании возбудителя в кровоток паразиты разносятся по всему организму. Образуются некрозы с формированием фиброзной ткани и кальцификацией (отложение солей кальция в организме).
Под воздействием иммунитета безоболочечные трофозоиты превращаются в брадизоиты (оболочечные скопления токсоплазм), т.е. в тканевые цисты, которые сохраняются десятками лет в неактивном состоянии и при значительном снижении иммунитета способны к обратной трансформации с развитием обострения.
При первичной инфекции у беременных возбудитель проникает в ткани плода и вызывает воспалительный процесс, причём в разные периоды развития наблюдается различный характер воспаления: у эмбриона происходит лишь альтерация (дистрофия и некроз ткани без фиброза), в раннем фетальном периоде дополняется повышенным образованием соединительной ткани (фиброзом), а в позднем фетальном периоде присоединяется сосудистый компонент. Отсюда вытекают различные по характеру и тяжести поражения плода, которые зависят от сроков инфицирования матери. [1] [2]
Классификация и стадии развития токсоплазмоза
По течению процесса токсоплазмоз бывает:
- острым — до одного месяца;
- подострым – 1-3 месяц;
- хроническим — более трёх месяцев.
По клиническим признакам выделяют пять форм заболевания:
- Врождённый острый токсоплазмоз:
- манифестная форма (с указанием ведущих проявлений);
- субклиническая форма (с указанием способа верификации диагноза).
- Врождённый хронический токсоплазмоз:
- обострение / ремиссия;
- с резидуальными (остаточными) явлениями / без резидуальных явлений.
- Врождённый латентный токсоплазмоз.
- Приобретённый острый токсоплазмоз.
- Приобретённый хронический токсоплазмоз.
По степени тяжести заболевание бывает:
- лёгким;
- среднетяжёлым;
- тяжёлым (врождённая инфекция, токсоплазмоз при СПИДе).
По наличию осложнений выделяют:
- осложнённый токсоплазмоз;
- неосложнённый токсоплазмоз.
В Международной классификации болезней 10 пересмотра выделены шесть типов заболевания:
- B58.0 Токсоплазмозная окулопатия;
- B58.1 Токсоплазмозный гепатит (K77.0*);
- B58.2 Токсоплазмозный менингоэнцефалит (G05.2*);
- B58.3 Легочный токсоплазмоз (J17.3*);
- B58.8 Токсоплазмоз с поражением других органов;
- B58.9 Токсоплазмоз неуточнённый. [1][2][3]
Осложнения токсоплазмоза
При врождённой форме может возникнуть гидроцефалия, микроцефалия, задержка психомоторного развития и слепота. Эти осложнения сопровождаются увеличением или уменьшением размеров черепа, различными неврологическими расстройствами — косоглазием, судорогами, трудностью с сидением и держанием головы, рвотой и другими.
При глазной форме заболевания развивается слепота, снижение остроты зрения и воспалительные явления всех сред глаза. Причём возможно как рождение с грубыми дефектами зрения, так и появление воспалительных явлений и нарушения зрения спустя много лет после рождения.
Токсоплазмоз у иммунокомпрометированных людей осложняется шизофренией, токсоплазменный энцефалитом и полиорганной недостаточностью — тяжёлой патологией различных органов при выраженном иммунодефиците. При этом свойственна картина тяжёлого энцефалита. Прогноз, как правило, неблагоприятный. [1] [5] [8] [9]
Диагностика токсоплазмоза
Лабораторная диагностика:
- Клинический анализ крови: снижение уровня тромбоцитов, увеличение количества лимфоцитов и эозинофилов.
- Биохимический анализ крови: возможно повышение уровня трансаминаз и билирубина.
- Иммуноферментный анализ (ИФА):
- Выявление специфических антител класса M — острая инфекция или её реактивация. Имеет ряд недостатков — низкая специфичность, длительная циркуляция в организме, иногда до года после острого процесса. В сложных случаях уточнение следует производить при помощи метода “двойной сэндвич” или “иммунозахват” IgM ELISA.
- Выявление специфических антител класса G (клеток памяти) — носительство, инфицированность — появляются в среднем со второй недели заболевания и достигают пика на 1-2 месяце, сохраняются пожизненно, за исключением СПИД-ассоциированных заболеваний.
- Авидность IgG — уточнение давности заболевания. Недостатком является отсутствие стандартизации результатов, что зачастую приводит к различным ошибкам интерпретации. Наибольшее значение имеет высокая авидность, остальные результаты низкой и слабой авидности могут быть ошибочными и не должны трактоваться как недавно перенесённое заболевание при отсутствии других подтверждающих этот факт тестов.
- ПЦР-диагностика: выявление ДНК токсоплазмы в крови, других жидкостях и тканях человеческого организма. Особенно информативна в диагностике генерализованного, глазного и врождённого токсоплазмоза, в т. ч. в антенатальном периоде путём проведения амнио (не ранее 16 недель) и кордоцентеза (с 18 недели беременности).
- УЗИ-диагностика: внутриутробное выявление гидро- и микроцефалии, кальцификатов, гепатоспленомегалии и выраженной задержки развития. [1][2][4][5][6]
Дифференциальная диагностика
Токсоплазмоз — это инфекция с необычайно разнообразными проявлениями, поэтому ввиду неспецифичности проявлений основное место в дифференциальной диагностике отводиться лабораторному обследованию, а именно специфическим серологическим тестам.
Необходимо исключить следующие заболевания:
-
(ВЭБ-инфекцию) — боли в горле, преимущественное увеличение затылочных и заднешейных лимфоузлов, характерные изменения гемограммы (появление большого количества атипичных мононуклеаров и отсутствие столь выраженных изменений при врождённом течении), положительные IgM и ПЦР крови; — лимфоцитарный характер гемограммы, частое поражение слюнных желёз, положительные IgM, ПЦР крови;
- туберкулёз — длительное постепенное начало, лёгкий субфебрилитет (до 38,0 °C), ночная потливость, нездоровый румянец на щеках, кашель, специфические изменения в лёгких, положительные пробы на туберкулёз, выявление бациллы Коха в мокроте;
- лимфопролиферативные заболевания (лимфома Ходжкина, неходжкинские лимфомы) — специфические изменения при биопсии поражённой ткани (лимфоузлов);
- ВИЧ-инфекция — наличие факта возможного заражения, увеличение всех групп лимфоузлов, положительная серология;
- саркоидоз — специфические изменения в лёгких, положительные результаты гистологического исследования. [1][2][5]
Лечение токсоплазмоза
Большинство случаев приобретённого токсоплазмоза протекают в лёгкой или бессимптомной форме, они не регистрируются и, по-видимому, не нуждаются в каком-либо лечении.
Необходимость проведения специфической этиотропной терапии возникает лишь у некоторых групп пациентов:
- беременные с доказанным первичным инфицированием (в ряде случаев при реактивации хронической инфекции);
- дети с врождённой формой токсоплазмоза (при наличии явных клинических и лабораторных проявлений заболевания, субклинических и инаппарантных формах) — сроки и объём терапии зависят от конкретных данных;
- иммунокомпрометированные люди, у которых токсоплазмоз (острый или в фазе реактивации хронического процесса) протекает с выраженными клинико-лабораторными проявлениями. Основное направление воздействия в этом случае должно быть на устранение причины иммунодефицита, повышение уровня СД4 клеток.
Проведение лечения может осуществляться как в стационаре, так и амбулаторно в зависимости от выраженности процесса, реакции пациента на вводимые препараты, необходимости тех или иных вариантов патогенетического и симптоматического обеспечения. [1] [4] [7]
Прогноз. Профилактика
При приобретённом токсоплазмозе у иммунокомпетентных лиц прогноз благоприятный, у иммунокомпрометированных лиц (СПИД) прогноз серьёзен, нередки летальные исходы.
При врождённом токсоплазмозе исход заболевания зависит от сроков инфицирования плода:
- при инфицировании в первом триместре, как правило, происходит выкидыш;
- в более поздние сроки последствия варьируются от тяжёлых до резидуальных форм.
Основным методом профилактики приобретённого и врождённого токсоплазмоза является соблюдение санитарно-гигиенических правил, особенно беременными, не имеющими антител класса G к токсоплазмам:
- ограничение контакта с кошками;
- запрет на употребление сырого мяса, фарша и морепродуктов;
- тщательная промывка зелени, фруктов и овощей;
- мытьё рук перед едой;
- работа на приусадебном участке только в перчатках.
Для беременных особенно важен скрининг антител к токсоплазме, позволяющий выявить активно протекающее заболевание или риск его возникновения, а также вовремя провести медикаментозную профилактику острого токсоплазмоза беременной и снизить риск врождённой инфекции на 60 %. При отсутствии антител класса G в первом триместре необходимо отслеживать антитела IgM и IgG не только в тертьем, но и во втором триместре беременности.
В очаге токсоплазмоза противоэпидемические мероприятия не проводятся, вакцина на разработана. [2] [3]
Токсоплазмоз
Токсоплазмоз — это заболевание человека, вызванное микроскопическим одноклеточным паразитом Toxoplasma gondii. Отличается большим разнообразием клинических проявлений, в основном поражает:
- Нервную систему.
- Глаза.
- Скелетные и сердечную мышцы.
- Лимфатическую систему.
Возбудитель очень распространен в природе, его переносят несколько сотен видов животных и птиц, в том числе – домашних. Паразит легко проникает в организм, но часто не приводит к развитию острой инфекции. Заболевание обычно развивается у людей со сниженной иммунной реакцией – больных СПИДом и другими иммунодефицитными состояниями, при приеме иммуносупрессоров.
Возбудители заболевания, его источники
Наиболее опасным является внутриутробное инфицирование, которое нередко заканчивается выкидышем либо тяжелыми врожденными патологиями. По этой причине анализ на токсоплазмоз должен обязательно проводится при подготовке к беременности и вынашиванию ребенка.
По статистическим данным токсоплазма обнаруживается у 25-80% населения планеты. В отдельных регионах степень заражения достигает 95%.

Токсоплазма – внутриклеточный паразитический организм, который способен существовать в трех формах:
- Тахиозоиты. Имеют форму полумесяца и размер 2-4 мкм. Характерная особенность – при специальной окраске (по Романовскому-Гимзе) ядро приобретает красный цвет, а цитоплазма становится серо-голубой. В этой форме паразит проникает в клетки иммунной системы (макрофаги, фагоциты), в которых быстро размножается. После гибели клетки тахиозоиты высвобождаются и заражают здоровых макрофагов.
- Брадиозоиты (псевдоцисты). Это защитная форма токсоплазмы, в которой происходит большая часть жизнедеятельности возбудителя при нормальной иммунной реакции со стороны зараженного организма. Форма клетки брадиозоитов удлиненная, ядро смещено к одному из окончаний. Токсоплазмы в этой форме часто формируют тканевые псевдоцисты состоящие из множества клеток паразиты покрытых общей защитной оболочкой.
- Ооцисты. Эта форма токсоплазмы встречается только в эпителиальных клетках кишечника домашней кошки и ее диких родственников. Образуется в результате полового размножения паразита внутри клеток животного. Затем незрелые ооцисты выделяются в окружающую среду вместе с фекалиями. При достаточной температуре и притоке свежего кислорода ооцисты созревают в течение 2-7 дней. После завершения созревания ооцисты становятся способны заражать промежуточных хозяев токсоплазмы, в том числе – людей.
Основным источником заражения являются представители семейства кошачьих, в подавляющем большинстве – домашняя кошка. Механизм передачи паразита – фекально-оральный. Реализуется за счет:
- Употребления недостаточно термически обработанных мясных продуктов (особенно свинины и баранины).
- Через плохо вымытые овощи, зелень, фрукты.
- Несоблюдение правил личной гигиены (немытые руки).
Изредка возможно прямое заражение токсоплазмой через микроповреждения кожных покровов. От матери к ребенку паразит передается редко. В среднем одно заражение на 2-3,5 тыс. беременных. Наиболее вероятно инфицирование плода токсоплазмой если в процессе вынашивания организм беременной впервые столкнулся с паразитом.
Восприимчивость к токсоплазме крайне высока, для заражения достаточно единичных ооцист. Наиболее восприимчивы молодые люди, у пожилых (после 60 лет) паразит выявляется значительно реже.

Приобретенный токсоплазмоз, симптомы

Явные клинические симптомы у большей части заразившихся отсутствуют, болезнь сразу переходит в латентную фазу носительства. Инкубационный период составляет от 1 до 3 недель.
При проявлении выраженной клинической картины симптоматика нарастает медленно. Обычно болезнь начинается бессимптомно с увеличения региональных лимфатических узлов (паховых, подмышечных, шейных). Лимфоузлы эластичны, безболезненны, больные в этот период не предъявляют никаких жалоб.
Затем температура тела поднимается до 38-39 градусов, появляется головные боли, развиваются симптомы острого гастроэнтерита. В особо тяжелых случаях токсоплазмоза лихорадка начинается внезапно, температура тела может повышаться до 40 и более градусов. Наблюдается интенсивное потоотделение, выраженная интоксикация, боли в животе и макулезная сыпь.
После первой недели развития инфекционного процесса происходит увеличение селезенки и печени. Могут возникать ноющие боли в крупных мышечных группах нижних и верхних конечностей. У каждого пятого в этот период развивается хориоретинит проявляющийся в выпадении участков поля зрения.
Начиная со второй недели симптоматика поражения ЖКТ начинает затухать. Уменьшаются и быстро исчезают симптомы энтерита, снижается общая интоксикация организма. Одновременно развивается поражение:
- Опорно-двигательной системы. Усиливается болевой синдром в конечностях, суставах, возможно нарушение подвижности и мелкой моторики.
- Ретикулоэндотелиальной. Проявляется гепатолиенальным синдромом, мезаденитом.
- Сердечно-сосудистой. Нередко развиваются нарушения ритма сердечных сокращений, симптомы миокардита либо перикардита.
На 3-4 неделе заболевание завершается затуханием всех проявлений и переходом токсоплазмоза в бессимптомное носительство. При воздействии негативных факторов, ослабляющих иммунитет возможна манифестация заболевания с развитием вышеописанной клинической картины, которая снова переходит в латентную фазу.
Частые рецидивы острой формы токсоплазмоза, особенно на фоне иммуноподавляющих факторов, могут приводить к серьезным осложнениям. Чаще встречаются:
- Миокардиодистрофия.
- Психоневрологические патологии.
- Снижение интеллекта.
- Атрофия зрительного нерва вплоть до полной слепоты.
- Синдром хронической усталости.
Острый токсоплазмоз у женщин может приводит к нарушению менструального цикла, выкидышам и другим патологиям со стороны половой системы.
Хронический приобретенный токсоплазмоз – достаточно редкое явление, считается СПИД-ассоциированной формой заболевания. Протекает с периодическими обострениями, часто развиваются осложнения со стороны ЦНС в виде энцефалитов и поражения органов зрения.
Наиболее тяжелое следствие хронического токсоплазмоза – генерализованная инфекция в ходе которой быстро развивается полиорганная недостаточность, иногда данное осложнение завершается смертью больного.
Врожденный токсоплазмоз, возникающий при беременности

Возникает при проникновении паразита через плацентарный барьер и заражении плода. В большинстве случаев происходит при первичном заражении во время беременности, реже – при рецидиве токсоплазмоза связанном со снижением иммунитета. Основная группа риска – женщины, которые не были заражены токсоплазмой до наступления беременности. Если в результате контакта с возбудителем произойдет манифестация заболевания в процессе вынашивания плода – достаточно высока вероятность развития врожденного токсоплазмоза.
Процент выживаемости детей при внутриутробном инфицировании зависит от срока, на котором оно произошло:
- При инфицировании на первом триместре шанс на выживание плода – 15%
- На втором – 30%.
- На третьем – 60%
Даже если беременность успешно завершается, сохраняется крайне высокая степень развития врожденных патологий и врожденного токсоплазмоза. Болезнь протекает тяжело, особенно если инфицирование произошло на ранних сроках. Развивается характерная тетрада патологигй:
- Гидроцефалия.
- Двусторонний ретинохороидит.
- Задержка психофизического развития.
- Церебральные кальцификаты.
Прогноз в случае врожденного токсоплазмоза неблагоприятный, в большинстве случаев болезнь завершается смертью новорожденного либо тяжелой инвалидизацией. Даже если после внутриутробного заражения острая клиническая картина не возникла такие дети находятся в группе риска развития:
- Умственной недостаточности.
- Эпилепсии.
Возможно развития многих других патологий, которые проявляются спустя месяцы и годы после рождения. По этой причине острая форма токсоплазмоза, возникшая во время беременности – показание к проведению аборта даже на поздних сроках. При беременности необходимо сдавать массу анализов, которые помогают выявить наличие не только токсоплазмоза, но и ЦМВ-инфекции.
Показания к обследованию
Анализ чаще всего назначают в двух случаях:
- При планировании беременности в составе стандартного пакета лабораторной диагностики TORCH-инфекции.
- При подозрении на токсоплазмоз и определенных симптомах.
Также лабораторная диагностика используется при выявлении симптомов острого токсоплазмоза у взрослых либо детей.
В общей врачебной практике данный анализ назначают в случае проявления у пациентов специфических симптомов (нарушение зрения, судороги) а также ВИЧ-инфицированным.
Дифференциальная диагностика
Проводится с болезнями, симптомы которых схожи с острой и хронической формой токсоплазменной инфекции. В их число входят:
- Инфекционный мононуклеаз.
- Микоплазмоз.
- Хламидиоз.
- Цитомегалия.
- Туберкулез.
Также необходимо исключить онкологические патологии и системные заболевания (ревматизм, лимфогранулематоз). Окончательный диагноз устанавливается после получения результатов специфичных серологических исследований и ПЦР. Существует достаточно много лабораторных методик обнаружения специфических антител к токсоплазме. В их число входят:
- ИФА. Иммуноферментный анализ.
- РНИФ. Реакция непрямой иммунофлюоресценции. Становится позитивной с первой недели заболевания. Высокий титр антител может сохранятся до 15 лет.
- РСК. Реакция связывания комплемента. Становится положительной с 10-14 дня развития болезни, сохраняется на протяжении 2-3 лет.
Материал для исследования

Для обнаружения специфических антител к токсоплазме производится забор крови из вены, особой подготовки процедура не требует. Для проведения ПЦР-реакции подходит любой биологический материал – кровь, слюна, образцы тканей, другие биологические жидкости (ликвор, моча).
Если возникает потребность в диагностике токсоплазмоза у плода возможен забор крови из пупочного канатика. Процедура назначается редко потому что связана с высоким риском осложнений и преждевременного прерывания беременности. Более щадящая методика – взятие на анализ околоплодной жидкости путем пункции. Эти методики применяют в случае, когда результаты специфических анализов беременной с подозрением на токсоплазмоз не дают достаточной ясности диагноза.
Показания к применению различных лабораторных исследований и особенности интерпретации результатов у разных категорий обследуемых
В зависимости от категории пациента (возрастной группы, группы риска) показано применения различных наборов методик диагностики. Особенно важен правильный выбор диагностических методов в случае подозрений на токсоплазмоз у беременных женщин.
Обследование на токсоплазмоз при беременности
Если в процессе беременности у беременной выявлены симптомы которые могут свидетельствовать о развитии острого токсоплазмоза необходимо при помощи серологических методов установить уровень специфических иммуноглобулинов.
Для выявления острой стадии заболевания лучше всего подходит иммуноферментный метод (ИФА). Он наиболее точно показывает концентрацию IgM, повышение уровня которого свидетельствует о протекающем, либо недавно присутствовавшем остром токсоплазмозе.
Определение уровней IgG менее информативно так как эти антитела сохраняются долгое время после перенесенной инфекции и свидетельствуют скорее о носительстве, чем о недавнем заражении либо обострении. Женщины, перенесшие инфицирование токсоплазмой до беременности застрахованы от заражения плода и не входят в группу риска.
Также важно получение иммунологической картины в динамике, для чего специфические тесты проводятся не реже 1 раза в 2 недели. Изучение динамики изменений титров антител позволяют с большей точностью установить диагноз.
Нужно учитывать, что серологическая картина, свидетельствующая об инфицировании токсоплазмой не является 100% показанием для прерывания беременности. В этом случае потребуется проведение дополнительных анализов путем взятия крови плода из пупочного канатика и образцов амниотической жидкости пункционным методом.
Обследование новорожденных детей и детей раннего возраста
Направлено на раннее обнаружение возбудителя, до начала острой фазы врожденного токсоплазмоза и развития тяжелых осложнений. Назначается, когда есть подозрение на инфицирование токсоплазмой, включает в себя следующие тесты:
- Выделение паразита путем внесения материала из плаценты и пупочного канатика в живых мышей.
- Проведение ПЦР-анализа амниотической и люмбальной жидкостей.
- Компьютерная томография либо МРТ головы. Позволяет выявить на ранних стадиях специфические изменения в головном мозге, например, гидроцефалию.
Серологические методики также применяются, но они дают только дополнительную информацию. Иммунная система новорожденного недостаточно активна, часто неспособна выработать достаточно высокий титр специфических антител.
Обследование больных ВИЧ-инфекцией
Диагностика заключается в регулярном отслеживании титров иммуноглобулинов G серологическими методами. Титрование иммуноглобулинов M неинформативно так как у большинства ВИЧ-позитивных уровень антител этой группы крайне вариабелен.
В прямом выявлении возбудителя путем микроскопии образцов ткани либо заражения лабораторных животных как правило необходимости нет. Диагноз достаточно точно можно установить за счет серологической диагностики и наличия специфической клиники токсоплазмоза. У ВИЧ-позитивных больных она более выражена, что значительно упрощает постановку диагноза.
Обследование в Медарт

На базе медицинского центра Медарт выполняется полный комплекс серологических анализов для выявления токсоплазмы в организме пациента. Иммунологическое исследование с целью выявления специфических иммуноглобулинов входит в состав комплексных тестов ЗППП, предназначенных для пар, планирующих рождение ребенка. Возможно выполнения забора крови и других биологических жидкостей для установления наличия токсоплазмы и уточнения клинической картины протекания заболевания.
Высокоточное современное оборудование позволяет в кратчайшие сроки получить точные результаты исследований.
Преимущества медицинского центра Медарт:
- Квалифицированные специалисты.
- Возможность быстро получить точный результат исследования.
- Доступная стоимость.
На базе медцентра предоставляется полный комплекс услуг, от предварительного приема и консультаций до постановки и уточнения диагноза и назначения эффективных схем лечения и профилактики токсоплазмоза и других заболеваний.
X Международная студенческая научная конференция Студенческий научный форум – 2018

ТОКСОПЛАЗМОЗ. ПРИЧИНЫ, СИМПТОМЫ, ДИАГНОСТИКА И ЛЕЧЕНИЕ
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке “Файлы работы” в формате PDF
Введение. Токсоплазмоз – врожденное или приобретенное паразитарное заболевание с длительным, нередко хроническим течением, характеризующееся весьма частым поражением ЦНС, глаз, печени, селезенки и других органов и систем. Заболевание широко распространено как среди людей, так и среди теплокровных животных, включая птиц. На территории нашей страны, по неполным данным, инфицировано около 30% населения. Однако среди инфицированных манифестные формы болезни встречаются редко – не более 1% всего населения. Большинство случаев первичного поражения токсоплазмозом приходится на детский возраст.
Заболевание, вызываемое облигатным внутриклеточным паразитом Toxoplasma gondii, характеризующееся преимущественно латентным течением. При наличии иммунного дисбаланса (иммунодефицита) может протекать с поражениями ЦНС, органов ретикулоэндотелиальной системы, поперечно-полосатой мускулатуры различной степени выраженности, вплоть до летальных исходов.
Биология и жизненный цикл. Токсоплазма относится к классу споровиков (на переднем конце таких паразитов расположен комплекс, обеспечивающий их проникновение внутрь клеток хозяина).
Имеют очень сложный жизненный цикл, в нем выделяется половой и бесполый процессы (с формированием и слиянием половых клеток – гамет), в организме окончательного хозяина из семейства кошачьих (домашние и дикие кошачьи).
Токсоплазма существует в виде 3 форм: тахизоит – быстро размножающая внутриклеточная форма, брадизоит – медленно размножающаяся внутриклеточная форма и ооциста. В результате полового размножения формируется спора – ооциста. В ооцисте путем деления формируется несколько спорозоитов, служащих для заражения других хозяев.
Человек заражается 3 путями:
при попадании в организм ооцист, с пищей или водой;
трансплацентарно происходит заражение плода, если мать заражается токсоплазмозом во время беременности;
при употреблении недостаточно термически обработанного или сырого мяса животных или птиц, зараженных токсоплазмозом и содержащих брадизоиды.
Способы инфицирования токсоплазмой. Алиментарный путь. Заражение наступает при употреблении в пищу инфицированных продуктов животного происхождения (например, мясо, молоко, яйца), не прошедших должным образом термическую обработку. Согласно результатам проведенных исследований, особенно много токсоплазм может находиться в мясе свиньи и барана. Вертикальный путь. Данный путь передачи еще называют трансплацентарным, так как передача токсоплазм происходит через плаценту от матери к плоду. Трансплацентарный путь передачи токсоплазмоза является наиболее опасным, так как во время беременности внедрение инфекции может спровоцировать у будущего ребенка серьезные патологические изменения (например, умственная отсталость, эпилепсия, внутричерепное давление, слепота). Инфицирование ребенка на ранней стадии беременности (первый триместр) нередко приводит к гибели плода. Фекально-оральный путь. Результаты проведенных исследований доказали, что инфицированные токсоплазмами кошки за две недели способны выделять в окружающую среду порядка двух миллиардов ооцист, которые считаются заразными в течение двух лет. Передача токсоплазм осуществляется при заглатывании пыли вместе с паразитами в тех местах, где испражнялась инфицированная кошка (например, песочница, огород, сад). Также инфекцию можно занести через рот с помощью загрязненных рук после контакта с больной кошкой, на шерсти которой обычно сохраняются частички ее испражнений.
Симптомы. Различают врождённый и приобретённый токсоплазмоз.
Врожденный токсоплазмоз. Особую опасность представляет вероятность внутриутробного заражения плода. Токсоплазма способна проникать через плаценту и вызывать болезнь у еще не родившегося ребенка. Но это возможно только в том случае, когда мать заражается токсоплазмозом во время беременности. В случае если она заразилась еще до беременности, будущему ребенку ничего не угрожает.
При врожденном токсоплазмозе поражение органов очень значительно. Так, возможны врожденные уродства глазного яблока, вплоть до развития слепоты, недоразвитие головного и спинного мозга. Тяжесть поражения плода тесно связана со сроками беременности – чем моложе плод, тем тяжелее болезнь.
В результате врождённого токсоплазмоза плод либо погибает в результате возникновения уродств, несовместимых с жизнью, либо рождается с симптомами острого врождённого токсоплазмоза – интоксикацией, лихорадкой, желтушностью, поражениями печени, селезёнки, лимфатических узлов и центральной нервной системы (энцефаломиелит).
Но токсоплазмоз может поражать плод только один раз, все последующие беременности будут надежно защищены образовавшимися у матери антителами.
Приобретённый токсоплазмоз нередко протекает в латентной (скрытой) форме; острая форма может напоминать тиф или энцефалит, нередки поражения глаз. Длится острая стадия примерно 7 дней. Острый токсоплазмоз начинается с высокой температуры, головной боли, судорог, рвоты. Увеличивается печень и селезенка, могут присоединиться воспаление легких и параличи.
Наиболее частой является хроническая форма заболевания, с длительным повышением температуры до 37,2-37,8 градусов, головными болями, увеличением печени, селезёнки, лимфатических узлов; мышечными и суставными болями. Возможно и носительство инфекции.
Хроническая форма и носительство нередко переходят в острую форму на фоне стресса, беременности, снижения иммунитета различной природы. На выраженность проявлений токсоплазмоза существенно влияет общее состояние здоровья, иммунный статус. У лиц с иммунодефицитом (включая СПИД) заболевание протекает крайне тяжело, часто со смертельным исходом.
Диагностика. Дифференциальная диагностика. Токсоплазмоз следует дифференцировать с инфекционным мононуклеозом, доброкачественным лимфоретикулезом, туберкулезом, бруцеллезом, листериозом, микоплазмозом, хламидиозом, цитомегалией, герпесом и рядом других бактериальных, вирусных и паразитарных инфекций. Следует исключить онкологические и системные заболевания (например: лимфогранулематоз, ревматизм и т.д.).
Лабораторная диагностика. Для лабораторной диагностики токсоплазмоза чаще всего применяют серологические методы: реакцию связывания комплемента (РСК), реакцию непрямой иммунофлюоресценции (РНИФ), иммуноферментный анализ (ИФА). Диагноз подтверждается достоверно нарастающей динамикой показателей этих тестов, их высоким уровнем либо наличием антител класса IgM.
Формирование диагноза. При формировании развернутого диагноза токсоплазмоза следует указывать:
форму токсоплазмоза (приобретенный, врожденный);
характер течения процесса (острый, подострый, хронический, инаппарантный);
органную или системную патологию;
Лечение. Выбор тактики лечения зависит от формы и характера течения заболевания, выраженности клинической симптоматики, тяжести течения, наличия осложнений и преобладающих органно-системных поражений.
Абсолютными показаниями к назначению лечения являются острый и подострый токсоплазмоз. Лечение хронического токсоплазмоза проводится в зависимости от выраженности клинической симптоматики, характера преобладающих поражений. Требует лечения и инаппарантный токсоплазмоз, выявленный у беременных женщин.
Назначаются препараты «Фансидар», «Ровамицин» и «Бисептол». Фансидар содержит сульфадоксин 500 мг и пириметамин 25 мг. Этиотропная терапия состоит из 2–3 циклов. Назначается 1 таблетка 1 раз в 3 дня (№ 8 таблеток). Между циклами назначается фолиевая кислота. При непереносимости препаратов группы пириметаминов назначают Ровамицин, 1 таблетка которого содержит спиромицина 3 млн МЕ. Назначают по 3 млн МЕ 3 раза в день с семидневным перерывом. Хорошая переносимость Ровамицина больными, отсутствие лекарственного взаимодействия, высокая эффективность позволяют назначать его для лечения токсоплазмоза во всех возрастных группах.
Возможно применение комбинированных препаратов; Потесептила (триметоприм + сульфадимезин), Бисептола (триметоприм + сульфаметоксазол), которые назначаются по 1 таблетке 2 раза в день в течение 10 дней (цикл), в количестве 2–3 циклов (курс). При непереносимости указанных препаратов при пероральном приеме возможно назначение внутривенно или капельно Бисептола: по 10 мл в день, в течение 5 дней (курс). В перерывах между циклами (курсами) этиотропной терапии назначается фолиевая кислота, в среднем до 0,01 г в сутки.
В случае выявления иммунодефицитного состояния совместно с этиотропной терапией назначаются иммунотропные средства: Ликопид, Циклоферон, Витамедин-М, а также натуральные гормоны тимуса телят и их синтетические аналоги: Тактивин, Тимамин, Тимоген, Декарис.
В комплексной терапии используют и препараты системной энзимотерапии (СЭТ), в частности Вобэнзим и Флогэнзим. Для сохранения микробиоценоза кишечника рекомендовано назначение про- и пребиотиков.
Лечение и дальнейшее диспансерное наблюдение за больными должно проводиться у специалистов в зависимости от характера преобладающей патологии— врачей-инфекционистов, врачей-невропатологов, врачей-окулистов, акушеров-гинекологов и др. Госпитализация осуществляется в стационар соответствующего профиля (инфекционный, неврологический, офтальмологический, акушерско-гинекологический, детский и т.д.). Это обусловлено особенностями органной патологии, спецификой обследования и назначением дополнительных средств лечения.
Профилактика. Профилактика токсоплазмоза включает: употребление в пищу только хорошо термически обработанных мясных продуктов; исключение привычки дегустации сырого мясного фарша или сырого мяса; употребление в пищу чисто вымытых овощей, зелени и фруктов (с земли); тщательное мытье рук после обработки сырого мяса, сырых мясных продуктов, после работы в саду, огороде, у детей – после игры на детской площадке, особенно в песочнице; борьбу с беспризорными кошками; лечение больных токсоплазмозом домашних кошек, предупреждение заражения последних. Специфическая профилактика токсоплазмоза не разработана.
Заключение: На сегодняшний день это заболевание не достаточно изучено, и требует большого внимания. Практически в каждом доме имеются кошки и собаки, первые же в свою очередь являются абсолютным источником заражения.
Источники:
Засухин Д.Н, Калякин В.Е, Акиншина Г.Т. Современные представления о цикле развития токсоплазм. Паразитология , 1971, №4, 5, с. 302 – 309; в кн.: Токсоплазмоз животных под ред. И.Г. Галузо. Алма-Ата, 1965 – C. 25- 30
Андреева Е.A. Врожденный токсоплазмоз / Е.А. Андреева // Эпидемиология и инфекционные болезни. – 2006. – № 1. – С. 49-52.
А. П. Казанцев /. Токсоплазмоз – Ленинград: Медицина: Ленингр. отд-ние, 1985. – 168 с.
Агринский Н.И. и А.Ф. Кухто. Токсоплазмоз – В кн.: Малоизученные заразные болезни животных. (Под. ред. Ф. М. Орлова. М, 1959.
Токсоплазмоз , как причина психических расстройств

Toxoplasma gondii – возбудитель токсоплазмоза – это облигатный внутриклеточный апикомплексный паразит с широким географическим распространением и способностью инфицировать практически любой тип клеток в широком диапазоне хозяев, включая людей, домашних животных, домашний скот и диких животных
Паразитическое простейшее Toxoplasma gondii поражает около трети населения развитых стран. Однако, современный человек не является естественным хозяином токсоплазмы. Постоянное присутствие этого паразита в состоянии покоя в головном мозге и мышечных тканях инфицированного человека обычно считается бессимптомным с клинической точки зрения. Скрытый токсоплазмоз, то есть пожизненное наличие кист в головном мозге и мышечных тканях, явно себя не проявляет , но влияет на здоровье человека.Так , например , инфицированные субъекты получают худшие результаты в тестах на психомоторную работоспособность и имеют другие личностные профили, чем субъекты с отрицательным токсоплазмозом.
За последние 20 лет исследования, проведенные в основном на военнослужащих, студентах университетов, беременных женщинах и донорах крови, показали, что это «бессимптомное» заболевание оказывает большое влияние на различные аспекты жизни человека.. Исследователи предположили, что изменение черт личности вызвано манипуляционной активностью паразита, направленной на увеличение вероятности передачи паразита от промежуточного хозяина ( кошка) к окончательному хозяину.
Пути заражения паразитом
Люди обычно заражаются либо случайно проглатывая инфекционные ооцисты, либо употребляя недоваренное мясо, содержащее тканевые цисты (брадизоиты). Ооцисты токсоплазмы могут быть обнаружены в почве или воде, загрязненной кошачьими фекалиями, что делает потребление сырых овощей и воды из небезопасных питьевых источников важным фактором риска заражения. Потребление сырого или недоваренного мяса также является фактором риска, поскольку домашний скот и дичь часто содержат брадизоиты. Паразит также может передаваться внутриутробно развивающемуся плоду, если женщина заразилась впервые во время беременности. Трансплантация твердых органов, таких как трансплантация сердца, печени и почек, является еще одним средством, при помощи которого может возникнуть инфекция T. gondii , хотя это случается очень редко.
В борьбе с болезнями, их профилактике и ликвидации ключевую роль играет выявление факторов риска инфицирования. Горизонтальная передача T. gondii может происходить при контакте с подстилкой для кошачьих туалетов, потреблении сырого мяса, употреблении сырых или недоваренных овощей, трансплантации органов и переливании крови. Владение кошкой, контакт с наполнителем для кошачьего туалета и обращение с сырым мясом – важные факторы риска заражения токсоплазмоза Поскольку T. gondii размножается половым путем в желудочно-кишечном тракте домашних животных из семейства кошачьих, у лиц, которые владели кошками или регулярно контактировали с наполнителем для кошачьего туалета, риск заражения T. gondii был на 76% и 66% выше, соответственно, по сравнению с людьми, которые не владели кошками и не держали кошек. Кроме того, поскольку T. gondii способен проникать в ткани инфицированных животных, люди, регулярно работающие с сырым мясом, также подвергаются большему риску заражения.
T. gondii способен проникать в любую ядросодержащую клетку, включая незрелые эритроциты. В качестве механизма выживания внутриклеточные паразиты должны покинуть и повторно заразить другие клетки. Механизм выхода T. gondii из инфицированных клеток до сих пор неясен. Некоторые исследования in vitro продемонстрировали, что T. gondii покидает клетку, оказывая натяжение на мембрану клетки-хозяина, часто вызывая разрыв клетки. Другие исследования показали, что паразит покидает клетку-хозяин, разрушая цитоскелет подобно Plasmodium , что приводит к лизису клеток.
Передача паразита при беременности и дети, рожденные с токсоплазмозом
Способность почти всех подклассов IgG – за заметным исключением IgG2 – проникать через плаценту обеспечивает некоторую форму защиты плода . Период беременности, в котором будущая мама заражается, сильно влияет на частоту и тяжесть заболевания. Инфекция в первом триместре беременности несет примерно 6% риск передачи плоду, тогда как во втором и третьем триместрах риск врожденной передачи составляет примерно 33–47% и 60–81% соответственно . В отличие от гестационного риска передачи, риск развития клинических симптомов заболевания (врожденный токсоплазмоз) наивысший, когда инфицирование матери происходит в течение первого триместра, и постепенно снижается во втором и третьем триместрах
Врожденная передача T. gondii сопряжена с риском выкидыша или мертворождения, а дети, рожденные с токсоплазмозом, могут страдать от серьезных симптомов, таких как гидроцефалия, кальцификаты мозга или ретинохориоидит, в более позднем возрасте, если не лечить токсоплазмоз
Группа крови RhD защищает от токсоплазмоза
Наконец, пять независимых исследований, проведенных с участием доноров крови, беременных женщин и военнослужащих, показали, что положительная группа крови RhD, особенно у гетерозигот RhD, защищает инфицированных субъектов от различных эффектов латентного токсоплазмоза, таких как увеличение времени реакции, повышенный риск во время дорожного движения несчастные случаи и чрезмерная прибавка веса при беременности
Токсоплазмоз , как причина дорожных аварий
Токсоплазмоз увеличивает время реакции инфицированных субъектов, что может объяснить повышенную вероятность дорожно-транспортных происшествий у инфицированных людей, о которой сообщалось в трех ретроспективных и одном очень большом проспективном исследовании «случай-контроль».
Лабораторная диагностика токсоплазмоза
Во время острой первичной инфекции T. gondii сначала вырабатывается иммуноглобулин M (IgM) против T. gondii . Однако титры IgM снижаются в течение следующих нескольких месяцев и становятся неопределяемыми в течение года. Иммунная система также продуцирует IgG к T. gondii через несколько недель после первоначального заражения. Уровни антител IgG обычно достигают пика в течение одного или двух месяцев после заражения, но обнаруживаются на протяжении всей жизни инфицированного человека.
Нейроиммунологические эффекты паразита
Эффекты токсоплазмы (паразита ) связаны не с манипуляциями в эволюционном смысле, а просто с неврологическими или точнее нейроиммунологическими эффектами присутствия паразита. Тахизоиты могут проникать в различные типы нервных клеток, такие как нейроны, астроциты и микроглиальные клетки головного мозга, а также клетки Пуркинье в мозжечке. Внутриклеточные тахизоиты манипулируют несколькими признаками механизмов трансдукции, участвующих в апоптозе, функциях противомикробных эффекторов и созревании иммунных клеток.
Скрытый токсоплазмоз связан с иммуносупрессией, что может объяснить повышенную вероятность рождения мальчика у инфицированных токсоплазмой женщин, а также чрезвычайно высокую распространенность токсоплазмоза у матерей детей с синдромом Дауна.
Предполагается, что наличие кист паразитов в головном мозге вызывает повышение концентрации дофамина.
Эпидемиологические исследования
Распространенность антител против T. gondii.зарегистрирован по всему миру и колеблется от 51% до 72% в нескольких странах Латинской Америки и Карибского бассейна, включая Аргентину, Бразилию, Кубу, Ямайку и Венесуэлу. Сообщается, что в Скандинавии серопозитивность антител, специфичных к T. gondii , колеблется от 11% до 28%, в то время как в Юго-Восточной Азии, Китае и Корее серопозитивность к воздействию T. gondii оценивается в диапазоне от 4% до 39%. женщины репродуктивного возраста . Кроме того, как активные, так и латентные инфекции T. gondii были зарегистрированы во многих африканских странах, особенно у людей, страдающих ВИЧ / СПИДом. Например, 88,2% ВИЧ-инфицированных, обратившихся за медицинской помощью в больницу Арба-Минч в Эфиопии, также имели серопозитивные Т. гондий инфекция , а исследование , проведенное в Буркина – Фасо среди беременных женщин показали общие серораспространенности 31,1%.
Эпидемиологические исследования указывают на роль токсоплазмоза в этиологии шизофрении, вероятно, во время беременности и в раннем периоде жизни. Эта связь согласуется с исследованиями на животных моделях, указывающими, что воздействие на развивающийся мозг животных инфекционных агентов или иммуномодулирующих агентов может быть связано с изменениями поведения ( психопатологическая симптоматика ) , которые не проявляются, пока животное не достигнет полной зрелости.
Toxoplasma gondii и психические расстройства
Пациенты с психическими расстройствами имеют повышенный уровень токсоплазматических антител, причем разница между случаями и контрольной группой наибольшая у лиц, обследованных незадолго до появления психопатологических симптомов.
Токсоплазмоз и шизофрения
Повышение уровня дофамина в мозге инфицированных субъектов может представлять собой недостающее звено между токсоплазмозом и шизофренией. Токсоплазма также, по-видимому, участвует в возникновении более тяжелых форм шизофрении. По крайней мере 40 исследований подтвердили повышенную распространенность токсоплазмоза среди больных шизофренией. Больные шизофренией, инфицированные токсоплазмой, отличаются от больных шизофренией, не страдающих токсоплазмой, анатомией головного мозга и большей интенсивностью бреда и галлюцинаций
Токсоплазмоз и обсессивно – компульсивное расстройство
Токсоплазмоз и обсессивно-компульсивное расстройство (ОКР): уровень серопозитивности для анти-Т. gondii IgG антител у пациентов с ОКР значительно выше, чем у здоровых добровольцев. Инфекция базальных ганглиев может быть вовлечена в патогенез ОКР у серопозитивных субъектов на токсоплазм.
Токсоплазмоз и личность
Инфицированные паразитом мужчины кажутся более догматичными, менее уверенными, более ревнивыми, более осторожными, менее импульсивными и более упорядоченными, чем другие. И наоборот, инфицированные женщины становятся более теплыми, сознательными, неуверенными в себе, более ханжескими и настойчивыми, чем другие представительницы этого пола. Инфицированные токсоплазмой люди отличаются от неинфицированных контрольных групп по профилю личности, оцененному с помощью двух вариантов опросников 16PF Кеттелла, TCI Клонингера и большой пятерки. Большинство этих различий увеличивается с течением времени с момента начала инфекции, предполагая, что токсоплазма влияет на личность человека, а не личность человека, влияет на вероятность заражения. Недавно в литературе сообщалось об отрицательной связи между инфекцией токсоплазмы и стремлением к новизне.
У людей с положительной реакцией на токсоплазмы были более низкие показатели поиска новизны (NS) (P = 0,035) и более низкие оценки по трем из четырех подшкал, а именно по импульсивности , экстравагантности и беспорядку, чем у субъектов с отрицательной реакцией на токсоплазму.
Токсоплазмоз и цитомегаловирус
Снижение стремления к новизне связано также с цитомегаловирусной инфекцией. Поскольку цитомегаловирус распространяется в популяции путем прямого контакта (а не путем хищничества, как с токсоплазмой), наблюдаемые изменения являются побочным продуктом инфекций головного мозга, а не результатом манипуляционной активности паразита.
Токсоплазмоз и гормоны
Студенты-мужчины, инфицированные токсоплазмой, примерно на 3 см выше, чем испытуемые, свободные от токсоплазмы, и их лица оцениваются женщинами как более мужественные и доминирующие. Эти различия могут быть вызваны повышенной концентрацией тестостерона.
Лечение токсоплазмоза
Больных токсоплазмозом можно лечить с помощью комбинации таких препаратов, как пириметамин и сульфадиазин ( антибиотик ) , а также фолиевой кислоты. Используются также такие препараты, как «Фансидар», «Ровамицин» и «Бисептол»
Влияние антипсихотиков и нормотимиков на паразита
Галоперидол и стабилизатор настроения вальпроевая кислота наиболее эффективно ингибируют рост токсоплазмы in vitro с синергической активностью.
Исследование , проведенные в нашей клинике ( ООО “Психическое здоровье” )
В нашей клинике мы сравнили повышенные титры IgG к токсоплазме с особенностями психопатологической симптоматики и тем или иным психическим расстройством , а также проанализировали общий анализ крови больных токсоплазмозом и рядом психических расстройств.
Оказалось, что для хронического токсоплазмоза характерно : снижение таких показателей общего анализа крови , как MCV и MCH , то есть регистрируются признаки микроцитарной анемии; также снижено, общее количество лейкоцитов , и в частности, нейтрофилов и в то же время повышен MPV ( объем тромбоцитов , указывающий на их большие размеры и повышенную активность). Интересно отметить, что согласно экспериментальным наблюдениям Biswas et al., (2017) истощение нейтрофилов приводит к снижению продукции IFN-γ, что приводит к увеличению паразитарной нагрузки на центральную нервную систему. Несмотря на то, что точные молекулярные процессы, управляющие этими различиями, все еще неясны, появляется все больше доказательств того, что латентный токсоплазмоз может вызывать хроническое воспаление низкой степени тяжести, которое, в свою очередь, может приводить к анемии
Для шизофрении характерны аналогичные изменения ( снижение лейкоцитов и нейтрофилов , повышение MPV, но отсутствуют признаки микроцитарной анемии ( MCV и MCH обычно повышены) . Кровь больного рекуррентной депрессией несколько похожа на кровь больного с хроническим токсоплазмозом ( микроцитарная анемия , повышение MPV ) , однако , повышено количество лейкоцитов и нейтрофилов при рекуррентной депрессии, напротив , в отличие от крови пациентов с повышенными титрами IgG к токсоплазме. По большинству показателей общий анализ крови больного хроническим токсоплазмозом напоминал параметры крови больного с обсессивно – компульсивным расстройством.
Исходя из вышесказанно, можно предположить , что такие препараты, как Пириметамин и Сульфадиазин, а также «Фансидар», «Ровамицин» и «Бисептол». могут быть полезны больным с ОКР с высокими титрами IgG к токсоплазме.


