Острый лимфобластный лейкоз
Острый лимфобластный лейкоз – это злокачественная патология костного мозга и крови, которая заключается в продуцировании кроветворным органом бластных (незрелых) лейкоцитов. Эти клетки неспособны выполнять свою функцию и постепенно вытесняют нормальные клетки, что приводит к катастрофическому падению иммунитета, анемии, инфекционным воспалительным процессам, кровотечениям и другим нарушениям нормальной жизнедеятельности организма. Заболевание развивается очень быстро и при отсутствии квалифицированной медицинской помощи в течение нескольких месяцев приводит к летальному исходу.
Общепринятая классификация острых лимфобластных лейкозов (ОЛЛ) подразделяет их на две группы, в зависимости от типа пораженных лейкоцитов.
- В-клеточный (до 85% всех случаев) наиболее характерен для детского возраста, причем пик заболеваемости приходится на 3-й год жизни. Взрослые заболевают крайне редко. Вторая группа риска – это люди старше 60 лет, но среди пожилых людей заболеваемость в 5-6 раз ниже, чем у детей
- Т-клеточный (15-20% случаев) характеризуется более тяжелым течением и высокой агрессивностью. Наибольшее количество заболевших приходится на 15-летний возраст.
Патологическая мутация В-лейкоцитов и Т-лейкоцитов может происходить на разных этапах созревания. Если в крови появляются недозрелые клетки, мутировавшие на начальных этапах, то к названию формы лейкоза добавляют приставку «пре». Это отличает лимфоцитарные онкопатологии от острого нелимфобластного лейкоза, при котором такого разделения нет.
Симптомы
Первые проявления острого лимфоидного лейкоза неспецифичны и характерны для многих заболеваний:
- бледность кожных покровов из-за развивающейся анемии;
- вялость, упадок сил, сонливость;
- частые инфекционные заболевания из-за снижения иммунитета;
- повышенная температура тела.
С развитием болезни, увеличением в крови количества бластных лимфоцитов и недостатком здоровых клеток появляются более выраженные симптомы:
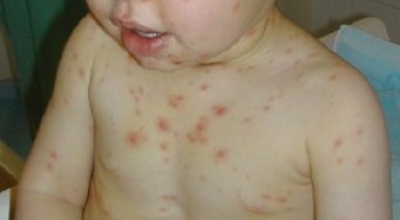
- кровоточивость слизистых оболочек;
- синяки, точечные кожные кровоизлияния;
- длительное заживление даже небольших царапин и ранок, сопровождающееся инфицированием, воспалениями, нагноениями;
- боли в конечностях, вызванные ростом опухоли костного мозга;
- увеличение размеров печени, селезенки, лимфоузлов, приводящие к болям в животе;
- затрудненное дыхание, одышка;
- паралич лицевого нерва, ухудшение зрения, рвота из-за поражения мозговых оболочек.
В каждом отдельном случае формируется индивидуальный симптомокомплекс, в который перечисленные признаки могут входить частично или полностью.
Причины и факторы риска
Непосредственной причиной заболевания всегда становится злокачественная мутация клеток кроветворной системы, из-за которой они становятся способны к быстрому бесконтрольному размножению. Существует предположение, что изменение генома происходит еще во время внутриутробного развития, но до определенного момента процесс остается незавершенным. «Спусковым крючком» нередко становятся внешние обстоятельства:
- радиоактивное излучение любой природы, в том числе во время лечения других форм рака;
- некоторые химические соединения – бензол, определенные препараты химиотерапии;
- вирусные инфекции (Эпштейна-Барр, HTLV);
- унаследованная предрасположенность.
Острый лимфоцитарный лейкоз часто развивается у детей, реже – у людей старше 60 лет, совсем редко – у взрослых. Представители белой расы заболевают чаще темнокожих, мужчины – несколько чаще женщин.
Стадии
Поскольку при онкозаболеваниях крови опухоль, как таковая, не развивается, то общие критерии стадийности для оценки их течения не подходят. Начальной стадией острого лимфобластного лейкоза считают период от появления злокачественного клона до появления выраженных симптомов. Далее выделяют следующие этапы.
- Первая атака, или дебют. В это время заболевание стремительно развивается, пациент обращается к врачу, его помещают в гематологический стационар и проводят индукционную терапию.
- Ремиссия. Она может быть полной, со снижением уровня бластных лейкоцитов менее 5% и наличием в миелограмме всех здоровых ростков кроветворения, и частичной, при которой улучшение показателей крови является временным и через определенный период прекращается.
- Рецидив. Состояние наступает после ремиссии и характеризуется возвратом признаков заболевания с повышением уровня бластоза выше 5%. Выделяют ранний (с ремиссией менее года) и поздний (с ремиссией дольше года) рецидив острого лимфобластного лейкоза.
Иногда после нескольких ремиссий и рецидивов у пациента наступает терминальная стадия, при которой проводимая терапия не дает никаких результатов. После этого неизбежно наступает летальный исход. У большинства больных результаты лечения оказываются более благоприятными, и после ремиссии, как правило, происходит выздоровление.
Диагностика
Чтобы диагностировать острый лимфоцитарный лейкоз, необходим ряд лабораторных анализов и инструментальных исследований.
Общий анализ крови обязательно проводят с подсчетом лейкоцитарной формулы, чтобы выявить первичные признаки болезни.
Биохимический анализ крови проводят для уточнения состояния внутренних органов, в частности – печени и почек.
Биопсия костного мозга из подвздошной кости предоставляет материал для основных исследований.
Рентген грудной клетки необходим для выявления увеличенных лимфоузлов, а также для определения воспалительного процесса в легких.
В процессе лечения может появиться необходимость в дальнейших диагностических и мониторинговых исследованиях.
Вы можете бесплатно получить медицинскую помощь в АО «Медицина» (клиника академика Ройтберга) по программе по программе Государственных гарантий ОМС (Обязательного медицинского страхования) и ВМП (высокотехнологичной медицинской помощи).
Чтобы узнать подробности, позвоните, пожалуйста, по телефону +7 (495) 775-73-60 , или можете прочитать более подробно здесь…
Лечение
Стратегию лечения острого лимфобластного лейкоза разрабатывает и утверждает консилиум, в который входят медики нескольких специализаций: онколог общего профиля, химиотерапевт, радиолог, гематолог, другие специалисты. Как правило, пациенту назначают комплекс мероприятий, включающий наиболее эффективные методики.
Химиотерапия является ключевым методом при онкозаболеваниях крови и костного мозга. Современные препараты эффективно уничтожают злокачественные клетки либо угнетают их рост и деление. В зависимости от показаний, каждому пациенту разрабатывают индивидуальный курс с несколькими разными химиопрепаратами. Если они не оказывают желаемого эффекта, назначения корректируют с учетом новых данных.
Лучевая терапия используется в качестве вспомогательного метода при лечении некоторых подвидов заболевания. Наиболее часто она предшествует хирургической операции по пересадке костного мозга, когда требуется тотальное уничтожение опухолевых клеток.
Лечение состоит из нескольких этапов:
- подготовительного, необходимого для снижения количества лейкозных клеток в крови;
- индукции ремиссии – интенсивного курса, целью которого является максимально возможное уничтожение опухоли;
- консолидации, направленной на закрепление результата и уничтожение остаточных очагов;
- реиндукции, или повторении индукции, чтобы полностью исключить вероятность рецидива;
- поддерживающей терапии, которая при успешном лечении продолжается около двух лет и состоит из небольших доз цитостатиков.
Между этапами делаются перерывы, необходимые для восстановления организма после воздействия тяжелых препаратов.
Прогнозы
При остром лимфобластном лейкозе прогноз зависит, в первую очередь, от возраста пациента. У детей выздоровление наступает в 80-90% случаев. Для взрослых этот показатель в настоящее время составляет 40-45%, причем у более молодых пациентов шансы существенно выше, чем у людей старше 60 лет. Не следует забывать, что за последние годы онкологи добились существенных успехов в лечении заболеваний крови. Ежегодно появляются новые, все более эффективные и безопасные химиопрепараты направленного действия.
Профилактика
Специальных мер для предупреждения острого лимфоидного лейкоза не существует. Чтобы снизить риски заболевания, необходимо придерживаться здорового образа жизни, укреплять естественный иммунитет, избегать радиационных и канцерогенных воздействий.
Реабилитация
В течение реабилитационного периода пациент нуждается в полном восстановлении функций организма, для чего необходимо:
- поддерживать и укреплять иммунную систему;
- восстанавливать кишечную микрофлору;
- выводить из организма токсины, образовавшиеся после распада патогенных клеток;
- укреплять нервную систему, бороться со стрессами и депрессивными состояниями.
Диагностика и лечение острого лимфобластного лейкоза в Москве
Если у вас или члена вашей семьи обнаружены признаки острого лимфобластного лейкоза, обратитесь в клинику «Медицина». Мы предлагаем своим пациентам:
- лечение у онкологов, химиотерапевтов, гематологов высокой квалификации;
- диагностику с использованием новейшего медицинского оборудования;
- пребывание в комфортабельной палате стационара под круглосуточным наблюдением;
- медицинский сервис в соответствии с жесткими стандартами мировой медицины.
Позвоните нам, чтобы выяснить интересующие вас подробности и записаться на консультацию.
Вопросы и ответы
Сколько живут при остром лимфобластном лейкозе?
Заболевание отличается стремительным течением, поэтому без медицинской помощи летальный исход наступает в течение нескольких месяцев. При своевременно начатом лечении шансы прожить более 7 лет имеются у 80-90% детей и около 40% взрослых.
Сколько времени продолжается лечение острого лимфобластного лейкоза?
- Подготовительный этап лечения продолжается 1-2 недели.
- Индукция – до 8 недель.
- Консолидация – до 4 месяцев.
- Реиндукция – несколько месяцев.
- Поддерживающая терапия – до полутора лет.
Общая продолжительность лечения составляет примерно два или два с половиной года.
Как понять, что у тебя острый лимфобластный лейкоз?
Если у вас появились:
- симптомы общего недомогания – вялость, слабость, повышенная температура;
- кровотечения из носа, десен, других слизистых оболочек;
- плохо заживающие ранки на коже;
- сильная потливость по ночам –
необходимо как можно скорее обратиться к онкологу или гематологу и сделать анализы. Перечисленные симптомы далеко не всегда свидетельствуют о начале острого лимфобластного лейкоза, однако это заболевание развивается стремительно и агрессивно. Для успеха лечения дорог буквально каждый день.
Внимание!
Вы можете бесплатно вылечить это заболевание и получить медицинскую помощь в АО «Медицина» (клиника академика Ройтберга) по программе Государственных гарантий ОМС (Обязательного медицинского страхования) и ВМП (выскокотехнологичной медицинской помощи).
Чтобы узнать подробности, позвоните, пожалуйста, по телефону +7(495) 775-73-60, или на странице ВМП по ОМС
Острый лимфобластный лейкоз
Острый лимфобластный лейкоз – злокачественное поражение системы кроветворения, сопровождающееся неконтролируемым увеличением количества лимфобластов. Проявляется анемией, симптомами интоксикации, увеличением лимфоузлов, печени и селезенки, повышенной кровоточивостью и дыхательными расстройствами. Из-за снижения иммунитета при остром лимфобластном лейкозе часто развиваются инфекционные заболевания. Возможно поражение ЦНС. Диагноз выставляется на основании клинических симптомов и данных лабораторных исследований. Лечение – химиотерапия, радиотерапия, пересадка костного мозга.
МКБ-10
Общие сведения
Острый лимфобластный лейкоз (ОЛЛ) – самое распространенное онкологическое заболевание детского возраста. Доля ОЛЛ составляет 75-80% от общего количества случаев болезней системы кроветворения у детей. Пик заболеваемости приходится на возраст 1-6 лет. Мальчики страдают чаще девочек. Взрослые пациенты болеют в 8-10 раз реже детей. У пациентов детского возраста острый лимфобластный лейкоз возникает первично, у взрослых нередко является осложнением хронического лимфоцитарного лейкоза. По своим клиническим проявлениям ОЛЛ схож с другими острыми лейкозами. Отличительной особенностью является более частое поражение оболочек головного и спинного мозга (нейролейкоз), при отсутствии профилактики развивающееся у 30-50% пациентов. Лечение осуществляют специалисты в области онкологии и гематологии.
В соответствии с классификацией ВОЗ различают четыре типа ОЛЛ: пре-пре-В-клеточный, пре-В-клеточный, В-клеточный и Т-клеточный. В-клеточные острые лимфобластные лейкозы составляют 80-85% от общего количества случаев заболевания. Первый пик заболеваемости приходится на возраст 3 года. В последующем вероятность развития ОЛЛ повышается после 60 лет. Т-клеточный лейкоз составляет 15-20% от общего количества случаев болезни. Пик заболеваемости приходится на возраст 15 лет.

Причины острого лимфобластного лейкоза
Непосредственной причиной острого лимфобластного лейкоза является образование злокачественного клона – группы клеток, обладающих способностью к неконтролируемому размножению. Клон образуется в результате хромосомных аберраций: транслокации (обмена участками между двумя хромосомами), делеции (утраты участка хромосомы), инверсии (переворота участка хромосомы) или амплификации (образования дополнительных копий участка хромосомы). Предполагается, что генетические нарушения, вызывающие развитие острого лимфобластного лейкоза, возникают еще во внутриутробном периоде, однако для завершения процесса формирования злокачественного клона нередко требуются дополнительные внешние обстоятельства.
В числе факторов риска возникновения острого лимфобластного лейкоза обычно в первую очередь указывают лучевые воздействия: проживание в зоне с повышенным уровнем ионизирующей радиации, радиотерапию при лечении других онкологических заболеваний, многочисленные рентгенологические исследования, в том числе во внутриутробном периоде. Уровень связи, а также доказанность наличия зависимости между различными лучевыми воздействиями и развитием острого лимфобластного лейкоза сильно различаются.
Так, взаимосвязь между лейкозами и лучевой терапией в наши дни считается доказанной. Риск возникновения острого лимфобластного лейкоза после радиотерапии составляет 10%. У 85% пациентов болезнь диагностируется в течение 10 лет после окончания курса лучевой терапии. Связь между рентгенологическими исследованиями и развитием острого лимфобластного лейкоза в настоящее время остается на уровне предположений. Достоверных статистических данных, подтверждающих эту теорию, пока не существует.
Многие исследователи указывают на возможную связь между ОЛЛ и инфекционными заболеваниями. Вирус возбудителя острого лимфобластного лейкоза пока не выявлен. Существуют две основные гипотезы. Первая – ОЛЛ вызывается одним пока не установленным вирусом, однако болезнь возникает только при наличии предрасположенности. Вторая – причиной развития острого лимфобластного лейкоза могут стать разные вирусы, риск развития лейкоза у детей повышается при недостатке контактов с патогенными микроорганизмами в раннем возрасте (при «нетренированности» иммунной системы). Пока обе гипотезы не доказаны. Достоверные сведения о наличии связи между лейкозами и вирусными заболеваниями получены только для Т-клеточных лейкозов у взрослых больных, проживающих в странах Азии.
Вероятность развития острого лимфобластного лейкоза повышается при контакте матери с некоторыми токсическими веществами в период гестации, при некоторых генетических аномалиях (анемии Фанкони, синдроме Дауна, синдроме Швахмана, синдроме Клайнфельтера, синдроме Вискотта-Олдрича, нейрофиброматозе, целиакии, наследственно обусловленных иммунных нарушениях), наличии онкологических заболеваний в семейном анамнезе и приеме цитостатиков. Некоторые специалисты отмечают возможное негативное влияние курения.
Симптомы острого лимфобластного лейкоза
Болезнь развивается стремительно. К моменту постановки диагноза суммарная масса лимфобластов в организме может составлять 3-4% от общей массы тела, что обусловлено бурной пролиферацией клеток злокачественного клона на протяжении 1-3 предыдущих месяцев. В течение недели количество клеток увеличивается примерно вдвое. Различают несколько синдромов, характерных для острого лимфобластного лейкоза: интоксикационный, гиперпластический, анемический, геморрагический, инфекционный.
Интоксикационный синдром включает в себя слабость, утомляемость, лихорадку и потерю веса. Повышение температуры может провоцироваться как основным заболеванием, так и инфекционными осложнениями, которые особенно часто развиваются при наличии нейтропении. Гиперпластический синдром при остром лимфобластном лейкозе проявляется увеличением лимфоузлов, печени и селезенки (в результате лейкемической инфильтрации паренхимы органов). При увеличении паренхиматозных органов могут появляться боли в животе. Увеличение объема костного мозга, инфильтрация надкостницы и тканей суставных капсул могут становиться причиной ломящих костно-суставных болей.
О наличии анемического синдрома свидетельствуют слабость, головокружения, бледность кожи и учащение сердечных сокращений. Причиной развития геморрагического синдрома при остром лимфобластном лейкозе становятся тромбоцитопения и тромбозы мелких сосудов. На коже и слизистых выявляются петехии и экхимозы. При ушибах легко возникают обширные подкожные кровоизлияния. Наблюдаются повышенная кровоточивость из ран и царапин, кровоизлияния в сетчатку, десневые и носовые кровотечения. У некоторых больных острым лимфобластным лейкозом возникают желудочно-кишечные кровотечения, сопровождающиеся кровавой рвотой и дегтеобразным стулом.
Иммунные нарушения при остром лимфобластном лейкозе проявляются частым инфицированием ран, царапин и следов от уколов. Могут развиваться различные бактериальные, вирусные и грибковые инфекции. При увеличении лимфатических узлов средостения отмечаются нарушения дыхания, обусловленные уменьшением объема легких. Дыхательная недостаточность чаще обнаруживается при Т-клеточном остром лимфобластном лейкозе. Нейролейкозы, спровоцированные инфильтрацией оболочек спинного и головного мозга, чаще отмечаются во время рецидивов.
При вовлечении ЦНС выявляются положительные менингеальные симптомы и признаки повышения внутричерепного давления (отек дисков зрительных нервов, головная боль, тошнота и рвота). Иногда поражение ЦНС при остром лимфобластном лейкозе протекает бессимптомно и диагностируется только после исследования цереброспинальной жидкости. У 5-30% мальчиков появляются инфильтраты в яичках. У пациентов обоих полов на коже и слизистых оболочках могут возникать багрово-синюшные инфильтраты (лейкемиды). В редких случаях наблюдаются выпотной перикардит и нарушения функции почек. Описаны случаи поражений кишечника.
С учетом особенностей клинической симптоматики можно выделить четыре периода развития острого лимфобластного лейкоза: начальный, разгара, ремиссии, терминальный. Продолжительность начального периода составляет 1-3 месяца. Преобладает неспецифическая симптоматика: вялость, утомляемость, ухудшение аппетита, субфебрилитет и нарастающая бледность кожи. Возможны головные боли, боли в животе, костях и суставах. В период разгара острого лимфобластного лейкоза выявляются все перечисленные выше характерные синдромы. В период ремиссии проявления болезни исчезают. Терминальный период характеризуется прогрессирующим ухудшением состояния больного и завершается летальным исходом.
Диагностика острого лимфобластного лейкоза
Диагноз выставляют с учетом клинических признаков, результатов анализа периферической крови и данных миелограммы. В периферической крови пациентов с острым лимфобластным лейкозом выявляются анемия, тромбоцитопения, повышение СОЭ и изменение количества лейкоцитов (обычно – лейкоцитоз). Лимфобласты составляют 15-20 и более процентов от общего количества лейкоцитов. Количество нейтрофилов снижено. В миелограмме преобладают бластные клетки, определяется выраженное угнетение эритроидного, нейтрофильного и тромбоцитарного ростка.
В программу обследования при остром лимфобластном лейкозе входят люмбальная пункция (для исключения нейролейкоза), УЗИ органов брюшной полости (для оценки состояния паренхиматозных органов и лимфатических узлов), рентгенография грудной клетки (для обнаружения увеличенных лимфоузлов средостения) и биохимический анализ крови (для выявления нарушений функции печени и почек). Дифференциальный диагноз острого лимфобластного лейкоза проводят с другими лейкозами, отравлениями, состояниями при тяжелых инфекционных заболеваниях, инфекционным лимфоцитозом и инфекционным мононуклеозом.
Лечение и прогноз при остром лимфобластном лейкозе
Основой терапии являются химиопрепараты. Выделяют два этапа лечения ОЛЛ: этап интенсивной терапии и этап поддерживающей терапии. Этап интенсивной терапии острого лимфобластного лейкоза включает в себя две фазы и длится около полугода. В первой фазе осуществляют внутривенную полихимиотерапию для достижения ремиссии. О состоянии ремиссии свидетельствуют нормализация кроветворения, наличие не более 5% бластов в костном мозге и отсутствие бластов в периферической крови. Во второй фазе проводят мероприятия для продления ремиссии, замедления или прекращения пролиферации клеток злокачественного клона. Введение препаратов также осуществляют внутривенно.
Продолжительность этапа поддерживающей терапии при остром лимфобластном лейкозе составляет около 2 лет. В этот период больного выписывают на амбулаторное лечение, назначают препараты для перорального приема, осуществляют регулярные обследования для контроля над состоянием костного мозга и периферической крови. План лечения острого лимфобластного лейкоза составляют индивидуально с учетом уровня риска у конкретного больного. Наряду с химиотерапией используют иммунохимиотерапию, радиотерапию и другие методики. При низкой эффективности лечения и высоком риске развития рецидивов осуществляют трансплантацию костного мозга. Средняя пятилетняя выживаемость при В-клеточном остром лимфобластном лейкозе в детском возрасте составляет 80-85%, во взрослом – 35-40%. При Т-лимфобластном лейкозе прогноз менее благоприятен.
Острый лимфобластный лейкоз

Острым лимфобластным лейкозом (общепринятая аббревиатура — ОЛЛ) называют злокачественное заболевание крови и костного мозга, при котором кроветворный орган неконтролируемо продуцирует незрелые (бластные) лимфоциты. Это приводит к резкому ухудшению состояния больного, повышает риск кровотечений и восприимчивость к инфекциям. Наиболее часто болезнь поражает детей в возрасте от года до шести лет, причём у мальчиков она встречается чаще, чем у девочек. Взрослые страдают от ОЛЛ на порядок реже детей, причём самые высокие показатели заболеваемости — у пожилых людей старше 60 лет.
По типу поражённых лимфоцитов клинические случаи подразделяются на:
- В-клеточные, на долю которых приходится до 85% больных, у которых кроветворный орган активно продуцирует незрелые В-клетки (в здоровом организме вырабатывающие антитела к патогенам);
- Т-клеточные, составляющие до 15% пациентов, у которых продуцируются незрелые Т-клетки (в норме отвечающие за регуляцию производства антител).
Острый лимфобластный лейкоз В-типа наиболее часто поражает маленьких детей и людей старшей возрастной группы. Основную группу риска ОЛЛ Т-типа составляют подростки 14-15 лет.
Симптомы
Первые признаки заболевания развиваются с увеличением в составе крови незрелых лимфоцитов:
- бледность кожи;
- быстрая утомляемость;
- повышенная температура тела;
- чрезмерное выделение пота, особенно по ночам;
- частые простуды;
- кровоподтёки и синяки на коже;
- потеря веса без видимых причин.
По мере распространения лейкозных клеток развиваются симптомы острого лимфоцитарного лейкоза, свидетельствующие о поражении других органов:
- головные боли, нарушения зрения и слуха, ухудшение координации движений, онемение лицевых мышц при проникновении в головной мозг и нервную систему;
- боли в костях и суставах при тотальном поражении костного мозга;
- боли в правом подреберье при метастазировании в печень и селезёнку.
Могут встречаться и другие проявления болезни, в зависимости от локализации повреждений.
Причины и факторы риска
Онкогематологи связывают появление злокачественных клонов, дающих начало острому лимфобластному лейкозу, с рядом провоцирующих факторов.
- Радиоактивное излучение, в том числе лучевая терапия по поводу другого онкозаболевания.
- Некоторые инфекционные заболевания.
- Длительный контакт с канцерогенными химическими соединениями.
- Наличие близких родственников, страдавших аналогичной онкопатологией.
- Заболевания, связанные с генетическими отклонениями.
- Курение табака.
У детей болезнь может развиваться, если мать испытывала воздействие одного или нескольких перечисленных факторов во время беременности.
Стадии
Различают следующие стадии заболевания.
- Начало. Характеризуется общим ухудшением самочувствия, появлением первых неспецифических признаков — бледности, быстрой утомляемости, появлении болей в мышцах и костях.
- Разгар. Характерные для онкопатологии симптомы ярко выражены, состояние больного резко ухудшается.
- Ремиссия. Самочувствие больного улучшается, клинико-гематологические показатели возвращаются к норме.
- Рецидив. После ремиссии количество бластных лимфоцитов вновь возрастает, возвращаются патологические симптомы.
- Терминальная стадия. Заболевание быстро прогрессирует, поражаются жизненно важные органы. Наиболее частое завершение — летальный исход.
Диагностика
Поскольку заболевание развивается очень быстро, то при обращении к онкологу или онкогематологу симптомы острого лимфоидного лейкоза у него уже, как правило, ярко выражены. Однако для подтверждения диагноза и для определения методов лечения необходимы лабораторные анализы, а также проведение инструментальных исследований:
- общий и биохимический анализы крови;
- миелограмма — исследование клеток костного мозга, цитохимический анализ, иммунофенотипирование;
- пункция спинного мозга с гистологическим и цитологическим исследованием биоптата;
- УЗИ внутренних органов и лимфоузлов;
- рентген грудной клетки;
- ЭКГ и другие исследования согласно симптоматике.
Лечение
Как правило, схема лечения острого лимфобластного лейкоза включает три основных этапа.
Индукция. Продолжительность составляет несколько недель. Интенсивная химиотерапия направлена на уничтожение злокачественных лимфоцитов. К окончанию этапа в костном мозге должно быть не более 5% незрелых клеток.
- Консолидация. Усилия онкологов направлены на закрепление достигнутого результата и предотвращение рецидива острого лимфобластного лейкоза. Для этого пациенту курсами вводят химиотерапевтические средства. На этом этапе возможна пересадка здоровых стволовых клеток для восстановления кроветворной функции. При отсутствии стойкой ремиссии и высокой угрозе рецидива может быть назначена пересадка костного мозга.
- Поддерживающая терапия. Как правило, этот этап подразумевает амбулаторное лечение, но он не менее важен, чем предыдущие для достижения стойкой ремиссии. Пациенту назначают пероральные химиотерапевтические препараты, он регулярно проходит обследования, выполняет все назначения онкогематолога.
На всех этапах лечение сопровождается приёмом антимикробных средств, переливаниями тромбоцитной массы и крови. Периодически проводится дезинтоксикация организма, чтобы очистить кровь от продуктов распада лейкозных клеток.
Прогнозы
При остром лимфобластном лейкозе прогноз благоприятен для 80-90% детей. У взрослых шансы на полное излечение достигают 40-45%, причём с возрастом они понижаются. Существенное влияние на успех лечения оказывает уровень бластных лимфоцитов в крови пациента на момент начала лечения, наличие у него хромосомных аномалий, а также распространение болезни в тканях головного мозга.
Профилактика
На сегодняшний день не существует специальных профилактических мер для безусловного предупреждения острого лимфобластного лейкоза. Общие рекомендации заключаются в поддержании здорового образа жизни, исключении курения, минимизации контактов с канцерогенными соединениями.
Реабилитация
Восстановление после химиотерапии ничем не отличается от аналогичных мер при остром нелимфобластном лейкозе и включает:
- меры, необходимые для активации собственной иммунной системы;
- приём пробиотиков и выполнение рекомендаций врача по сбалансированному питанию;
- выведение токсинов из организма;
- антистрессовую терапию, избавление от депрессивного состояния.
Важно, чтобы пациент выполнял все рекомендации онкогематолога.
Диагностика и лечение острого лимфобластного лейкоза в Москве
Квалифицированная диагностика острого лимфобластного лейкоза проводится в московской клинике Института ядерной медицины. Современное лечебно-диагностическое оборудование и высокая квалификация врачей-онкологов позволяют использовать для лечения онкозаболеваний передовые методы мировой практики с максимально высокой результативностью.
Вопросы и ответы
Какова продолжительность жизни при остром лимфобластном лейкозе?
При отсутствии лечения больной с ОЛЛ может прожить не более нескольких месяцев. Современные методики позволяют добиться полного выздоровления для 90% детей. У взрослых результативность терапии менее высока, однако у каждого пациента есть шансы, и необходимо их полностью использовать.
Нужна ли пересадка костного мозга при остром лимфобластном лейкозе?
Трансплантация костного мозга проводится только после наступления ремиссии при наличии показаний — при плохом ответе на индукционную терапию или из-за быстрого наступления рецидива. Как правило, у детей необходимости в пересадке не возникает. Костный мозг может быть взят у родственного либо у неродственного донора.
Можно ли вылечить острый лимфобластный лейкоз после рецидива?
Лечение при рецидиве заболевания зависит от локализации поражения — находится ли источник в костном мозге или вне его — например, в центральной нервной системе. Кроме того, имеет значение срок его развития — ранний либо поздний. Наиболее высоки шансы на успех при позднем рецидиве.
Острый лимфобластный лейкоз
Острый лимфобластный лейкоз чаще поражает детей. Его пик приходится на 2-4 года. Среди взрослых эта форма острого лейкоза встречается у 10-15% больных.
Патогенез (что происходит?) во время Острого лимфобластарного лейкоза:
К моменту диагностирования острого лимфобластного лейкоза опухоль уже достаточно велика, и ее масса достигает, как правило, 1 1012 клеток на 1 м2 поверхности тела и составляет около 3–4% его массы тела. Такое число лейкозных клеток может образоваться за 1-3 месяца болезни при удвоении числа лейкозных клеток в костном мозге за 4-10 дней. К моменту наступления улучшения от преднизолона и винкристина содержание лейкозных клеток снижается до 1 Ч 108 – 1 Ч 109 на 1 м2.
Симптомы Острого лимфобластарного лейкоза:
Особенность клинической картины данного лейкоза у детей заключается в частом увеличении лимфатических узлов и селезенки. В зависимости от места преимущественного увеличения лимфатических узлов меняются и признаки заболевания. При их локализации в области грудной клетки у больных появляется сухой кашель, одышка; увеличенные мезентериальные узлы могут вызывать боли в животе. Характерны боли в голенях. Однако начало острого лимфобластного лейкоза у детей достаточно редко сопровождается глубоким угнетением кроветворения, обычно отмечаются лишь нормохромная анемия и умеренная лейкопения.
Диагностика Острого лимфобластарного лейкоза:
Клиническое начало болезни может совпадать с алейкемической и лейкемической фазой. Нередко появляются неспецифические изменения в крови, связанные с нарушением структуры костного мозга: единичные эритрокариоциты, миелоциты, промиелоциты – признаки миелемии. Пункция костного мозга, выявляющая бластные клетки в большом проценте, разрешает все диагностические трудности.
Морфология бластных клеток имеет некоторые особенности: ядро с нежной сетью хроматина, как у всех бластов, обычно круглое, имеет 1-2 крупные нуклеолы во многих ядрах, цитоплазма зернистости не содержит. Как и при всех острых лейкозах, форма ядра в процессе болезни меняется: оно становится неправильным, его размеры растут; также увеличивается и ободок цитоплазмы.
Специфические гистохимические особенности этого лейкоза: бластные клетки не обнаруживают пероксидазы, фосфолипидов, эстераз, а гликоген, выявляемый PAS-реакцией, распределяется в цитоплазме глыбками в виде ожерелья вокруг ядра.
Изучение Т– и В-маркеров на бластных клетках острого лимфобластного лейкоза показало, что он представляет собой неоднородную группу. Имеются по крайней мере 3 формы этого лейкоза, выявляемые по антигенным маркерам: острый лимфобластный лейкоз с бластными клетками, имеющими маркеры В-лимфоцитов, маркеры Т-лимфоцитов и не имеющими маркеров Т– или В-лимфоцитов.
К В-форме острого лимфобластного лейкоза относятся лейкемизирующиеся стадии лимфосарком, лимфосаркомы Беркитта, очень редкие бластные кризы хронического лимфолейкоза. Лейкозным клеткам при этой форме свойственна высокая плотность IgM на их поверхности.
Клинически более четко изучены особенности Т-формы острого лимфобластного лейкоза. Вышеописанная форма наиболее часто выявляется у детей старшей возрастной группы, при этом средний возраст больных составляет 10 лет. Согласно большинству данных средняя продолжительность жизни больных с этой формой острого лейкоза составляет менее 24 месяцев, обострение в половине случаев начинается с экстрамедуллярного роста – чаще с поражения нервной системы.
Бластные клетки по своей антигенной структуре скорее напоминают тимоциты и претимоциты, чем периферические Т-клетки. Также данные клетки сохраняют некоторые функциональные свойства супрессоров. Цитохимической особенностью Т-бластов является высокая активность кислой фосфатазы, ее локализованность в цитоплазме.
Общая характеристика острого лимфобластного лейкоза относится преимущественно к его ни Т-, ни В-форме, включающей около 70% случаев.
По антигенным и энзиматическим особенностям представляющие ни Т– ни В-форму клетки лишены детерминант периферических Т- и В-лимфоцитов. Однако такие клетки имеют черты предшественников тимоцитов: реагируют с антисывороткой к тимусным антигенам, с некоторыми антисыворотками хронического лимфолейкоза, содержат много дезоксинуклеотидилтрансферазы. Следующей особенностью данных клеток является то, что они имеют много Ia-антигена, свойственного В-клеткам.
В остром лимфобластном лейкозе, кроме 3 основных выделенных по антигенным маркерам лимфоцитов форм (Т-острый лимфобластный лейкоз, В-острый лимфобластный лейкоз и ни Т– ни В-острый лимфобластный лейкоз), определено еще несколько.
Новые формы в основном отделились от ни Т– ни В-формы. Так, выделена пре-В-форма острого лимфобластного лейкоза: представляющие его бласты относятся к ранним клеткам – предшественницам В-лимфоцитов, так как они содержат цитоплазматический иммуноглобулин – тяжелую цепь IgM – и не имеют иммуноглобулинов на поверхности. Вышеописанная форма острого, по существу, В-клеточного лейкоза отличается значительно более благоприятным течением чем В-форма.
От ни Т– ни В-формы отделился лейкоз, представленный лимфобластами с теми же антигенными маркерами, но содержащими Ph’-хромосому. Эта форма острого лимфобластного лейкоза встречается у детей старшего возраста – после 10 лет; она течет неблагоприятно, давая короткое улучшение.
В небольшом проценте случаев встречается острый лимфобластный лейкоз, бласты которого относятся по иммунологической характеристике к пре-Т-лимфоцитам, к клеткам-предшественницам Т-лимфоцитов. В отличие от пре-В-формы острого лимфобластного лейкоза пре-Т, как и другие Т-клеточные острые лейкозы, относится к неблагоприятным по течению формам.
Т-клеточные формы острого лимфобластного лейкоза могут сопровождаться высокой эозинофилией. В крови при этом бывает лейкоцитоз, эозинофилия достигает 80-90%, а бластные клетки могут отсутствовать. Высокая эозинофилия требует пункции костного мозга, при которой в случае лейкоза находят высокий процент бластных клеток. В ремиссии эозинофилия исчезает и появляется вновь, иногда как первый признак рецидива.
У детей увеличение подчелюстных лимфатических узлов встречается часто из-за хронического тонзиллита, а увеличение селезенки – обычная реакция на инфекцию. Лейкозная инфильтрация лимфатических узлов придает им плотность (узлы обычно безболезненны), чаще увеличиваются надключичные лимфатические узлы, а не подчелюстные, как при тонзиллите. В сомнительных случаях всегда показана пункция органа: особенно это касается селезенки, так как в ней может быть местный рецидив с почти сплошным содержанием бластов в пунктате. Своевременная диагностика острого лимфобластного лейкоза как «быстрого» лейкоза имеет важнейшее значение не только из-за стремительности самого процесса, но и из-за заноса патологических клеток в мозговые оболочки.
По клинической картине, способности оставлять сохранными нормальные ростки кроветворения, частоте первой ремиссии острый лимфобластный лейкоз у взрослых похож на детский вариант.
Селезенка и лимфатические узлы при остром лимфобластном лейкозе увеличиваются большей частью одновременно с процессом в костном мозге. В отличие от острого миелобластного лейкоза это увеличение при данном лейкозе не есть новый этап прогрессии. Лейкемические клетки, инфильтрирующие лимфатические узлы и селезенку, оказываются, как правило, чувствительными к тем же цитостатическим препаратам, что и клетки в костном мозге.
Как правило, улучшение достигается применением комплекса цитостатических средств. Дальнейшее непрерывное лечение цитостатическими препаратами удерживает улучшение месяцы или годы. Однако у взрослых часто возникают обострения болезни. Обострение может быть либо только местным: появление нейролейкемии, инфильтрации нервных корешков или инфильтрации яичка, лейкемического эписклерита (воспаление наружной оболочки глазного яблока), либо костномозговым. Местное обострение определяется при спинномозговой пункции, либо у больных появляются боли, обусловленные инфильтрацией корешков. Костномозговое обострение может не сопровождаться выходом бластных клеток в кровь, поэтому грудную пункцию врач проводит регулярно: ежемесячно в первый год улучшения, а затем – 1 раз в 3 месяца. Кроме того, грудную пункцию делают при появлении бластов в крови и цитопении, не зависящей от цитостатиков.
Безусловным показанием к исследованию костного мозга должны быть явные клинические признаки обострения: увеличение лимфатических узлов, появление болей в костях, корешковый синдром, субфебрилитет, просто немотивированное ухудшение общего состояния. Признаки заболевания в период обострения острого лимфобластного лейкоза сильнее, чем при его первом приступе. Каждое последующее обострение развивается более злокачественно, чем предыдущие, и имеет худший прогноз.
Метастазирование процесса в яички и мозговые оболочки, наиболее частое при остром лимфобластном лейкозе детей, представляет собой новый этап опухолевой прогрессии.
процесс узлов средостения, раннее поражение центральной нервной системы и возраст моложе 1 года и старше 10 лет.
Лечение Острого лимфобластарного лейкоза:
Частота улучшений у детей при этой форме лейкоза составляет 94%, у лиц старше 15 лет – около 80%. Частота выздоровления у детей – более 50%. Прогностически неблагоприятными факторами, которые влияют на продолжительность жизни больных острым лимфобластным лейкозом, являются распространенность процесса к моменту постановки диагноза, лейкоцитоз выше 15 Ч 103 в 1 мкл, увеличение селезенки, вовлечение в процесс узлов средостения, раннее поражение центральной нервной системы и возраст моложе 1 года и старше 10 лет.
Проводится немедленное лечение цитостатическими препаратами и только по специальным программам.
Целью лечения острых лейкозов является достижение и максимальное продление улучшения или выздоровление.
Острые лимфобластный и недифференцируемый лейкозы у детей. Лечение проводится по программам (разработанным различными авторами), которые позволяют более чем у 50% детей сохранять улучшение дольше 5 лет.
Улучшение достигается за 4-6 недель с помощью одной из 3 схем, следует отметить, что данные схемы были внедрены еще в 1980-1990 гг. и до сих пор не потеряли свою актуальность.
Винкристин по 1,4 мг/м2 1 раз в 7 дней внутривенно, преднизолон по 40 мг/м2 в день (в схемах, рассчитанных на 4-6 недель, преднизолон отменяют в течение 6-8 дней).
Винкристин по 1,4 мг/м2 1 раз в 7 дней внутривенно, преднизолон по 40 мг/м2 в день, рубомицин по 60 мг/м2 2 дня подряд на 2-й неделе терапии (на 10-й и 11-й дни курса).
Винкристин по 1,4 мг/м2 1 раз в 7 дней внутривенно, преднизолон по 40 мг/м2 в день, L-аспарагиназа в течение 10 дней по 100 ЕД/кг в день внутривенно после 4-6 недель применения винкристина и преднизолона (если нет полного эффекта).
При неэффективности лечения по схеме 1 в течение 4-6 недель (у лиц моложе 10 лет) назначают лечение по схеме 2 или 3.
При отсутствии эффекта от лечения по схемам врач назначает комбинации с онковином или с винбластином.
Закрепляющие курсы проводят 1-3 раза, в зависимости от значительности нарушения условий выполнения лечения в период улучшения, протяженности этого периода, распространенности лейкемического процесса в начале лечения, полноты полученного улучшения. Если врач обнаруживает селезенку в глубине подреберья, то это может послужить основанием для повторения курса закрепляющего лечения. Если селезенка увеличена, то врач ее пунктирует и в случае ее лимфоцитарного состава назначает лечение, направленное на поддержание улучшения.
Сразу после установления диагноза проводят спинномозговую пункцию с введением в спинномозговой канал метотрексата в дозе 12,5 мг/м2; во время улучшения и курса, закрепляющего улучшение, регулярно 1 раз в 2 недели повторяют спинномозговые пункции с введением метотрексата в дозе 12,5 мг/м2. В случае обнаружения любого числа бластных клеток в спинномозговой жидкости начинают лечение нейролейкемии, профилактическое облучение головы отменяется.
Достижение улучшения обязательно подтверждается контрольной пункцией костного мозга; первую после диагностической пункцию костного мозга в период улучшения производят через 7 дней после начала лечения (уменьшение бластоза в этом пунктате на 50% от исходного и более означает хороший прогноз), затем через 4 недели от начала лечения.
Пролиферативная активность лейкозных клеток резко возрастает после периода улучшения, как и после любого цитостатического курса. В связи с этим непосредственно после достижения улучшения врач назначает поддерживающее лечение.
В комбинации в период поддерживания улучшения дозы цитостатических препаратов, исключая винкристин и преднизолон, уменьшают вдвое.
Развитие полиневрита (снижение сухожильных рефлексов, мышечного тонуса, онемение в пальцах рук и ног и в дальнейшем развитие пареза конечностей с атрофией мышц), обусловленное токсическим действием винкристина, требует снижения дозы этого препарата вдвое, а при выраженности или нарастании изменений – замены его винбластином (через несколько недель после отмены препарата полиневрит проходит). Лечение цитостатическими препаратами отменяется при уровне лейкоцитов ниже 1 Ч 103 (1000) в 1 мкл, язвенном стоматите, диарее, тяжелой рвоте, при высокой температуре, сохраняющейся более 2 дней.
Профилактику нейролейкемии при острых лимфобластном и недифференцируемом лейкозах у детей проводят при цитологически нормальном составе спинномозговой жидкости (бластных клеток нет, цитоз менее 10 в 1 мкл) с первой недели улучшения.
Первая схема профилактики: облучение головы в суммарной дозе 24 Гр и параллельно 5 введений метотрексата эндолюмбально. Профилактику можно проводить в основном амбулаторно.
Профилактика Острого лимфобластарного лейкоза:
Дозу 24 Гр на голову дают на 3 недели по 1,5 Гр за сеанс с двух латеральных полей.
Одну из двух инъекций метотрексата, вводимого 2 раза в неделю в спинномозговой канал, во время облучения головы целесообразно производить в субботу, так как в этот день, как правило, не бывает лучевой терапии, другую – в один из первых дней недели
после сеанса облучения головы; в день эндолюмбального введения метотрексата больной остается в стационаре.
В период профилактики нейролейкемии с помощью как облучения, так и введения метотрексата и цитозара, больные получают внутрь 6-меркаптопурин ежедневно в дозе 25 мг/м2 и циклофосфамид в дозе 100 мг/м2 1 раз в неделю.
После окончания профилактики нейролейкемии делают пункцию костного мозга, и если признаков рецидива нет, то начинают поддерживающую терапию.
Вторым методом профилактики нейролейкемии является эндолюмбальное введение метотрексата и цитозара. Препараты вводят с интервалом 3-4 дня, при плохой переносимости 1 раз в неделю.
Оба метода профилактики нейролейкемии надежны и позволяют отказаться от поддерживающих интралюмбальных введений метотрексата.
Непрерывное поддерживающее лечение в период улучшения острых лимфобластного и недифференцируемого лейкозов детей проводится амбулаторно, в течение 5 лет до полного улучшения. Начинают лечение сразу после достижения полного улучшения или после курсов, закрепляющих достигнутое улучшение.
Дети получают непрерывное лечение тремя препаратами по следующей схеме: 6-меркаптопурин внутрь ежедневно; метотрексат внутрь на 6-й день недели; циклофосфамид внутрь на 7-й день недели, в эти дни 6-меркаптопурин не отменяют.
Для «группы риска» в период непрерывного поддерживающего лечения тремя препаратами каждые 1,5-2 месяца проводится курс СО АР. Во время данного курса в течение недели после него поддерживающее лечение тремя препаратами отменяется, а затем в течение недели проводится половинными дозами. После этого поддерживающее лечение проводится полными дозами.
Условия проведения непрерывного лечения:
1) анализ крови с определением тромбоцитов и ретикулоцитов 1 раз в неделю;
2) при снижении уровня лейкоцитов до 1 Ч 103 – 2 Ч 103 (1000-2000) в 1 мкл врач снижает дозу цитостатических препаратов вдвое, при последующем его повышении более 2,5 Ч 103 (2500) в 1 мкл восстанавливают прежнюю дозу;
3) лечение прерывают на любом этапе при падении уровня лейкоцитов в крови ниже 1000 в 1 мкл, при значительном повышении температуры, стоматите, диарее;
4) пункцию костного мозга в первый год улучшения производят 1 раз в месяц; на 2-5-м году улучшения – 1 раз в 3 месяца.
Лечение острого лимфобластного лейкоза усиливается, когда речь идет о процессе Т-клеточной природы. По программе американских педиатров-онкологов для устранения проявлений болезни при Т-лимфобластном остром лейкозе начинают с внутривенного введения циклофосфана по 1200 мг/м2 в 1-й день лечения или между 2-м и 5-м днем (при уровне лейкоцитов более 5 Ч 104 (50 000) в 1 мкл и значительной органомегалии, требующих предварительного назначения аллопуринола из-за высокого уровня мочевой кислоты в сыворотке и опасности развития мочекислого диатеза). С 3-4-го дня (или в 1-й день, если введение циклофосфана отсрочено) еженедельно (1 раз в неделю) по этой программе, как и по программе Aur, вводится винкристин в течение 4 недели, а также
применяют преднизолон и рубомицин в дозах и в сроки, соответствующие схеме 2 лечения острого лимфобластного лейкоза.
При достижении ремиссии проводится курс ее консолидации, включающий 5-дневное непрерывное введение цитозара по 100 мг/(м2/сут.), прием тиогуанина (или 6-меркаптопурина) по 50 мг/м2 каждые 12 ч в течение 5 дней введения цитозара. Проводят 3 курса лечения цитозаром и тиогуанином (6-меркаптопурин) с интервалом между курсами 14 дней.
Затем в течение 7-14 дней внутривенно капельно вводят L-acnapaгиназу по 200-300 ЕД/кг. В случае высокого уровня лейкоцитов и большой массы опухолевых лимфатических узлов спленомегалии или гепатомегалии терапию нужно проводить, назначая больному большое количество жидкости, щелочное питье, наряду с аллопуринолом для профилактики мочекислого диатеза.
Если при Т-клеточном остром лейкозе в средостении определяются увеличенные лимфатические узлы, плохо сокращающиеся от химиотерапии, то рекомендуется локальное облучение этой области в дозе 30 Гр; локальное облучение целесообразно и при значительном увеличении лимфатических узлов любой другой области.
Лечение в период улучшения при Т-клеточном лейкозе должно быть усилено: наряду с непрерывной терапией 6-меркаптопурином, метотрексатом, циклофосфаном.
К каким докторам следует обращаться если у Вас Острый лимфобластный лейкоз:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Острого лимфобластарного лейкоза, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Лейкоз
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Лейкоз: причины появления, симптомы, диагностика и способы лечения.
Определение
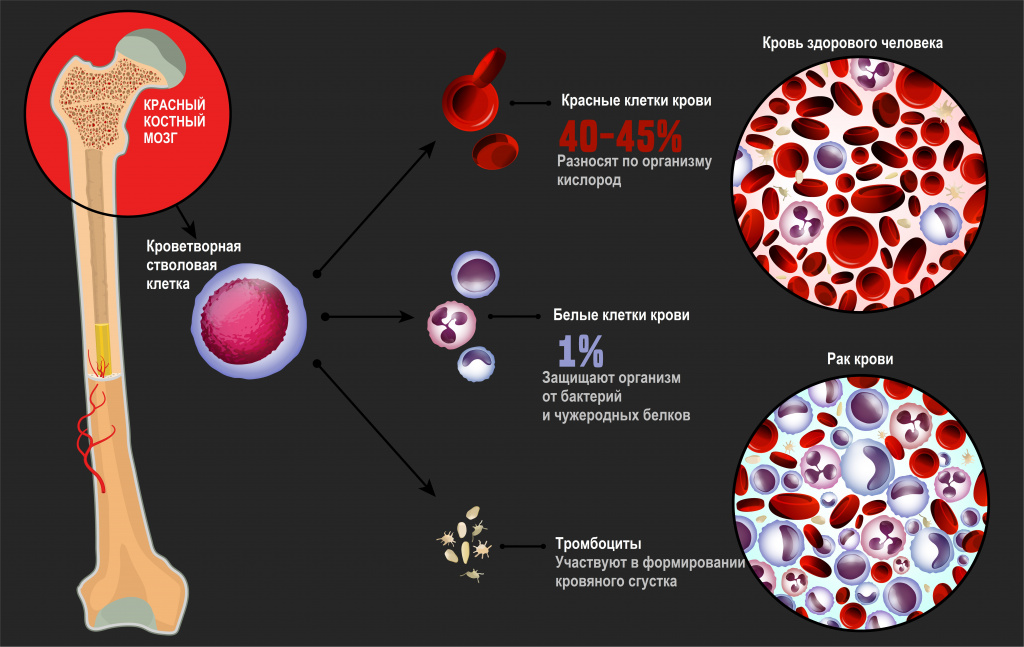
Лейкозы – большая группа заболеваний кроветворной системы. Кроветворение (гемопоэз) – это многоэтапный процесс образования форменных элементов крови в специализированных органах кроветворения. К форменным элементам крови относятся лейкоциты (белые кровяные тельца), которые участвуют во врожденном и приобретенном иммунитете, эритроциты (красные кровяные тельца), которые осуществляют транспорт кислорода и углекислого газа, и тромбоциты, обеспечивающие свертываемость крови.
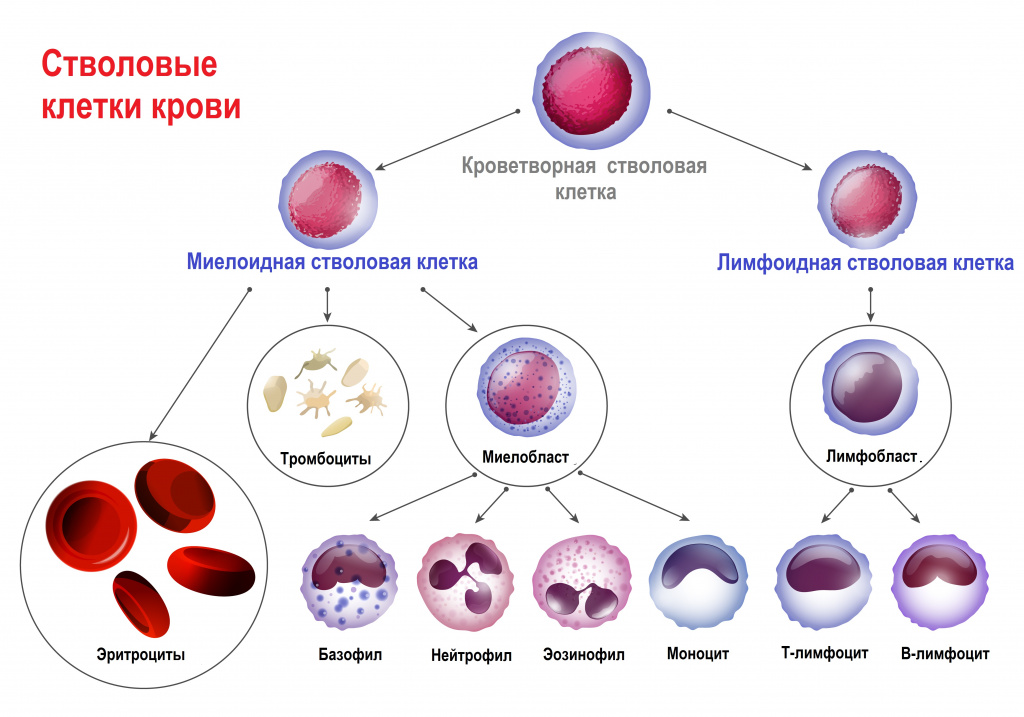
У всех клеток крови есть одна общая «родоначальница» – полипотентная стволовая клетка. Термин «полипотентная» означает, что такая клетка может развиваться в различные виды зрелых клеток.
Главный орган, где располагаются полипотентные стволовые клетки, – костный мозг, который как раз и поражается при лейкозах.
В результате повреждения (мутации) в генетическом материале полипотентной стволовой клетки-предшественницы нарушается процесс созревания клеток. При остром лейкозе возникает большое количество незрелых (бластных) клеток, из которых образуется опухоль, разрастается в костном мозге, замещает нормальные ростки кроветворения и имеет тенденцию к метастазированию – распространению с током крови или лимфы в здоровые органы. При хронических лейкозах заболевание течет годами, происходит частичная задержка созревания клеток и опухоль образуется из созревающих и зрелых клеток.
Причины возникновения лейкозов
К факторам риска развития лейкоза относятся:
- ионизирующая радиация: лучевая терапия по поводу других опухолей, облучение на рабочем месте, ультрафиолетовое излучение;
- воздействие на организм химических канцерогенных веществ;
- некоторые вирусы: HTLV (Т-лимфотропный вирус человека);
- бытовые факторы: добавки в пищевые продукты, курение, плохая экологическая обстановка;
- наследственная предрасположенность к раковым заболеваниям.
Лейкозы подразделяют на острые и хронические, а по типу поражения ростка кроветворения – на лимфоидные и миелоидные. Острый лейкоз никогда не переходит в хронический, а хронический не может стать острым (но его развитие может перейти в стадию бластного криза).
В зависимости от преобладания тех или иных опухолевых клеток выделяют бластные, цитарные и недифференцированные лейкозы.
Острый лимфобластный лейкоз (ОЛЛ) диагностируется у лиц любого возраста, начиная с младенческого и заканчивая пожилым, однако пик заболеваемости приходятся на детский возраст (60% пациентов с ОЛЛ моложе 20 лет). Острый лимфобластный лейкоз – самая распространенная опухоль кроветворной ткани у детей, которая составляет 30% всех злокачественных опухолей детского возраста. Заболеваемость ОЛЛ у пациентов пожилого возраста неуклонно возрастает: так, ежегодная частота ОЛЛ увеличивается с 0,39 случая на 100 тыс. населения в возрасте 35–39 лет, до 2,1 случая на 100 тыс. населения в возрасте ≥85 лет. Кроме того, приблизительно 30% ОЛЛ диагностируются в возрасте ≥60 лет.
Острым миелоидным лейкозом (ОМЛ) страдает в среднем 3-5 человек на 100 тыс. населения в год. Заболеваемость резко возрастает в возрасте старше 60 лет и составляет 12–13 случаев на 100 тыс. населения у лиц в возрасте старше 80 лет.
Хронический лимфобластный лейкоз (ХЛЛ) – самый частый вид лейкозов у взрослых, в то время как у детей этот вид опухоли не регистрируется. В европейских странах его частота составляет 4 случая на 100 тыс. населения в год и непосредственно связана с возрастом. У лиц старше 80 лет она составляет более 30 случаев на 100 тыс. в год.
Хронический миелолейкоз (ХМЛ) – редкое заболевание: 0,7 на 100 тыс. взрослого населения, пик заболеваемости приходится на 50-59 лет, однако до 33% больных ОМЛ – люди моложе 40 лет.
Симптомы лейкозов
Острый лейкоз в большинстве случаев дебютирует резко – внезапно повышается температура, появляются озноб, боль в горле, в суставах, отмечается резко выраженная слабость. Реже острый лейкоз может проявиться кровотечением. Иногда острый лейкоз начинается с постепенного ухудшения состояния больного, появления невыраженной боли в суставах и костях, кровоточивости. В единичных случаях возможно бессимптомное начало заболевания. У многих больных увеличиваются лимфоузлы и селезенка.
При хроническом лейкозе на начальной стадии, которая длится от года до трех лет, пациенты могут ни на что не жаловаться. Иногда беспокоят слабость, потливость, частые простудные заболевания, могут отмечаться тупые, ноющие боли в костях.
При подавлении эритроидного ростка, дающего красные кровяные тельца, возникает анемия и гемическая гипоксия (снижение количества кислорода в крови). При этом пациенты отмечают слабость, утомляемость, бледность кожных покровов.
При поражении мегакариоцитарного ростка падает количество тромбоцитов, поэтому возникает кровоточивость десен, слизистой оболочки носа, пищеварительного тракта, образуются синяки, кровоизлияния в различные органы. При прогрессировании лейкоза могут развиваться массивные кровотечения в результате ДВС синдрома (синдрома диссеминированного внутрисосудистого свертывания).
В результате недостатка лейкоцитов и снижения иммунитета развиваются инфекционные осложнения различной степени тяжести, что чаще всего проявляется лихорадкой.
Могут возникать язвенно-некротическая ангина, перитонзиллярные абсцессы, некротический гингивит, стоматит, пиодермия, параректальные абсцессы, пневмония, пиелонефрит. Существует значимый риск тяжелого течения инфекционных осложнений вплоть до развития сепсиса.
С током крови и лимфы опухолевые клетки попадают в здоровые органы, нарушают их структуру и функцию – наиболее подвержены метастатическим процессам печень, селезенка, лимфатические узлы, но метастазы могут поражать и кожу, и мозговые оболочки, и почки, и легкие.
Основные причины летальности у пациентов с лейкозом связаны с тем, что осложнения могут спровоцировать развитие сепсиса, полиорганную недостаточность, кровоизлияния в различные органы. Острый лейкоз без лечения приводит к смертельному исходу в течение нескольких недель или месяцев.
Диагностика лейкозов
Диагностика лейкозов основывается на оценке морфологических особенностей клеток костного мозга и периферической крови. Поэтому всем пациентам с подозрением на лейкоз назначают общий анализ крови с подсчетом лейкоцитарной формулы и определением числа тромбоцитов.
Клинический анализ крови – одно из основных лабораторных исследований для количественной и качественной оценки всех классов форменных элементов крови. Включает цитологическое исследование мазка крови с подсчетом процентного содержания разновидностей лейкоцитов (определение общего количества лейкоцитов и процентного соотношения основных субпопуляций лейкоцитов: нейтрофилов, лимфоцитов, моноцитов, эозинофилов и базофилов) и определение скорости оседания эритроцитов.
Для определения объема опухолевого поражения, вероятности развития синдрома лизиса опухоли рекомендовано выполнение общетерапевтического биохимического анализа крови: АСТ, АЛТ, общий билирубин, глюкоза, мочевина, креатинин, общий белок, ЛДГ, магний, натрий, калий, кальций.
Определение уровня АЛТ в сыворотке крови применяют преимущественно в диагностике и контроле течения болезней печени, а также в комплексных биохимических исследованиях.
Определение уровня АСТ в сыворотке крови используют преимущественно в диагностике и контроле течения болезней печени, а также в комплексных биохимических исследованиях.
Определение уровня билирубина в сыворотке крови используют для выявления поражений печени различного происхождения, закупорки желчных путей, гемолитической анемии, желтухи новорожденных.
Глюкоза – основной источник энергии для метаболических процессов в организме человека, является обязательным компонентом большинства внутриклеточных структур, участвует в синтезе нуклеиновых кислот (рибоза, дезоксирибоза), образует соединения с белками (гликопротеиды, протеогликаны) и липидами (гликолипиды).
Мочевина – конечный продукт расщепления белковых молекул, выводимый из организма почками. Определение уровня мочевины в сыворотке крови используют для оценки выделительной функции почек и контроля эффективности лечения пациентов с почечными заболеваниями.
Креатинин – продукт метаболизма мышечных клеток, удаляется из крови почками. Тест используют в качестве маркера функции почек для диагностики и мониторинга острых и хронических болезней почек, а также в скрининговых обследованиях.
Общий белок выступает показателем белкового обмена, отражающим содержание всех фракций белков в сыворотке крови. Тест используется в комплексных биохимических обследованиях пациентов при различных заболеваниях.
Лактатдегидрогеназа – гликолитический фермент, участвующий в конечных этапах превращений глюкозы. Тест используют в диагностике различных заболеваний (сердца, печени, мышц, почек, легких, системы крови).
Магний – один из основных катионов организма. Исследование магния в сыворотке крови в комплексе с другими электролитами используют для выявления нарушений электролитного баланса.
Определение уровня калия, натрия и хлора в сыворотке крови используется для скрининга электролитов и исследования кислотно-щелочного дисбаланса.
Общий кальций – основной компонент костной ткани и важнейший биогенный элемент, обладающий важными структурными, метаболическими и регуляторными функциями в организме.
Для определения вероятности развития тяжелых коагуляционных нарушений (как геморрагических, так и тромботических) рекомендовано исследование свертывающей системы крови.
Базовый набор тестов, применяемый для скрининговой оценки состояния свертывающей системы крови.
С целью исключения поражения почек выполняют общий анализ мочи.
Общий анализ мочи – комплексная оценка ряда физических и химических параметров мочи, а также элементов мочевого осадка, нацеленное на выявление патологии почек и мочевыводящих путей.
Диагностику хронического лейкоза проводят с помощью иммунофенотипического исследования лимфоцитов крови (ИФТ) методом проточной цитометрии.
Рекомендовано проведение стернальной пункции (пункции грудины) для получения цитологического препарата костного мозга и цитологическое и цитохимическое исследование мазка с целью уточнения диагноза и определения прогноза.
В ряде случаев показана биопсия опухолевого образования или лимфатического узла (или другого метастатического очага) и патологоанатомическое исследование полученного биопсийного материала.
Кроме того, врач может рекомендовать проведение иммунофенотипирования гемопоэтических клеток-предшественниц в костном мозге, цитогенетическое исследование аспирата костного мозга, молекулярно-генетические исследования мутаций в генах и др.
Из инструментальных методов диагностики проводятся:
-
эхокардиография для оценки функционального состояния сердечной мышцы;
Сканирование головного мозга, черепа и окружающих их тканей, позволяющее диагностировать различные патологии.
Исследование, позволяющее получить данные о состоянии органов грудной клетки и средостения.
Сканирование внутренних органов брюшной полости для оценки его функционального состояния и наличия патологии.
Лечение лейкозов
Лечение лейкозов проводится в стационаре. Медикаментозное воздействие на опухоль специальными препаратами, губительно действующими на быстро делящиеся клетки, называется химиотерапией. При лечении острых лейкозов химиотерапию проводят в несколько этапов: индукция ремиссии, консолидация (закрепление) ремиссии, поддерживающая терапия и профилактика нейролейкемии (метастазирования опухолевых лейкозных клеток в головной и спинной мозг).
Период индукции ремиссии – это начальный этап, цель которого максимально уменьшить опухолевую массу и достичь ремиссии. Обычно для этого требуется 1-2 курса химиотерапии. Далее идет консолидация достигнутого эффекта – наиболее агрессивный и высокодозный этап лечения, задачей которого является по возможности еще большее уменьшение числа остающихся после индукции лейкемических клеток. Этот этап также занимает 1-2 курса. За ним следует противорецидивное или поддерживающее лечение. При некоторых вариантах острых лейкозов требуется профилактика или, при необходимости, лечение нейролейкемии.
Для разных видов лейкозов у разных возрастных групп профессиональными сообществами разработаны схемы химиотерапии.
При лечении ХМЛ основными препаратами выбора являются ингибиторы тирозинкиназы, применяемые в непрерывном режиме – ежедневно, длительно, постоянно. Перерывы в приеме могут способствовать снижению эффективности терапии и прогрессированию заболевания. В случае неэффективности терапии может быть проведена трансплантацию гемопоэтических стволовых клеток или костного мозга.
В терапии ХЛЛ цели и схемы терапии химиотерапии определены возрастом пациента, числом и тяжестью сопутствующих заболеваний. Разработаны протоколы лечения для разных пациентов, в том числе схемы моно- и полихимиотерапии. Для профилактики инфекционных осложнений применяют внутривенное введение иммуноглобулина, рекомендована вакцинация от гриппа и пневмококковой инфекции.
Помимо химиотерапии пациенту может потребоваться трансфузионная терапия: переливание эритроцитарной массы, тромбоцитарной массы, изотонических растворов.
При присоединении инфекций показана антибиотикотерапия. На фоне лечения могут возникать тромботические осложнения, что требует антикоагулянтной терапии. Пациентам высокого риска в связи с вероятностью рецидива лейкоза применяют трансплантацию гемопоэтических стволовых клеток.
Осложнения
Основные осложнения лейкозов – инфекционные, вплоть до сепсиса, и тромботические и/или геморрагические осложнения с развитием синдрома диссеминированного внутрисосудистого свертывания. При метастазировании опухолевых клеток развивается полиорганная недостаточность, в т.ч. лейкозные клетки могут попадать в оболочки головного и спинного мозга, инфильтрировать периферические нервы с развитием разнообразных двигательных и чувствительных нарушений (лейкемоидная инфильтрация). Кроме того, встречается так называемый «синдром лизиса опухоли» – сложный процесс, возникающий в результате спонтанного или вызванного лечением разрушения большого числа опухолевых клеток с выходом внутриклеточного содержимого в кровоток. При этом может развиться острая почечная недостаточность. Летальность при лизисе опухоли достигает 70%.
Профилактика лейкозов
Так как причины возникновения лейкозов не установлены, методов специфической профилактики до сих пор не существует.
Однако доказано, что между курением и риском развития острого лейкоза существует дозовая зависимость, которая особенно очевидна для лиц старше 60 лет.
Ряд исследователей предполагают, что около 20% случаев ОМЛ являются следствием курения.
- Клинические рекомендации «Острые миелоидные лейкозы». Общероссийский национальный союз «Ассоциация онкологов России», некоммерческое партнерство содействия развитию гематологии и трансплантологии костного мозга «Национальное гематологическое общество», 2020.
- Клинические рекомендации «Острые лимфобластные лейкозы». Общероссийский национальный союз «Ассоциация онкологов России», некоммерческое партнерство содействия развитию гематологии и трансплантологии костного мозга «Национальное гематологическое общество», 2020.
- Клинические рекомендации «Хронический лимфоцитарный лейкоз/ лимфома из малых лимфоцитов». Общероссийский национальный союз «Ассоциация онкологов России», некоммерческое партнерство содействия развитию гематологии и трансплантологии костного мозга «Национальное гематологическое общество», региональная общественная организация «Общество онкогематологов», 2020.
- Клинические рекомендации «Хронический миелолейкоз у взрослых». Национальное гематологическое общество, 2017.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Острый лимфобластный лейкоз
Острый лимфобластный лейкоз представляет собой онкологическое заболевание костного мозга, которое всем нам знакомо под другим названием – рак крови. Оно характеризуется нарушением нормального кроветворения и в большинстве случаев встречается у детей. Пик заболеваемости приходится на возрастной период от 1 до 5 лет с постепенным уменьшением количества заболевших в возрасте от 7 лет и старше. Менее заметный рост числа детей с этим диагнозом приходится на возраст от 10 до 14 лет. Острым лимфобластным лейкозом болеют чаще всего мальчики, чем девочки. Эта закономерность наиболее ярко отслеживается в младенческом возрасте. В возрасте 10 – 13 лет заболеваемость острым лимфобластным лейкозом лейкоза среди представителей разных полов имеет одинаковый уровень. Почему возникает острый лимфобластный лейкоз? Можно ли распознать признаки этого вида онкологии? Как осуществляется лечение острого лимфобластного лейкоза, и есть ли шанс выздороветь у пациента с этим страшным диагнозом?
Острый лимфобластный лейкоз: понятие и описание болезни
Острый лимфобластный лейкоз – раковое заболевание белых кровяных телец, защищающих человеческий организм от инфекций. Оно характеризуется накоплением патологически измененных клеток в спинном и головном мозге. Белые кровяные тельца не могут обеспечить организму прежнюю защиту, поэтому это заболевание сопровождается повышением температуры тела на фоне протекания различных инфекционных болезней.
Для острого лимфобластного лейкоза характерно распространение раковых клеток по всему организму. Первоначально лейкозы находятся в костном мозге, а затем по кровяным потокам перемещаются в лимфатическую систему и другие органы. Результатом острого лимфобластного лейкоза становится патологии всей системы органов, поэтому он относится к системным злокачественным заболеваниям. Быстрое прогрессирование онкологического процесса требует незамедлительного лечения. В противном случае есть вероятность наступления летального исхода всего после нескольких месяцев болезни.
Рассмотрим факторы, влияющие на прогноз – предвидение вероятного исхода и развития острого лимфобластного лейкоза:
- Возраст больного на момент диагностики лейкоза. Чем моложе вы, тем более сильное сопротивление оказывает ваш организм злокачественной болезни, а, значит, у вас есть больше шансов для выздоровления;
- Число хромосом. Большая вероятность излечения характерна для людей с повышенным количеством хромосом в лейкозных клетках;
- Исходное количество лейкоцитов. Пациенты с высоким количеством лейкоцитов при первичной диагностике нуждаются в более интенсивной терапии острого лимфобластного лейкоза, в отличие от больных с более низким их количеством;
- Пол пациента. По необъяснимым причинам у девочек с острым лимфобластным лейкозом вероятность выздоровления значительно выше, чем у мальчиков;
- Ответ на лечение. Пациенты, достигшие признаков ремиссии после непродолжительного курсового лечения химиотерапией, имеют больше шансов на выздоровление.
2. Причины болезни
К сожалению, нельзя точно назвать условия, способствующие развитию онкологических заболеваний, а, следовательно, предотвратить их появление. Выделяют несколько факторов риска, увеличивающих вероятность заболевания лимфобластным лейкозом:
- радиационное воздействие;
- влияние некоторых химических средств;
- синдром Дауна;
- мужской пол.
3. Симптомы острого лимфобластного лейкоза
Лейкемические клетки, подобно здоровым клеткам крови, свободно циркулируют по всему организму. Признаки онкологического заболевания зависят от числа патологических клеток и мест их скопления. У детей, страдающих острым лимфобластным лейкозом, как правило, наблюдается снижение количества здоровых тромбоцитов и красных кровяных телец. Результатом этого процесса становится нарушение транспортировки кислорода к тканям тела и последующее возникновение анемии.
К наиболее распространенным симптомам лимфобластного лейкоза можно отнести такие проявления, как:
- повышение температуры тела;
- усталость;
- болезненность и отечность лимфатических узлов, селезенки и печени;
- потеря аппетита и снижение веса;
- частые инфекционные заболевания;
- кровоподтеки и кровотечения;
- затрудненное дыхание;
- головная боль;
- бледность кожи;
- боли в суставах и костях.
Большинство признаков острого лимфобластного лейкоза являются следствием недостатка здоровых клеток, так как их «лейкемические клоны» распространяются по всему организму. Поэтому симптомы лейкоза зависят в первую очередь от того, в каком месте произошло скопление патологических клеток.
4. Лечение заболевания
Лечение острого лимфобластного лейкоза зависит от множества факторов: вашего возраста, течения заболевания и других нюансов. В большинстве случаев врач использует несколько разнообразных методик лечения, наблюдая за состоянием пациента. К ним относятся:
Химиотерапия. Она представляет собой медикаментозный способ лечения, суть которого заключается в блокировке роста патологических клеток. Чаще всего одного вида препарата недостаточно для того, чтобы уничтожить все лейкозные клетки, поэтому применяются комбинации из следующих лекарственных средств:
- Винкристин;
- Цитарабин;
- Даунорубицин;
- Этопозид;
- L-Аспарагиназа;
- Тенипозид;
- Метотрексат.
Лучевая терапия. Лучевая терапия основана на применении высокоэнергетического излучения, убивающего раковые клетки. Главная цель такого метода лечения лейкоза заключается в удалении злокачественных клеток с минимальным повреждением окружающих их тканей.
Таргетная терапия. В ее основе лежат принципы целевого воздействия на фундаментальные молекулярные механизмы, которые вызывают то или иное заболевание. В отличие от классических методик лечения онкологии, таргетная терапия способствует уничтожению только раковых клеток, не оказывая неблагоприятного влияния на здоровые ткани организма.
Пересадка костного мозга. Трансплантация стволовых клеток, как правило, осуществляется, когда все другие методы лечения острого лимфобластного лейкоза не были эффективными.
Лечение острого лимфобластного лейкоза состоит из двух этапов. Первый этап – это ремиссионо-индукционная терапия, главная цель которой заключается в уничтожении лейкозных клеток в костном мозгу и крови. Второй этап – постремиссионная терапия. Этот заключительный этап терапии начинается сразу после того, как все лейкозные клетки будут удалены.
Заболевания 
Первичное обследование 
- Анализы крови на онкомаркеры
- МРТ головы, позвоночника, органов малого таза, органов брюшной полости
- МСКТ органов грудной клетки
- МСКТ органов брюшной полости (виртуальная колоноскопия)
- Гастроскопия (возможность проведения под наркозом, биопсия)
- Колоноскопия (возможность проведения под наркозом, биопсия)
- Бронхоскопия (с биопсией)
- Сцинтиграфия (костей скелета, легких)
Если вы обнаружили у себя подобные симптомы, возможно, это сигнал заболевания, поэтому рекомендуем проконсультироваться с нашим специалистом.
Диагностика 
- Анализы крови на онкомаркеры
- МРТ головы, позвоночника, органов малого таза, органов брюшной полости
- МСКТ органов грудной клетки
- МСКТ органов брюшной полости (виртуальная колоноскопия)
- Гастроскопия (возможность проведения под наркозом, биопсия)
- Колоноскопия (возможность проведения под наркозом, биопсия)
- Бронхоскопия (с биопсией)
- Сцинтиграфия (костей скелета, легких)
Наши цены 
- Консультация врача онколога, профессор – 10000 р.
- Онкомаркеры:
- ПСА (простатический специфический антиген) общий – 575 р.
- ПСА общий/ПСА своб.(отношение) – 1040 р.
- РЭА (раковый эмбриональный антиген) – 730 р.
- СА 15-3 – 780 р.
- СА 19-9 – 770 р.
- СА 125 – 740 р.
- UBC (антиген рака мочевого пузыря) – 1775 р.
- СА 72-4 – 1170 р.
- Cyfra 21-1 – 1220 р.
- NSE (нейрон-специфическая енолаза) – 1550 р.
- SCC (антиген плоскоклеточной карциномы) – 1550 р.
- НЕ 4 (секреторный белок эпидидимиса 4) – 1150 р.
- СА 242 – 900 р.
- Белок S 100 – 2475 р.
- CgA (хромогранин А) – 2490 р.
- МРТ (головы, позвоночника, органов малого таза. органов брюшной полости) один отдел на базе ЛПУ-партнера – от 6000 р.
- МСКТ органов грудной клетки на базе ЛПУ-партнера – от 6000 р.
- Гастроскопия (ЭГДС, эзофаго-гастро-дуоденоскопия) на базе ЛПУ-партнера без наркоза/с наркозом (во сне) – от 6000/10000 р.
- Колоноскопия на базе ЛПУ-партнера без наркоза/с наркозом (во сне) – от 12000/20000 р.
- ПЭТ-КТ на базе ЛПУ-партнера – от 35000 р.
- Сцинтиграфия костей скелета на базе ЛПУ-партнера – от 8000 р.
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Острый лимфобластный лейкоз
Лейкоз, или лейкемия – заболевание кроветворной системы, в обиходе иногда называемое «раком крови». При лейкозе в костном мозге производится избыточное количество аномальных незрелых клеток крови, обычно предшественников лейкоцитов. Эти бластные клетки, размножаясь и накапливаясь в костном мозге, мешают выработке и функционированию нормальных клеток крови, что и обусловливает основные симптомы заболевания. Кроме того, эти опухолевые клетки могут накапливаться в лимфоузлах, печени, селезенке, центральной нервной системе и других органах, также вызывая появление специфических симптомов.
Как известно, различные клетки крови развиваются по-разному и имеют разных предшественников – то есть относятся к различным линиям кроветворения (см. схему в статье «Кроветворение»). Линия кроветворения, приводящая к появлению лимфоцитов, называется лимфоидной; остальные же лейкоциты относятся к миелоидной линии. Соответственно, различают лейкозы из клеток-предшественников лимфоцитов (такие лейкозы называют лимфобластными, лимфоцитарными или просто лимфолейкозами) и из предшественников других лейкоцитов (миелобластные, миелоидные, миелолейкозы).
Острый лимфобластный лейкоз (ОЛЛ) – самый распространенный вид лейкоза у детей, но это заболевание встречается и во взрослом возрасте. Термин «острый» означает быстрое развитие болезни, в противоположность хроническому лейкозу. Термин «лимфобластный» означает, что незрелые клетки, составляющие основу болезни, являются лимфобластами, то есть предшественниками лимфоцитов.
Частота встречаемости и факторы риска
На долю ОЛЛ приходится 75-80% всех опухолевых заболеваний кроветворной системы у детей и примерно 25% всех детских онкозаболеваний вообще (примерно 4 случая на 100 тысяч детей в год). Именно ОЛЛ – самое распространенное онкологическое заболевание у детей. Чаще всего ОЛЛ возникает в возрасте до 14 лет; пик детской заболеваемости приходится на возраст 2-5 лет. У мальчиков эта болезнь встречается немного чаще, чем у девочек.
Вероятность возникновения ОЛЛ несколько повышена у людей, ранее получавших лечение от какой-либо другой болезни (обычно злокачественной опухоли) с использованием облучения или определенных видов цитостатической химиотерапии. Также риск ОЛЛ повышен у детей с некоторыми генетическими нарушениями – например, с синдромом Дауна, нейрофиброматозом типа I или рядом первичных иммунодефицитных состояний.
Риск заболеть для ребенка выше среднего, если у его брата- или сестры-близнеца уже был диагностирован лейкоз. Другие случаи, когда в одной и той же семье ОЛЛ возникает более чем у одного ребенка, бывают, но исключительно редки.
Впрочем, в большинстве случаев ОЛЛ не удается обнаружить никакого известного фактора риска, и причины, вызвавшие болезнь, остаются неизвестными.
Признаки и симптомы
ОЛЛ характеризуется множеством различных признаков и у разных больных может проявляться совершенно по-разному. Большинство наблюдаемых симптомов, однако, обусловлено тяжелыми нарушениями кроветворения: избыток аномальных бластных клеток при ОЛЛ сочетается с недостаточным количеством нормальных функциональных клеток крови.
Обычно наблюдаются слабость, бледность, снижение аппетита, потеря веса, учащенное сердцебиение (тахикардия) – проявления анемии и опухолевой интоксикации. Недостаток тромбоцитов проявляется мелкими кровоизлияниями на коже и слизистых оболочках, кровотечениями из десен, носовыми и кишечными кровотечениями, кровоподтеками, синяками. Из-за накопления бластных клеток часто увеличиваются лимфоузлы – в частности, шейные, подмышечные, паховые. Нередко увеличиваются также печень и селезенка – как говорят, возникает гепатоспленомегалия.
Часто наблюдаются боли в костях и суставах, иногда возникают патологические (то есть вызванные заболеванием) переломы костей. Из-за недостаточного количества нормальных зрелых лейкоцитов возможны частые инфекции. Повышение температуры может наблюдаться как в связи с возникшей на фоне лейкоза инфекцией, так и из-за опухолевой интоксикации. Иногда одним из проявлений острого лейкоза является продолжительная ангина, плохо поддающаяся терапии антибиотиками.
В некоторых случаях ОЛЛ вызывает изменения и в других органах: глазах, почках, яичках у мальчиков и яичниках у девочек, причем у мальчиков поражение половых органов наблюдается чаще. Может возникнуть поражение центральной нервной системы – нейролейкемия.
Так как все наблюдаемые симптомы могут быть связаны и с другими заболеваниями и не специфичны для ОЛЛ, перед началом лечения необходима лабораторная диагностика, которая в срочном порядке производится в больничных условиях.
Диагностика
При ОЛЛ возникают изменения в обычном клиническом анализе крови: как правило, понижены уровни эритроцитов и тромбоцитов, появляются бластные клетки. Очень высокий лейкоцитоз (гиперлейкоцитоз) возможен, но, вопреки распространенному мнению, наблюдается далеко не во всегда. В целом же надежно поставить диагноз можно только при исследовании образца костного мозга; для этой цели необходима костномозговая пункция.
При морфологическом исследовании диагноз «острый лимфобластный лейкоз» ставится при обнаружении более 25% бластных клеток в костном мозге (в противном случае речь может идти о лимфобластной лимфоме). Но обязательно производятся более тонкие исследования: цитохимическое (окрашивание клеток, позволяющее более точно установить их природу), цитогенетическое (изучение строения хромосом в лейкемических клетках), иммунофенотипирование (изучение белковых молекул-маркеров, находящихся на поверхности клеток). Дело в том, что при диагностике очень важно не только надежно отличить ОЛЛ от острого миелоидного лейкоза, но и определить конкретный вариант ОЛЛ, поскольку он сильно влияет на терапию и прогноз заболевания.
Так, ОЛЛ может быть B-клеточным (около 80% случаев) и T-клеточным, в зависимости от того, относятся ли лейкемические клетки к B- или T-лимфоцитарной линии. В зависимости от «степени зрелости» бластных клеток выделяют несколько вариантов среди как В-, так и Т-клеточных лейкозов; их установление методом иммунофенотипирования важно для определения стратегии лечения. Существенны для назначения терапии цитогенетические особенности опухолевых клеток (см. ниже).
В ходе диагностики ОЛЛ также необходимо исследовать состояние центральной нервной системы. Анализ спинномозговой жидкости (ликвора) позволяет определить, нет ли у больного поражения центральной нервной системы – нейролейкемии. Образец ликвора для анализа получают посредством пункции спинномозгового канала.
Возможны и дополнительные диагностические процедуры для исследования пораженных лимфоузлов и внутренних органов – компьютерная томография (КТ), ультразвуковое исследование (УЗИ) и так далее.
Диагностические исследования позволяют для каждого конкретного больного определить ту или иную группу риска, от которой зависят прогноз заболевания и планируемое лечение. Так, говорят о стандартном, промежуточном, высоком риске и т. д. Отнесение к той или иной группе в рамках конкретного протокола лечения зависит от многих факторов. Перечислим некоторые из них.
Возраст больного: менее благоприятным считается возраст до 1 года или старше 10 лет.
Количество лейкоцитов: риск увеличивается при очень высоком лейкоцитозе в момент постановки диагноза.
Распространение ОЛЛ в другие органы, помимо костного мозга (например, возникновение нейролейкемии), определяет более высокий риск.
При раннем или повторном рецидиве риск повышается.
Кроме того, выбор стратегии лечения зависит от варианта лейкоза (В- или Т-клеточный ОЛЛ), а также от цитогенетических аномалий в лейкемических клетках, связанных с числом хромосом и транслокациями. Некоторые из них достоверно влияют на течение болезни и ход терапии, другие только изучаются. Так, филадельфийская хромосома – транслокация t(9;22) – требует подключения к терапии дополнительных таргетных лекарств. Транслокация t(4;11) часто требует трансплантации костного мозга. В то же время, например, транслокация t(12;21) обычно связана с относительно хорошим прогнозом.
Лечение
Как упомянуто в предыдущем разделе, современное лечение ОЛЛ основано на разделении пациентов на группы риска – в зависимости от того, насколько вероятно у них достижение и сохранение ремиссии при одинаковой терапии. Соответственно, пациенты, относящиеся к группам более высокого риска (то есть те, у кого изначальный прогноз хуже), получают более интенсивную терапию, а в группах более низкого риска можно использовать менее интенсивную терапию и тем самым избегать излишней токсичности и тяжелых осложнений.
Терапия ОЛЛ, как правило, состоит из трех этапов:
Индукция ремиссии (то есть терапия, направленная на достижение ремиссии) проводится в течение нескольких первых недель лечения. Под ремиссией здесь подразумеваеся содержание менее 5% бластных клеток в костном мозге и отсутствие их в обычной (периферической) крови в сочетании с признаками восстановления нормального кроветворения.
В ходе индукции проводится интенсивная многокомпонентная химиотерапия лекарствами-цитостатиками, которые вызывают разрушение лейкемических клеток. На этом этапе могут применяться, в зависимости от протокола, такие лекарства, как гормоны-глюкокортикостероиды, аспарагиназа и пэгаспаргаза, винкристин, даунорубицин, другие препараты. Индукция позволяет достигнуть ремиссии более чем у 95% детей и у 75-90% взрослых с ОЛЛ. Принципиально важно посредством лабораторных анализов оценить ответ на терапию индукции: в случае плохого ответа (к контрольному сроку не удалось достичь нужных результатов) пациент переводится в группу более высокого риска.
Консолидация (закрепление) ремиссии направлена на уничтожение остаточных аномальных бластных клеток во избежание рецидива заболевания. Общая продолжительность этого этапа измеряется месяцами и сильно зависит от конкретного протокола лечения. В ходе курсов терапии на этапе консолидации могут использоваться, опять-таки в зависимости от конкретного протокола, метотрексат, аспарагиназа, 6-меркаптопурин, винкристин, глюкокортикостероиды, даунорубицин и ряд других лекарств в зависимости от протокола и терапевтической группы.
На этапах индукции и консолидации введение химиотерапевтических препаратов производится в основном внутривенно, в условиях больничного стационара или стационара одного дня.
Поддерживающая терапия проводится для поддержания ремиссии, то есть для дополнительного снижения риска рецидива после этапов индукции и консолидации. Продолжительность поддерживающей терапии – полтора-два года. На этом этапе основными препаратами являются 6-меркаптопурин и метотрексат.
Поддерживающая терапия представляет собой этап наименее интенсивного лечения. Ребенок живет дома, постоянное пребывание или ежедневные визиты в больницу не требуется.
Существует также понятие реиндукции: это периодически повторяемые уже после достижения ремиссии циклы интенсивной полихимиотерапии. Реиндукция позволяет дополнительно снизить число лейкемических клеток и тем самым повысить «надежность» ремиссии.
Если требуется лечение или профилактика нейролейкемии на перечисленных этапах, химиопрепараты вводятся интратекально, то есть в спинномозговой канал посредством люмбальных пункций. Иногда лекарства вводят в желудочки (особые полости) головного мозга через специальный резервуар Оммайя, который устанавливается под кожей головы. Для интратекального введения при ОЛЛ используются метотрексат, цитарабин и гормоны-глюкокортикостероиды. У некоторых пациентов применяется и облучение головы – краниальное облучение.
К сожалению, несмотря на все перечисленные меры, иногда возникает рецидив ОЛЛ – костномозговой, экстрамедуллярный (то есть вне костного мозга – например, с поражением центральной нервной системы или яичек) или комбинированный. В этом случае проводится противорецидивная терапия. Выбор метода лечения рецидива зависит от сроков его возникновения (ранний или поздний) и от того, является ли рецидив костномозговым или экстрамедуллярным. При раннем рецидиве шансы на успех одной только лекарственной терапии значительно снижаются и практически всегда планируется трансплантация.
В ходе лечения ОЛЛ может применяться трансплантация костного мозга от родственного или неродственного донора. Если по плану лечения предусмотрена трансплантация, то ее проводят после достижения ремиссии. Как правило, трансплантация показана только при высоком риске (например, после раннего рецидива или при плохом ответе на терапию индукции), поскольку это очень тяжелое лечение, а хорошие результаты стандартной терапии при ОЛЛ в среднем вероятны, особенно у детей.
Химиотерапия ОЛЛ высокоэффективна, но зачастую тяжело переносится и может быть связана с серьезными побочными эффектами. Так, в процессе лечения подавляется кроветворение и бывают необходимы переливания компонентов донорской крови – тромбоцитов во избежание кровотечений при очень низком уровне собственных тромбоцитов больного, эритроцитов для борьбы с анемией. Переливания донорских гранулоцитов применяются только в редких случаях при тяжелых инфекционных осложнениях.
В числе «обычных» побочных эффектов химиотерапии можно также назвать тошноту, рвоту, облысение. Серьезнае проблема связана с возможностью аллергических реакций на химиопрепараты, вплоть до анафилактического шока – жизнеугрожающего состояния, которое характеризуется отеком, затруднением дыхания, сильным зудом и т.д. Так, сравнительно часто встречается аллергия на аспарагиназу, и может быть необходимо использование аналогов этого препарата («Онкаспар», «Эрвиназа»).
Поскольку и лейкоз сам по себе, и используемая при его лечении химиотерапия резко снижают сопротивляемость организма различным инфекциям, больным во время лечения необходимы эффективные антибактериальные и противогрибковые лекарства для профилактики и терапии инфекционных осложнений. Опасны как обычные, так и оппортунистические инфекции.
Интенсивное лечение ОЛЛ накладывает серьезные ограничения на образ жизни больного. Необходимо соблюдать определенную диету и строгие гигиенические требования. Во избежание инфекций ограничиваются контакты с внешним миром. При очень низком уровне тромбоцитов нельзя не только допускать травмы, но даже, например, чистить зубы зубной щеткой, чтобы не спровоцировать кровотечение из десен. После достижения ремиссии строгость этих ограничений постепенно снижается. Врачи и медсестры сообщают каждому больному, что ему можно и что нельзя на текущем этапе лечения.
В последние годы появилось несколько новых возможностей лечения даже самых сложных случаев ОЛЛ. Особо следует отметить иммунопрепараты «Блинцито» (блинатумомаб) и «Биспонса» (инотузумаб озогамицин), а также CAR T-клеточную терапию, применяемые при В-клеточном ОЛЛ. Есть и специальные препараты для Т-клеточного ОЛЛ, такие как «Атрианс» (неларабин). Иногда применяется также «Эвольтра» (клофарабин). Некоторым больным помогает включение в терапию препарата «Велкейд» или «Бартизар» (бортезомиб). Есть и другие варианты.
Прогноз
Без лечения ОЛЛ приводит к гибели больного в течение нескольких месяцев. Однако использование современных протоколов лечения дает при ОЛЛ очень хороший результат: можно вылечить 85-90% больных детей. У взрослых, особенно пожилых, результаты хуже, но, тем не менее, примерно у 40% взрослых больных удается достичь долговременной ремиссии – то есть отсутствия рецидивов болезни в течение многих лет.





