Синдром Дресслера
Синдром, обусловленный аутосенсибилизацией к продуктам распада сердечной ткани и излившейся крови в перикард.
Развивается у 3-6% больных, чаще у больных, перенесших крупноочаговый инфаркт миокарда, осложнившийся эпистенокардитическим перикардитом.
Клиническая симптоматика возникает через 2-6 недель после начала инфаркта миокарда. Проявляется перикардитом, плевритом, пневмонитом. Реже встречаются миозит грудной мышцы, артрит плечевого сустава.
Длительность проявлений – от 3-4 дней до 4 недель.
При перикардите отмечается длительный болевой синдром, четко не связанный с нагрузками. Боль усиливается при глубоком вдохе, поворотах туловища. Значительного накопления жидкости в перикарде обычно нет. Выслушивается отчетливый шум трения перикарда, более выраженный слева от грудины в 3-5 межреберьях.
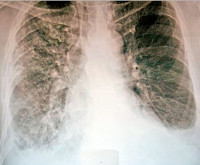
При пневмоните во время аускультации отмечают влажные хрипы, при рентгенологическом обследовании – различной выраженности затемнения. Пневмонит может сочетаться с накоплением жидкости в плевральной полости.
Миозиты грудной мышцы сопровождаются болями, определяющимися пальпаторно и усиливающимися при движении плечевого пояса.
На ЭКГ формируются подъемы сегмента ST в нескольких отведениях, увеличение отрицательной фазы T. Могут возникнуть трудности дифференциальной диагностики с рецидивом или повторным инфарктом миокарда. Для дифференциальной диагностики важны клинические данные и результаты лабораторного обследования.
Обычно выявляют лейкоцитоз, эозинофилию, повышение СОЭ, СРП, фибрина, сиаловых кислот, гамма-глобулинов.
Течение заболевания острое, затяжное или рецидивирующее. Обострения не зависят от характера течения и проявлений ИБС. По вариантам синдром Дресслера разделяют на типичный, атипичный и малосимптомный. Изредка синдром Дресслера протекает с проявлениями геморрагического васкулита (А.Я.Арипов и соавт., 1978), бронхиальной астмы, поражений почек, аутоиммунного гепатита (А.В.Сумароков, З.Г.Апросина, 1972), проктита, желудочно-кишечного кровотечения (А.Д.Хетагуров и др., 1987), перикардита с тампонадой сердца (А.И.Кирсанов и соавт., 1990).
Лечебные мероприятия заключаются в приеме преднизолона в дозе 15-20 мг в сутки. Меньшее значение имеют противовоспалительные и десенсибилизирующие средства.
Тромбоэндокардит
Поражение эндокарда при инфаркте миокарда приводит к образованию пристеночных тромбов.
Клиническими проявлениями этого осложнения являются длительный субфебрилитет, потливость, слабость, тахикардия, признаки сердечной недостаточности, лейкоцитоз, ускорение СОЭ. Характерны тромбоэмболии большого круга кровообращения.
Диагностика основывается на отчетливой клинической симптоматике и обнаружении пристеночных тромбов при эхокардиографическом обследовании. Могут проводиться исследования с радиоактивным фибриногеном, который откладывается в тромбах.
Лечебные мероприятия заключаются в назначении антикоагулянтов и дезагрегантов.
Тромбоэмболические осложнения
В настоящее время при использовании тромболитических препаратов и дезагрегантов тромбоэмболические осложнения встречаются у 2-6 % больных с инфарктом миокарда.
В механизмах их возникновения большое значение имеют повышение свертывающей активности крови, развитие ДВС синдрома; изменения сосудистой стенки в связи с атеросклерозом; застой крови, обусловленный шоком и сердечной недостаточностью; нарушение сердечной гемодинамики в связи с образованием аневризмы, дилатации миокарда, мерцательной аритмии; тромбоэндокардит; обострение тромбофлебитов малого таза, голеней. В развитии этих осложнений большое значение имеет длительная обездвиженность больного.
Наиболее часто отмечается тромбоэмболия легочной артерии. Диагностика ее сложна. Связано это с малой специфичностью симптоматики, трудностью отличия ее от проявлений инфаркта миокарда. У больных с ТЭЛА отмечается динамика ЭКГ, напоминающая задний инфаркт миокарда: Q III (SI-Q III), отрицательный T в III, aVF, V1-V4, высокий Р во II, III отведениях. Отличием являются: высокий R в III отведении, повышение «легочной» фракции ЛДГ3. Диагноз подтверждается динамикой рентгенологических изменений в легких.
Тромбоэмболии конечностей приводят к внезапной сильной боли, похолоданию ее, исчезновению пульса, появлению парестезии, исчезновению чувствительности, парезам.
Тромбоэмболия почечных артерий характеризуется различной выраженностью болей в области поясницы, слабостью, тошнотой, рвотой, повышением артериального давления, появлением эритроцитов в моче. Может быть олигурия, симптомы почечной недостаточности.
Тромбоэмболия мезентериальных артерий проявляется сильной, неопределенной болью в животе. Затем развивается парез кишечника и клиника динамической непроходимости. Может быть дегтеобразный стул. Часто развивается шок.
Тромбоэмболия мозговых сосудов. Клиническая картина характеризуется внезапной головной болью, развитием очаговой симптоматики. Могут быть различной выраженности общемозговые симптомы.
При всех тромбоэмболических осложнениях может возникать острая левожелудочковая недостаточность.
Синдром Дресслера (постинфарктный синдром)
Опасность инфаркта миокарда состоит не только в том, что он приводит к нарушению функционирования сердечно-сосудистой системы. После этого заболевания развиваются различные осложнения, которые способны намного ухудшить качество жизни. Одно из таких осложнений – синдром Дресслера, или постинфарктный синдром.
Каждому пациенту, обратившемуся к нам, мы готовы предложить плановую и экстренную помощь при сердечно-сосудистых заболеваниях. Для лечения пациентов с синдромом Дресслера врачи-кардиологи ОН КЛИНИК применяют самые современные и действенные методы, одобренные в лучших клиниках Европы и Израиля.
Поскольку все большее количество пациентов страдает сердечно-сосудистыми заболеваниями и нуждается в помощи высококвалифицированных специалистов, кардиология является одним из самых востребованных и стремительно развивающихся направлений в нашей клинике. Мы стремимся идти в ногу со временем и предлагаем пациентам лучшее из имеющегося в мировой медицине. Если Вас беспокоит сердце – не ждите осложнений, звоните и записывайтесь к нам на прием!
Что такое синдром дресслера?
Впервые это заболевание было описано немецким ученым Вильямом Дресслером в средине XX века и названо его именем. Постинфарктный синдром является аутоиммунной патологией, которая дает о себе знать такими заболеваниями, как перикардит, плеврит, пневмонит, воспалительные заболевания суставов. Атипичная форма синдрома Дресслера может привести к появлению проблем в функционировании легких, почек и желудочно-кишечного тракта.
По течению и периоду развития синдром Дресслера разделяют на ранний, который возникает сразу же после инфаркта миокарда, и поздний, развивающийся через несколько недель и даже месяцев. Согласно статистике, постинфарктный синдром развивается примерно у 4% пациентов, перенесших инфаркт миокарда. Однако, по мнению врачей, с этим осложнением сталкивается намного больше пациентов, так как синдром Дресслера может протекать малосимптомно и атипично, что затрудняет диагностику.
Симптомы синдрома дресслера
Среди самых распространенных симптомов постинфарктного синдрома:
- сжимающие или острые боли в груди;
- иррадиация болей в плечи, руки, ощущение онемения кожи;
- сильная одышка, сухой кашель с прожилками крови;
- ощущение давления в грудной клетке;
- повышенная температура тела, сильная потливость;
- кожная сыпь;
- боли в суставах;
- общее недомогание и плохое самочувствие.
Наличие любого из этих симптомов должно послужить поводом для немедленного обращения к врачу. Если Вы или Ваш близкий человек недавно пережили инфаркт и имеются жалобы на дискомфорт в области сердца – не медлите, записывайтесь на прием к кардиологу! В экстренных случаях у нас в медцентре врачи готовы принять пациента без записи.
ОН КЛИНИК – это современная диагностика и эффективное лечение кардиологических заболеваний. Обращайтесь, преодолеем болезнь вместе!

Соколова С.В., терапевт. Кардиология в ОН КЛИНИК: как снизить риск наступления инфаркта.
Диагностика и лечение синдрома дресслера в ОН КЛИНИК
В Международном медицинском центре ОН КЛИНИК работают лучшие кардиологи, которые постоянно повышают квалификацию в нашей стране и за рубежом. В нашей клинике применяются только оригинальные препараты и оборудование наиболее известных мировых производителей, качество которых подтверждено сертификатами соответствия.
Особое внимание у нас в клинике уделяют диагностике, ведь если заболевание протекает бессимптомно или с неявными симптомами, как это случается с синдромом Дресслера, обнаружить его можно только при помощи тщательного обследования и применения высокоточных современных аппаратов.
Диагностика при подозрении на синдром Дресслера включает в себя анализ анамнеза заболевания, жалоб пациента, физикальный осмотр врача и следующие виды исследований:
- электрокардиограмма;
- эхокардиография;
- рентгенография грудной полости;
- магнитно-резонансная томография;
- компьютерная томография;
- общие анализы мочи и крови, биохимический анализ крови.
Лечение постинфарктного синдрома медикаментозное и заключается в приеме кардиотропных, гиполипидемических и нестероидных противовоспалительных препаратов. Также могут потребоваться глюкокортикостероиды, бета-блокаторы, антикоагулянты и анальгетики для снятия выраженного болевого синдрома. Иногда требуется госпитализация. Все препараты пациенту должен подбирать врач-кардиолог, самолечение недопустимо и может привести к непоправимым последствиям!
Если у Вас или Ваших близких синдром Дресслера, подозрение на это заболевание или общее плохое самочувствие и постинфарктные перебои в работе сердца – приезжайте в ОН КЛИНИК, где Вашим здоровьем займутся профессионалы в области кардиологии.
Постинфарктный синдром
Постинфарктный синдром – это перикардит аутоиммунного генеза, развивающийся спустя несколько недель после острого инфаркта миокарда. Данное осложнение характеризуется классической триадой симптомов: боль в груди, шум трения листков перикарда, легочные проявления (хрипы, кашель, одышка). Для верификации диагноза выполняется общеклинический анализ крови, ЭКГ, рентген грудной клетки, УЗИ перикарда и плевральной полости. Лечение включает в себя симптоматическую, противовоспалительную и кардиотропную терапию. При осложненном течении проводится плевроцентез, перикардиоцентез или перикардэктомия.
Общие сведения
В клинической терминологии постинфарктным синдромом (ПС), или синдромом Дресслера, называется аутоиммунное поражение околосердечной сумки. Это осложнение, обусловленное неадекватной реакцией иммунной системы на деструктивно измененные белки миокарда, в 1955 году описал американский кардиолог В. Дресслер. В его честь болезнь получила свое второе название. Кроме того, в медицинской литературе встречаются такие термины, как поздний перикардит, посткардиотомический, посттравматический перикардиальный синдром и постинфарктный полисерозит. В целом распространенность ПС в популяции составляет 3-4%. Однако по данным различных авторитетных источников, с учетом атипичных и малосимптомных форм осложнение развивается у 15-30% пациентов, перенесших обширный, осложненный или повторный инфаркт миокарда (ИМ).

Причины постинфарктного синдрома
Первопричиной заболевания является ишемическое повреждение структурных волокон миокарда, повлекшее за собой гибель кардиомиоцитов. Чаще всего оно возникает при крупноочаговом осложненном инфаркте. В процессе разрушения некротизированных тканей в кровоток поступают денатурированные белки, на которые иммунная система реагирует, как на чужеродные. В результате развивается аутоиммунная реакция, являющаяся причиной возникновения постинфарктного синдрома.
Определенную значимость в формировании симптомокомплекса играют антигены крови, проникающей в околосердечную оболочку при нарушении целостности сердечной мышцы. Поэтому, помимо острого ИМ, пусковым механизмом развития заболевания может стать гемоперикард (кровоизлияние в перикардиальную полость), обусловленное травмами грудной клетки, ранениями сердца или неадекватными кардиохирургическими вмешательствами. Также в группу риска входят постинфарктные пациенты с аутоиммунными патологиями. Некоторые авторы считают, что причиной воспалительного процесса является вирусная инфекция. Однако единодушия по поводу данного вопроса у специалистов в области кардиологии до сих пор нет.
Патогенез
Постинфарктный синдром представляет собой аутоиммунный процесс, возникающий вследствие интенсификации выработки антител к кардиальным антигенам. Острое нарушение кровоснабжения миокарда и гибель клеток влечет за собой резорбцию участков некроза и выход денатурированных компонентов в кровь. Это приводит к формированию иммунного ответа с образованием аутоантител, направленных против белков, входящих в состав серозных оболочек органов-мишеней.
Специфические антитела к кардиомиоцитам, в большом количестве присутствующие в плазме крови постинфарктных больных, формируют иммунные комплексы с клетками собственных тканей. Свободно циркулируя в кровяном русле, они накапливаются в перикардиальной, висцеральной плевре и во внутренних слоях суставных сумок, провоцируя асептическое воспаление. В дополнение повышается уровень Т-ЦТЛ (цитотоксических лимфоцитов), разрушающих поврежденные клетки собственного организма. Таким образом, изменяется состояние и клеточного, и гуморального иммунитета, что подтверждает аутоиммунный генез симптомокомплекса.
Классификация
Постинфарктный синдром подразделяется на 3 основные формы. В пределах каждой из них имеется несколько вариантов, классификация которых основана на локализации воспалительного процесса.
- Типичная. Клинические проявления типичной (развернутой) формы ПС связаны с воспалением перикарда, висцеральной плевры и тканей легкого. Она включает одиночные и комбинированные варианты постинфарктного аутоиммунного повреждения соединительной ткани:
- перикардиальный – воспаляется висцеральный и париетальный листок околосердечной сумки;
- плевральный – мишенью аутоантител становится плевра, на первый план выходят признаки гидроторакса;
- пневмонический – обнаруживаются инфильтративные изменения в легких, приводящие к развитию пневмонита;
- перикардиально-плевральный – присутствуют признаки сенсибилизации тканей серозной оболочки перикарда и плевры;
- перикардиально-пневмоничекий – выявляется поражение околосердечной оболочки и ткани легкого;
- перикардиально-плеврально-пневмонический – воспаление с сердечной сумки переходит на плевральные и легочные структуры.
- Атипичная. Для этой формы свойственны варианты, связанные с поражением антителами тканей сосудов и суставов. Она сопровождается воспалением крупных суставных сочленений или кожными реакциями: «синдромом плеча», пекталгией, дерматитом, узловой эритемой.
- Стертая (малосимптомная). При стертой форме со слабо выраженными основными симптомами наблюдается упорная артралгия, лихорадочное состояние и изменение количественного и качественного состава белой крови. При диагностике стертых и атипичных форм нередко возникают определенные трудности, обуславливающие актуальность более углубленного изучения данной проблемы.
Симптомы постинфарктного синдрома
Классический постинфарктный синдром формируется через 2-4 недели после ИМ. Иногда сроки могут увеличиваться или уменьшаться. К наиболее характерным симптомам заболевания относят лихорадочное состояние, болевые ощущения и тяжесть в груди, одышку, кашель. Патологический процесс чаще всего начинается остро, повышением температуры тела до субфебрильных или фебрильных отметок. Появляется слабость, головокружение, тошнота, учащается пульс и дыхание. Иногда температурные показатели остаются в пределах нормы.
Обязательным компонентом симптомокомплекса является перикардит. Для него типичны различные по интенсивности болевые ощущения в области сердца, отдающие в середину живота, под мечевидный отросток, в шею, лопатки, плечи и обе руки. Боли могут быть острыми, приступообразными, или тупыми, сжимающими. При кашле и глотании появляется чувство сдавленности в груди, болезненность усиливается. В положении стоя или лежа на животе боль ослабевает. Нередко наблюдается одышка, сердцебиение, частое поверхностное дыхание.
У 85% постинфарктных пациентов с самого первого дня появляется характерный шум трения перикардиальных листков. Он обнаруживается при аускультации, независимо от дыхания и сердечного цикла. Через несколько суток боли стихают, а шум исчезает после появления выпота. Типичное проявление плеврита – колющая односторонняя боль в верхней части туловища. Она усиливается при глубоких вдохах и наклонах в здоровую сторону. Вынужденное положение на больном боку облегчает состояние. При пальпации обнаруживается крепитация.
Для пневмонита характерно ослабленное жесткое дыхание, мелкопузырчатые хрипы, одышка, сухой или влажный кашель. Реже развивается резистентная к антибиотикам нижнедолевая пневмония. Заболевание сопровождается слабостью, усиленным потоотделением и лихорадкой. В мокроте могут обнаруживаться кровяные примеси, что существенно усложняет диагностику. При атипичных формах постинфарктного симптомокомплекса нарушаются функции различных суставов: плечевых, кистевых, грудинно-реберных. Болезнь может протекать по типу моно- и полиартритов.
Осложнения
При отсутствии своевременной диагностики и профессиональной врачебной помощи постинфарктный синдром способен привести к развитию геморрагического или констриктивного перикардита (появлению кровянистого экссудата или сдавливанию сердечных тканей), а в запущенных случаях стать причиной тяжелой тампонады сердца. Для заболевания свойственно рецидивирующее течение с обострениями и ремиссиями, возникающими в промежутках от 1-2 недель до 2-х месяцев. Как правило, под влиянием лечения наблюдается ослабление симптомов, а при отсутствии терапевтической коррекции болезнь атакует с новой силой.
Диагностика
При постановке диагноза учитываются жалобы больного, характерные клинические проявления и результаты комплексного лабораторного и инструментального обследования. К наиболее ценным диагностическим параметрам, позволяющим дать заключение о состоянии пациента на момент исследования и на дальнейшую перспективу, относят:
- Клинические критерии. Объективными признаками, подтверждающими высокую вероятность формирования постинфарктного полисерозита, является перикардит и фебрильная лихорадка. Характерной считается боль за грудиной, иррадиирующая в межлопаточную область и распространяющаяся вдоль трапециевидной мышцы, сухой кашель, различная по степени выраженности одышка.
- Лабораторные исследования. В общем анализе крови возможен лейкоцитоз, эозинофилия, увеличение СОЭ. Чтобы дифференцировать синдром Дресслера от повторного ИМ, проводится исследование крови на сывороточные маркеры повреждения миокарда. Увеличение содержания глобулярных белков – тропонина I и тропонина Т – позволяет подтвердить факт гибели клеток, случившийся в промежутке 4-48 часов. Титр противокардиальных антител остается таким же, как и при неосложненном ИМ.
- ЭКГ. На повторных электрокардиограммах наблюдается отрицательная динамика. Наиболее характерный признак – однонаправленное смещение сегмента ST в большинстве отведений (с максимальным зубцом желудочкового комплекса). По мере накопления в перикардиальной полости экссудата амплитуда комплекса ORS может снижаться.
- Рентгенография грудной клетки. При плеврите обнаруживается утолщение междолевой плевры, при перикардите расширяется сердечная тень, при пневмоните выявляются ограниченные затемнения в легких, усиливается диффузный рисунок в прикорневых зонах. В отдельных случаях на снимке четко видна кардиомегалия, ограничение подвижности левого купола диафрагмы.
- УЗИ перикарда и плевральной полости. Производится оценка эхографической картины, визуализируется утолщение листков перикарда, выявляется наличие и определяется количество жидкости в перикардиальной и плевральной полостях.
В неясных диагностических случаях для дифференциации болей и выявления жидкости в полостях или инфильтратов в легочной ткани назначается МРТ сердца и легких. При наличии признаков тампонады для уточнения характера выпота, скопившегося в околосердечной сумке, проводится диагностический перикардиоцентез с последующим лабораторным исследованием полученного материала.
Лечение постинфарктного синдрома
Лечение проходит в условиях специализированного стационара. Главная роль в перечне лечебных мероприятий принадлежит медикаментозной терапии. Она преследует несколько целей, и предполагает применение фармакопрепаратов разнонаправленного механизма действия:
- Противовоспалительные. При отсутствии противопоказаний препаратами выбора являются НПВП, которые назначаются с учетом профиля безопасности. В случае резистентности к нестероидным средствам проводятся короткие курсы глюкокортикоидов. При тяжелом течении болезни, рефрактерном к противовоспалительной терапии нестероидными средствами и гормонами, применяются ЛС других групп (колхицин, метотрексат).
- Кардиотропные. Для устранения сердечных нарушений назначаются препараты, использующиеся при лечении ишемической болезни сердца: антиангинальные средства, бета-блокаторы, блокаторы кальциевых каналов, нитраты, сердечные гликозиды. При назначении учитывается основной механизм фармакологического действия, возможные побочные эффекты и кардиотоксичность.
Антикоагулянты в связи с высоким риском развития гемоперикарда не применяются. При необходимости их использования назначаются субтерапевтические дозировки. В каждом конкретном случае лечение ПС подбирается индивидуально. При выраженных болях показаны внутримышечные инъекции анальгетиков. При большом скоплении выпота выполняется плевроцентез или пункция перикардиальной полости. При сердечной тампонаде проводится хирургическая операция – перикардэктомия.
Прогноз и профилактика
Постинфарктный синдром не является опасным для жизни состоянием, и даже при самом тяжелом течении прогноз относительно благоприятный. Методы первичной профилактики, направленной на устранение причин ПС, еще не разработаны. Для снижения частоты суставных проявлений пациентам, перенесшим острый ИМ, рекомендуется ранняя активизация. При заболеваниях с рецидивирующим течением назначается противорецидивная терапия, призванная предотвратить повторные обострения патологического процесса.
Постинфарктный синдром Дресслера
ЛИХОРАДОЧНЫЙ СИНДРОМ ДРЕССЛЕРА ПРИ ИНФАРКТЕ МИОКАРДА
В течение острого инфаркта миокарда иногда развивается диффузное воспаление перикарда, которое бывает основным проявлением клинической картины синдрома, описанного Дресслером. Этот синдром, обозначаемый Дресслером в качестве «postmyocardial infarction syndrome» (синдром после инфаркта миокарда), отличается продолжительным жаром (febris continua), длительной болью в области грудной клетки плевроперикардиального характера, перикардиальным или так же плевральным шумом трения и, во многих случаях, перикардиальным и плевральным выпотом, а иногда, кроме того, и признаками воспаления легких. Болезнь может иметь рецидивирующее течение, продолжающееся в течение месяцев. Таким образом, клиническая картина этого синдрома похожа на клиническую картину доброкачественного перикардита и на клиническую картину синдрома, иногда наблюдаемого после операции на сердце. Частым явлением при патологическом состоянии, описанном выше, осложняющим инфаркт миокарда, бывает геморрагический характер перикардита, воспаления плевры или воспаления легких.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Причина описываемых воспалительных процессов, осложняющих течение острого инфаркта миокарда, не была до сих пор выяснена. При посеве из крови, мочи, перикардиального и плеврального выпотов не было изолировано специфических возбудителей. Даже результаты серологических проб у больных не свидетельствовали в пользу инфекции. Антибиотики обыкновенно не имеют действия. Сначала Дресслер предполагал, что причиной воспалительных изменений серозных оболочек является просачивание крови в серозные полости под влиянием антикоагулянтов, но синдром наблюдался и у тех больных, у которых не проводилось такое лечение. В настоящее время многие авторы придерживаются мнения, что в данном случае воспаление перикарда и плевры является автоиммунизационной реакцией на вещества, освободившиеся при инфаркте вследствие некроза сердечной ткани, играющие роль антигенов у предрасположенного больного. Таким образом процесс имеет аутоиммунный характер, аналогично процессу, который считается причиной возникновения постперикардиотомического синдрома. И, действительно, обнаружены антитела, реагирующие на сердечную ткань в сыворотке больных с лихорадочным синдромом Дресслера. Средние и высокие титры антител, реагирующие на сердечные антигены, были обнаружены и в сыворотке нескольких больных, у которых во время инфаркта миокарда не было обнаружено лихорадочного синдрома Дресслера. Таким образом нарушение миокарда у предрасположенных лиц может вызывать процессы, аналогичные процессам при травматическом и хирургическом поражениях сердца у ревматиков. В пользу гипотезы об автоиммунизационном происхождении лихорадочного синдрома Дресслера свидетельствует также благоприятное действие глюкокортикоидов на этот синдром. Были отмечены случаи этого синдрома, сопровождающиеся эозинофилией, воспалением суставов и образованием стойких подкожных узелков. С другой стороны, было обращено внимание на аналогию между постинфарктным синдромом и острым доброкачественным воспалением околосердечной сумки, а также на периодическое массовое появление этого синдрома. Это также привело к гипотезе о вирусном происхождении синдрома, хотя это мнение не было подтверждено фактами. Есть некоторые принципиальные отличия между плевроперикардиальными проявлениями лихорадочного постинфарктного синдрома и проявлениями, связанными с поражением легких. В то время как плевроперикардиальная реакция имеет непосредственную связь с заболеванием инфаркта миокарда и является сравнительно доброкачественным осложнением с малой смертностью, легочные изменения весьма часто осложняются ритмом галопа и другими признаками недостаточности сердца, а прогноз этих осложнений в общем бывает неблагоприятным. По этой причине легочные манифестации имеют другую этиологию, и они возможно являются следствием недостаточности левого желудочка.
РАСПРОСТРАНЕНИЕ
Согласно данным, опубликованным в литературе, постинфарктный синдром встречается приблизительно в 1—3% случаев инфаркта миокарда и в большинстве случаев бывает осложнением клинически выраженного инфаркта миокарда. Лихорадочный синдром Дресслера может значительно изменить клиническое течение заболевания и замаскировать основную болезнь. С другой стороны, он может осложнять и клинически менее выраженный случай инфаркта миокарда, как и некоторые случаи с клинически скрытым течением. Такие формы Дресслер обозначает названием «коронарный» перикардит, в качестве осложнения коронарной болезни сердца без явных клинических проявлений острого очагового поражения миокарда. Напрашивается вопрос, является ли данное осложнение единственным следствием острого инфаркта миокарда, или существуют еще и другие более отдаленные реакции. И действительно, при инфаркте миокарда можно отметить, что повышенные СОЭ и температура иногда продолжаются в течение недель и, как правило, исчезают вскоре после назначения глюкокортикоидов. Такое длительное повышение температуры возможно является самым элементарным проявлением воспалительного синдрома, вызванного некрозом миокарда.
Постинфарктный синдром Дресслера может развиться в течение нескольких часов после появления первых клинических проявлений инфаркта миокарда. Все же в большинстве случаев он развивается позже, чаще всего в течение первых недель болезни, но может развиться и значительно позже. Согласно наблюдениям синдром наблюдается чаще при инфарктах задней стенки сердца, чем при инфарктах других частей сердца, и нередко сопровождается нарушением сердечного ритма.
Клиническая картина
Боль в грудной клетке может быть разнообразной. Она часто имеет плевроперикардиальный характер, реже характер грудной жабы. Боль ограничивается передней стенкой грудной клетки, имеет эпицентр в области сердца и может проводиться в левую лопатку или в обе лопатки. Иногда боль ощущается в нижней части грудной клетки, в плечевых суставах, в предплечьях, в нижней челюсти или в надчревной области. Она может иметь режущий, колющий или сжимающий характер. Чаще же всего она бывает тупой. Боль обыкновенно появляется после исчезновения ишемических болей или когда они ослабевают и может достигать различной силы, усиливаться и ослабевать под влиянием дыхательных движений грудной клетки и движений туловища. Она может вызвать чувство удушья и тревоги. Только изредка она отсутствует на протяжении всего синдрома.
Боли в суставах могут быть иногда единственной жалобой. Температура обыкновенно бывает повышенной (38—39° и более). Жар, сопровождающий постинфарктный синдром, может непосредственно следовать за лихорадочным состоянием при инфаркте миокарда, а также может развиться некоторое время спустя после нормализации температуры. Жар может продолжаться различно долгий период времени, обыкновенно же редко более одной недели.
Поражение перикарда клинически может протекать в виде сухого фибринозного или эксудативного перикардита. Важным физическим признаком бывает шум перикардиального трения.
В отличие от раннего и, обыкновенно, едва заметного и летучего шума трения при перикардите исключительно в области инфаркта миокарда (pericarditis epistenocardica), шум перикардиального трения при лихорадочном синдроме Дресслера появляется позже, бывает более громким, более стойким. Иногда он может исчезать и снова появляться. Причиной кратковременности шума перикардиального трения может быть скопление жидкого экссудата в полости перикарда. Выпот бывает часто геморрагическим. Он может быть значительным, так что время от времени появляется необходимость прибегать к повторным пункциям. Кроме того, скопление перикардиального выпота может быть причиной развития тампонады сердца.
Электрокардиографические изменения, наблюдаемые при перикардитах, в таких случаях маскируются изменениями, связанными с основным заболеванием — инфарктом миокарда — а в некоторых случаях синдрома Дресслера они вообще могут отсутствовать. Однако возможна инверсия зубца Т в отведениях от конечностей и в грудных отведениях, которая может исчезнуть с прекращением остальных признаков перикардита.
Изолированный плеврит обыкновенно не осложняет инфаркт миокарда, хотя при синдроме Дресслера воспаление плевры бывает частым явлением. Клинически оно может протекать в качестве сухого фибринового плеврита или плеврита экссудативного. Экссудат довольно часто бывает геморрагическим, иногда с выраженной эозинофилией. В некоторых случаях наблюдаются признаками воспалительной легочной инфильтрации, обыкновенно в базальной части легкого. Воспаление легких, в свою очередь, может иметь геморрагический характер и сопровождаться кровохарканьем, так что нередко возникает подозрение на инфаркт легкого. Лейкоцитоз бывает частым явлением с повышением количества полинуклеаров и отклонением нейтрофилов влево.
ДИАГНОЗ
Для врача, знающего сущность синдрома, постановка диагноза не бывает затруднительной. Лихорадочный синдром Дресслера устанавливается при следующих обстоятельствах:
- а) если до истечения одной недели после начала клинических проявлений инфаркта миокарда температура остается повышенной и если отсутствует какая-либо другая причина лихорадочного состояния;
- б) если после инициального лихорадочного периода появляется новое повышение температуры;
- в) если в грудной клетке появляются боли плевроперикардиального характера, в особенности после исчезновения стенокардических жалоб;
- г) если появляется шум трения перикарда, в особенности, когда таковой выслушивается сравнительно долго;
- д) если на электрокардиографической кривой появляются изменения, характерные для воспаления перикарда, что подтверждается на эхокардиографии;
- е) если появляются признаки воспаления плевры или легких.
Характерным бывает частое несоответствие между интенсивностью и длительностью боли и жара и сравнительно бедными результатами объективного исследования. Постинфарктный лихорадочный синдром Дресслера отличается от диффузного перикардита, сопровождающего инфаркт и развивающегося в течение первых дней заболевания, геморрагическим характером выпота и со¬пряжением перикардита с плевритом или даже с воспалительными изменениями в легких.
Диагностические затруднения могут возникать при клинически и электрокардиографически слабо выраженных признаках инфаркта миокарда. В таких случаях бывает необходимо учесть и другие возможные причины перикардита, например, туберкулез или красную диссеминированную волчанку.
С дифференциально диагностической точки зрения необходимо помнить о возможности рецидива инфаркта миокарда и об инфаркте легких. Электрокардиографическое исследование часто бывает бес¬ценным с диагностической точки зрения, так как изменения, связанные с перикардитом, могут быть замаскированы изменениями на почве обширного инфаркта миокарда. Дифференциальный диагноз лихорадочного синдрома Дресслера от рецидива или дальнейшего развития острого инфаркта сердца возможен путем определения содержания различных трансаминаз в кровяной сыворотке.
Распознание постинфарктного синдрома Дресслера имеет важное значение с прогностической и терапевтической точек зрения. Если патологическое состояние не получает правильную оценку, то оно обыкновенно принимается за проявление прогрессии инфарктных изменений в миокарде. На самом же деле осложнение имеет, в сущности, доброкачественный характер.
ПРОГНОЗ
Продолжительность синдрома может быть различной. В среднем он продолжается от 7 до 14 дней. В случае осложнений и рецидивов он может продолжаться даже несколько месяцев. Шум перикардиального трения может выслушиваться в продолжение недель и месяцев. Если исключить риск, связанный с развитием тампонады сердца, можно считать прогноз синдрома, как такового, в общем благоприятным. Однако этот синдром может значительно продлить пребывание пациента в стационаре.
ЛЕЧЕНИЕ
Часто нет необходимости особого лечения, так как синдром излечивается самопроизвольно. Иногда приходится назначать синтетические болеутоляющие средства. В случаях с бурным течением постинфарктного синдрома, с упорными болями и длительным течением, рекомендуется назначение глюкокортикоидов. При этом способе лечения возможно быстрое падение температуры, исчезновение жалоб и быстрое рассасывание выпота. Также большинство авторов не считают целесообразным прерывать лечение антикоагулянтами у больных с большими инфарктами миокарда.
Синдром Дресслера

Постинфарктный синдром (или синдром Дресслера) — реактивное аутоиммунное осложнение инфаркта миокарда, развивающееся через 2—6 недель после его начала.
Частота развития
Первоначально считалось, что синдром Дресслера возникает примерно у 4% больных, перенесших инфаркт миокарда. C учетом атипичных и малосимптомных форм частота его развития значительно выше – 15–23 %, а по некоторым источникам достигает 30 %. Однако в последние годы частота синдрома Дресслера уменьшилась. Причинами могут быть широкое использование нестероидных противовоспалительных средств (ацетилсалициловой кислоты) и распространение реперфузионных методов лечения ИМ, уменьшающих объем повреждения мышцы сердца. Другой причиной снижения частоты развития синдрома Дресслера может быть включение в комплекс терапии инфаркт миокарда ингибиторов ангиотензинпревращающего фермента, антагонистов альдостерона и статинов, вследствие их иммуномодулирующего и противовоспалительного действия. Постинфарктый синдром развивается в подостром периоде (не ранее 10-го дня от момента заболевания) у 3—4 % пациентов, перенёсших инфаркт миокарда.
Причины развития
Основная причина синдрома Дресслера – инфаркт миокарда. Считается, что синдром Дресслера чаще развивается после крупноочаговых и осложненных инфарктов, а также после кровотечений в полость перикарда. Синдром Дресслера, точнее синдром постповреждения сердца, может развиваться после кардиохирургических вмешательств (постперикардиотомический синдром, посткомиссуротомический синдром). Помимо этого, типичные признаки синдрома Дресслера могут появляться после других повреждений сердца (ранение, контузия, непроникающий удар в область грудной клетки, катетерная абляция). В настоящее время синдром Дресслера рассматривается как аутоиммунный процесс, обусловленный аутосенсибилизацией к миокардиальным и перикардиальным антигенам. Определенное значение придается также антигенным свойствам крови, попавшей в полость перикарда.
При постинфарктном синдроме антитела к тканям сердца обнаруживаются постоянно. При анализе субпопуляций лимфоцитов у пациентов с синдром Дресслера было обнаружено увеличение числа активированных CD8-позитивных клеток. При изучении активации комплемента было отмечено, что у пациентов с СД наблюдали повышенный уровень фракции C3d в сочетании с более низкой концентрацией С3. Кардиальные реактивные антитела, связываясь с циркулирующими кардиальными антигенами с формированием растворимых иммунных комплексов, могут фиксироваться в различных местах, приводя к комплементопосредованному повреждению ткани.
При постинфарктном синдроме наблюдаются изменения и в клеточном иммунитете. Так, имеются данные, что при синдроме Дресслера значительно повышен уровень цитотоксических T-клеток. Этиологическим фактором синдрома Дресслера может быть инфекция, в частности вирусная, поскольку у больных, у которых этот синдром развился после кардиохирургических вмешательств, часто регистрируют повышение титра противовирусных антител.
Симптомы и течение
Развивается на 2–4-й неделе инфаркта миокарда, однако эти сроки могут уменьшаться – «ранний синдром Дресслера» и увеличиваться до нескольких месяцев, «поздний синдром Дресслера». Иногда течение синдрома Дресслера принимает агрессивный и затяжной характер, он может длиться месяцы и годы, протекать с ремиссиями и обострениями. Основные клинические проявления синдрома: лихорадка, перикардит, плеврит, пневмонит и поражение суставов. Лихорадка при синдроме Дресслера не имеет какой-либо строгой закономерности. Как правило, она бывает субфебрильной, хотя в отдельных случаях может быть фебрильной или вообще отсутствовать.
Перикардит является обязательным элементом синдрома Дресслера. Клинически он проявляется болью в перикардиальной зоне, которая может иррадиировать в шею, плечо, спину, брюшную полость. Боль может быть острой приступообразной (плевритическая) или давящей, сжимающей (ишемической). Она может усиливаться при дыхании, кашле, глотании и ослабевать в вертикальном положении или лежа на животе. Она длительная и исчезает или ослабевает после появления в полости перикарда воспалительного экссудата. Главный аускультативный признак перикардита – шум трения перикарда: в первый день болезни при внимательной аускультации он определяется у абсолютного большинства (до 85 %) больных. Шум лучше всего выслушивается у левого края грудины, при задержке дыхания и наклоне туловища пациента вперед. В классическом варианте он состоит из трех компонентов – предсердного (определяется в систолу) и желудочкового (систолического и диастолического). Как и боль, шум трения перикарда уменьшается или исчезает вовсе после появления в полости перикарда выпота, раздвигающего трущиеся листки перикарда. Обычно перикардит протекает нетяжело: уже через несколько дней боли стихают, а экссудат в полости перикарда почти никогда не накапливается в таком количестве, чтобы ухудшить кровообращение, хотя иногда могут появиться признаки тяжелой тампонады сердца. Иногда воспалительный процесс в перикарде при синдроме Дресслера принимает затяжной рецидивирующий характер и заканчивается развитием констриктивного перикардита. При применении антикоагулянтов на фоне синдрома Дресслера возможно также развитие геморрагического перикардита, хотя подобное осложнение может быть и при отсутствии антикоагулянтной терапии.
Плеврит. Проявляется болью в боковых отделах грудной клетки, усиливающейся при дыхании, затруднением дыхания, шумом трения плевры, притуплением перкуторного звука. Он может быть сухим и экссудативным, односторонним и двусторонним. Нередко плеврит носит междолевой характер и не сопровождается типичными физикальными симптомами.
Пневмонит. Пневмонит при синдроме Дресслера выявляется реже, чем перикардит и плеврит. Если очаг воспаления достаточно велик, также отмечается притупление перкуторного звука, ослабленное или жесткое дыхание, появление фокуса мелкопузырчатых хрипов. Возможен кашель и выделение мокроты, иногда с примесью крови, что всегда вызывает определенные диагностические трудности.
Поражение суставов. Для синдрома Дресслера характерно появление так называемого «синдрома плеча»: болезненных ощущений в области плечелопаточных суставов, чаще слева, ограничение подвижности этих суставов. Вовлечение в процесс синовиальных оболочек нередко приводит к возникновению болей и в крупных суставах конечностей.
Другие проявления. Проявлением постинфарктного синдрома может быть сердечная недостаточность вследствие диастолической дисфункции, геморрагический васкулит и острый гломерулонефрит.
Методы исследования
Лабораторные данные. Часто отмечается повышение СОЭ и лейкоцитоз, а также эозинофилия. Весьма характерно резкое повышение уровня С-реактивного белка. У больных с синдромом Дресслера регистрируются нормальные уровни маркеров повреждения миокарда (МВ-фракция креатинфосфокиназы (МВ-КФК), миоглобин, тропонины), хотя иногда отмечается их незначительное повышение, что требует проведения дифференциальной диагностики с рецидивом инфаркта миокарда.
Электрокардиография (ЭКГ). При наличии перикардита на ЭКГ определяются диффузный подъем сегмента ST и, периодически, депрессия сегмента PR, за исключением отведения aVR, в котором наблюдаются депрессия ST и подъем PR. По мере накопления экссудата в полости перикарда может снизиться амплитуда комплекса QRS.
Эхокардиография. При накоплении жидкости в полости перикарда выявляется сепарация его листков и могут появиться признаки тампонады сердца. Для синдрома Дресслера не характерен большой объем жидкости в полости перикарда – как правило, сепарация листков перикарда не достигает 10 мм в диастолу.
Рентгенография. Обнаруживают скопление жидкости в плевральной полости, междолевой плеврит, расширение границ сердечной тени, очаговые тени в легких.
Компьютерная или магнитнорезонансная томография также выявляют жидкость в полости плевры или перикарда и легочную инфильтрацию.
Плевральная и перикардиальная пункция. Извлеченный из полости плевры или перикарда экссудат может быть серозным или серозно-геморрагическим. При лабораторном исследовании в нем определяется эозинофилия, лейкоцитоз и высокий уровень С-реактивного белка.
Лечение
Нестероидные противовоспалительные препараты (НПВС). Препаратом выбора при синдроме Дресслера традиционно считается ибупрофен (400– 800 мг/сут). Реже используют аспирин. Хирургическое лечение применяется при констриктивном перикардите.
Осложнения
Тампонада сердца, геморрагический или констриктивный перикардит, окклюзия (сдавление) коронарного шунта и редко – анемия.
Прогноз
Прогноз при синдроме Дресслера, как правило, благоприятный. Вместе с тем его течение иногда принимает затяжной рецидивирующий характер. Кроме того, имеются данные о том, что выживаемость в течение 5 лет среди перенесших этот синдром, хотя и незначительно, но снижается.
Аутоиммунный процесс развивающийся после инфаркта миокарда и проявляющийся перикардитом, плевритом, воспалительными заболеваниями суставов и сосудов. Лечение проводится с помощью противовоспалительных препаратов.
Постинфарктный синдром
Постинфарктный синдром, несмотря на «всеобъемлющее» название, на самом деле является лишь одним из многочисленных возможных осложнений инфаркта миокарда. Это болезненное состояние часто определяют как сочетание трех «П» – плеврит, пульмонит, перикардит. Эпонимом послужило имя американского кардиолога Уильяма Дресслера, поляка по происхождению, который в 1956 году впервые описал данный симптомокомплекс как единый синдром.
Частота встречаемости синдрома Дресслера у лиц, перенесших острый инфаркт миокарда, поначалу оценивалась на уровне 1-3%. Однако дальнейшие исследования показали, что постинфарктное воспаление органов грудной клетки встречается в различных вариантах, и при корректном учете всех атипичных, редких, малосимптомных форм эпидемиологическую оценку пришлось бы поднять примерно до 30% от общего числа кардиологических больных, наблюдающихся после инфаркта. На сегодняшний день большинство источников сообщает о распространенности синдрома Дресслера в пределах 7-10%.
Причины
Этиопатогенез постинфарктного синдрома в настоящее время трактуется как аутоиммунная атака, реакция защитной системы организма на пораженные инфарктом клетки миокарда. Такая точка зрения поддерживается большинством отечественных и зарубежных специалистов, однако некоторые авторы оговаривают гипотетический ее характер: чтобы утверждать наверняка, необходимы дополнительные исследования и убедительные доказательства сугубо аутоиммунной природы данного синдрома. В последние годы, скажем, вновь активно обсуждается возможная этиологическая роль вирусных инфекций, хотя ранее такое предположение отвергалось. Кроме того, само название «постинфарктный синдром» является неполным, так как тот же симптомокомплекс может развиться после закрытой или проникающей травмы в области сердца, кардиохирургического вмешательства, кровоизлияния в сердечную сумку и т.д.
Симптоматика
Синдром Дресслера обычно манифестирует через 12-28 дней после острого инфаркта миокарда (или иного острого состояния, послужившего причиной развития, см. выше). Таким клиническим составляющим «синдрома трех П», как плеврит и перикардит, на нашем сайте посвящены отдельные материалы, поэтому нет нужды останавливаться на них подробно. Что касается третьей составляющей, – пневмонита, – то этот термин в разных контекстах используется для обозначения атипичных, неинфекционных пневмоний (см., например, «Бензиновая пневмония»), либо как указание на преимущественное поражение альвеолярных стенок, либо как как синоним аутоиммунного воспаления соединительнотканного «каркаса» легких.
Клинически сочетание плеврита, перикардита и пневмонита проявляется разнообразными по характеру болями в области сердца и в боковых отделах грудной клетки, часто с иррадиацией в шею, спину, плечо и т.д.; как правило, боль усиливается при кашле или глотании. Отмечаются затруднения дыхания, одышка, кашель, в некоторых случаях с мокротой или примесью крови. Малосимптомной форме синдрома Дресслера присуще стойкое повышение температуры тела, боли в суставах. Среди атипичных форм выделяют суставный и кожный варианты, – в первом случае доминирует симптоматика артрита, во втором наблюдаются различные высыпания, эритемы и другие признаки дерматита. Иногда постинфарктный синдром протекает со значительно выраженной сердечной недостаточностью, осложнениями со стороны сосудов, почек и т.п.
Диагностика
Выявление и дифференциация синдрома Дресслера от клинически сходных состояний может представлять непростую задачу даже для специалиста. Обследование всегда носит комплексный характер, включая батарею лабораторных анализов, ЭКГ, ЭхоКГ, рентгенографию органов грудной клетки, плевральную пункцию (см. «Торакоцентез»).
Лечение
Основу терапевтической стратегии составляют нестероидные противовоспалительные средства, антикоагулянты, в более тяжелых случаях – глюкокортикостероидные гормоны. Однако схема всегда строго индивидуальна, она определяется результатами диагностического обследования и особенностями конкретного случая. Изредка приходится прибегать к хирургическому вмешательству (перикардиоцентез, перикардэктомия). Прогноз обычно благоприятный, однако иногда встречаются затяжные, хронические, рецидивирующие формы.


