Нефротический синдром
Нефротический синдром (НС) представляет собой симптомокомплекс (т.е. комплекс из отдельных симптомов, при наличии которых ставится диагноз), которые характеризуется ниже перечисленными симптомами:
- Наличие ПРОТЕИНУРИИ (наличие белка в моче, более 3,5 г/1,73м2 в сутки (в норме отрицательный или до 0,03 г/л)
- Низкий уровень общего белка и его фракции (альбумин ниже 25 г/л) в крови, вследствие потери его с мочой
- Отеки мягкий тканей всего тела (чаще всего начинается с пастозности век, с отека лица, нижних конечностей и т.д.)
- Повышенный уровень холестерина в крови
Распространенность примерно 1 случай на 6000 детей.
В большинстве случаев у детей раннего возраста наиболее распространенным является идиопатический вариант НС (т.е. причина возникновения заболевания неизвестный), который чаще всего имеет гистопатологическую основу, именуемым «болезнь минимальных изменений», причины возникновения которого не известно.
КАКИЕ ИМЕННО СИМПТОМЫ НАБЛЮДАЮТСЯ ПРИ НЕФРОТИЧЕСКОМ СИНДРОМЕ?
ЗАБОЛЕВАНИЕ МОЖЕТ НАЧАТЬСЯ БЕЗ ВИДИМОЙ ПРИЧИНЫ, В РЯДЕ СЛУЧАЕВ ПРЕДШЕСТВУЮТ ИНФЕКЦИИ ИЛИ АЛЛЕРГИЧЕСКИЕ РЕАКЦИИ.
Ниже перечислены наиболее часто встречающиеся симптомы:
- Усталость и общее недомогание
- Сниженный аппетит
- Прибавка массы тела и отеки лица, нижних конечностей
- Увеличение объем живота (вследствие задержки жидкости) и боль в животе
- Пенистая моча
- Задержка жидкости в полостях организма (Асцит – задержка жидкости в брюшной полости; перикардит – задержка жидкости в околосердечной сумке; плеврит – задержка жидкости в плевральной полости)
- Иногда НС сочетается с гематурией (наличие эритроцитов в моче) и/или артериальной гипертензии, что требует исключения нефритического процесса
Данные симптомы нефротического синдрома могут быть схожи с другими патологиями и заболеваниями, всегда консультируйтесь с нефрологом в случае наличия таких симптомов у вашего ребенка.
КАК МОЖНО ДИАГНОСТИРОВАТЬ НЕФРОТИЧЕСКИЙ СИНДРОМ?
Дополнительно к клиническому осмотру и полноценному опросу истории болезни, необходимо проведение следующих диагностических тестов:
- Общий анализ мочи (выявление протеинурии)
- Биохимический анализ крови (анализ уровня общего белка и его фракции (альбумин) и уровень холестерина)
- Ультразвуковое исследование почек
ЛЕЧЕНИЕ НЕФРОТИЧЕСКОГО СИНДРОМА
Лечение назначается только лечащим врачом — нефрологом, учитывая:
- Возраст ребенка, общее здоровье и истории болезни
- Степень тяжести болезни
- Индивидуальная непереносимость к некоторым видам лекарствам (аллергия)
- Ожидаемые результаты от применения терапии
Во время первого эпизода нефротического синдрома, вашему ребенку может потребоваться госпитализация, для проведения мониторирования отеков (в случае тяжелых полостных отеков), артериального давления и т.д.
Стандартная терапия НС состоит в 6 недельном курсе преднизолона в дозе 2 мг/кг массы тела или 60 мг/м2, данная терапия сопровождается ремиссией (исчезновение симптомов болезни) протеинурии более чем у 90% детей, однако у большинства из них болезнь рецидивирует (возврат симптомов болезни). (Таблица 1: варианты НС в зависимости от ответа на стандартный курс преднизолона). По окончании 6 недельного курса переходят на прием преднизолона в альтернирующем режиме (через день). Данный режим используется в течение 4-6 недель, после чего производится постепенное снижение дозы по 10мг/м2 в неделю, а иногда и медленнее, до полной отмены.
При рецидиве НС возможно повторение той же схемы, что и при первом эпизоде болезни, если рецидив произошел после достаточно продолжительного срока ремиссии. В других случаях применяются другие схемы терапии и других лекарственных средств, которые решаются в зависимости от состояния развития рецидива НС (на фоне приема преднизолона и на какой дозе), тяжести заболевания, возраста ребенка.
Таким образом, если вы заметили выше перечисленные симптомы заболевания у вашего ребенка, не теряя времени, обращайтесь к специалисту, для решения вопроса о подборе терапии, так как запоздалое начало терапии может привести к серьезным последствиям.
Если Вас волнует проблема, изложенная в тексте, обращайтесь к нам, и мы Вам обязательно поможем.
Нефротический синдром у детей
Нефротический синдром у детей — это симптомокомплекс, который клинически проявляется отеками и снижением диуреза. Лабораторные признаки патологии — протеинурия, гиперлипидемия, гипоальбуминемия и диспротеинемия. Синдром развивается при первичных гломерулопатиях, аутоиммунных, онкогематологических и сердечно-сосудистых заболеваниях. Для диагностики проводят анализы крови и мочи, биопсию почки, ЭхоКГ и ЭКГ. Лечение включает длительные курсы иммуносупрессорной терапии (глюкокортикоиды, алкилирующие агенты, ингибиторы кальциневрина) в комбинации с нефропротекторными, гипотензивными и мочегонными препаратами.
МКБ-10

Общие сведения
Распространенность нефротического синдрома составляет 12-16 случаев на 100 тыс. детского населения. Ежегодно нефрологи выявляют от 2 до 7 новых случаев заболевания на 100 тысяч пациентов младше 18 лет. Патология не относится к самостоятельным нозологическим единицам, а представляет собой один из синдромов почечных или внепочечных болезней. Актуальность этой проблемы в педиатрической практике обусловлена сложностью терапии и частыми случаями резистентности к лекарствам.

Причины
У детей чаще выявляются первичные формы нефротического синдрома, вызванные поражением клубочкового аппарата почек. В 85% морфологическим субстратом является болезнь минимальных изменений, до 5-7% составляет фокально-сегментарный гломерулосклероз, 4-6% отводится мезангиопролиферативному гломерулонефриту. Вторичный вариант заболевания имеет несколько этиологических факторов:
- Аутоиммунные процессы. Они сопровождаются образованием иммунных комплексов и провоспалительных цитокинов, которые откладываются в почечных капиллярах, нарушая работу фильтрационной системы органа. У детей причиной могут послужить системные васкулиты, системная красная волчанка, синдром Шегрена.
- Злокачественные опухоли. Почечные поражения возникают при лимфоме Ходжкина и неходжкинских новообразованиях, которые зачастую встречаются в детском возрасте. Среди менее распространенных онкологических факторов выделяют множественную миелому, солидные опухоли.
- Токсические повреждения почек. Нефротический синдром возможен при длительном и бесконтрольном приеме ребенком нестероидных противовоспалительных средств и некоторых антибиотиков. Поражение почек также наблюдается при отравлении солями тяжелых металлов, ядами змей и перепончатокрылых насекомых.
- Нарушения почечного кровотока. Повышенная секреция белка в мочу происходит при структурных повреждениях почечных клубочков на фоне тотальной ишемии. Она может быть вызвана тромбозом почечной вены, серповидно-клеточной анемией, злокачественной гипертензией.
- Врожденные гломерулопатии. У детей встречается синдром Альпорта, для которого характерны мутации коллагеновых волокон в базальных мембранах клубочков. Реже диагностируется болезнь Фабри, когда нефропатия связана с нарушениями метаболизма сфинголипидов.
Патогенез
На начальных этапах нефротического синдрома развивается протеинурия, вызванная повышением проницаемости почечного фильтра для белков. Это обусловлено структурно-функциональными повреждениями компонентов почечного клубочка. Большую роль в этом процессе имеют аутоиммунные механизмы: активированные Т-лимфоциты вырабатывают специфические цитокины, которые повреждают клеточные мембраны и «щелевые» контакты подоцитов.
Повышенная потеря белков с мочой снижает онкотический показатель крови. Как следствие, жидкость по градиенту давления начинает перемещаться из сосудистого русла в ткани. Таким образом формируются массивные нефротические отеки. Их интенсивность зависит от степени белковых потерь и активности компенсаторных механизмов. В 10% случаев отечный синдром развивается вследствие первичной задержки натрия в организме.
Симптомы
Для патологии типично острое начало, связь с перенесенной инфекцией, переохлаждением, вакцинацией или обострением хронической соматической болезни. Сначала ребенок жалуется на общую слабость, недомогание, сонливость и заторможенность. Реже беспокоят головные и абдоминальные боли, тошнота, снижение аппетита. У девочек-подростков бывают нарушения менструального цикла.
Основное проявление нефротического синдрома — отеки. Вначале они возникают на лице (утром) и на голенях (вечером, после длительной ходьбы), а затем постепенно распространяются по всему телу. Первоначально они мягкие, расположены симметрично, кожа над ними теплая и сухая. Параллельно с этим снижается количество суточной мочи. Периферические отеки дополняются полостными — асцитом, гидроперикардом, гидротораксом, что ухудшает состояние ребенка.
Осложнения
Негативные последствия нефротического синдрома вызваны потерей альбуминов, которые в норме выполняют ряд физиологических функций. Потеря иммуноглобулинов ухудшает иммунную защиту организма, что проявляется частыми респираторными инфекциями, рецидивирующими тонзиллитами и синуситами. Снижение количества трансферрина (переносчика железа) приводит к рефрактерной железодефицитной анемии.
Значимым осложнением для детей младшего возраста является потеря витамин-Д-связывающего белка. В результате формируется рахитоподобный синдром, нарушается минерализация и рост костей скелета. В редких случаях развивается повышенная кровоточивость из-за дефицита прокоагулянтов. При стероидорезистентном варианте болезнь в течение 5-10 лет прогрессирует до терминальной ХПН.
Диагностика
При физикальном осмотре детский нефролог обращает внимание на симметричность и расположение отеков, проводит аускультацию сердца и легких, определяет признаки асцита и увеличения печени. Симптомы не дают возможности установить клинический диагноз, поэтому врач назначает полное обследование. Составляющие диагностического комплекса:
- Анализ мочи. Патогномоничными признаками нефротического синдрома являются протеинурия более 50 мг/кг/сутки, соотношение протеин/креатинин более 2 и экскреция альбумина свыше 40мг/м 2 /час. Для исключения эритроцитурии и лейкоцитурии показан анализ по Нечипоренко. Функцию почек оценивают с помощью пробы Реберга.
- Анализ крови. При биохимическом исследовании выявляют уровень альбумина сыворотки менее 30 г/л, повышение уровня холестерина и триглицеридов, увеличение показателя креатинина. Уровни натрия и кальция крови снижаются, а калий может быть повышен. В коагулограмме наблюдается повышение фибриногена.
- ЭхоКГ. Ультразвуковая визуализация необходима для обнаружения гидроперикарда, морфометрических изменений крупных сосудов вследствие отеков. Также рекомендована ЭКГ, которая позволяет вовремя заметить нарушения ритма и проводимости, связанные с электролитными нарушениями.
- Биопсия почки. Пункционный забор материала выполняется при нефротическом синдроме у младенцев до 1 года и подростков старше 12 лет, а также при неэффективности стандартной медикаментозной терапии. Биоптаты подвергают световой, электронной и иммунофлюоресцентной микроскопии.
Лечение нефротического синдрома у детей
Дети с острым нефротическим синдромом подлежат обязательной госпитализации на 2-3 недели. Двигательная активность при этом не ограничивается и соответствует самочувствию больного. В диете необходимо поддерживать высокий уровень белков, а подросткам с массивными отеками рекомендовано снизить потребление поваренной соли. При выраженных потерях протеинов назначается коррекция гомеостаза коллоидными и кристаллоидными растворами.
Основу патогенетического лечения детей с нефротическим синдромом составляет иммуносупрессивная терапия с применением глюкокортикоидов. Препараты уменьшают образование и поступление в патологический очаг воспалительных клеток, угнетают секрецию медиаторов воспаления, приостанавливают формирование токсических иммунных комплексов. Терапия глюкокортикоидами проводится в 3-х режимах:
- Постоянный. Показан в начале лечения, чтобы быстро достичь фазы ремиссии. Гормоны принимаются перорально в первой половине дня в суточной дозировке 1-2 мг/кг.
- Альтернирующий. Назначается после достижения ремиссии. Стандартные дозы глюкокортикоидов используются через день, чтобы сохранить клинический эффект, но снизить риски побочных реакций.
- Пульс-терапия. Применяется при тяжелом течении нефротического синдрома. Гормоны вводятся внутривенно капельно, чтобы в короткие сроки достичь высоких концентраций лекарства в крови.
При развитии тяжелых побочных эффектов на гормональные препараты или стероидорезистентном варианте заболевания переходят на другие виды иммуносупрессоров. В детской нефрологии наилучший результат показывают ингибиторы кальциневрина, алкилирующие агенты, некоторые моноклональные антитела к лимфоцитам. Они могут вызывать нефротоксичность, поэтому во время лечения врачи контролируют уровень СКФ.
Для устранения массивных отеков проводится терапия петлевыми диуретиками в возрастных дозировках. С целью ликвидации рефрактерных полостных отеков назначаются комбинации петлевых и тиазидных мочегонных. В качестве гипотензивных и нефропротекторных средств у детей лучше всего работают ингибиторы АПФ и блокаторы рецепторов ангиотензина. Коррекцию остеопении производят препаратами витамина Д.
Прогноз и профилактика
У детей с хорошим ответом на стероидную терапию в 95% наблюдается полное выздоровление без снижения функции почек. Менее благоприятный прогноз при стероидорезистентности, поскольку у таких пациентов высокий риск формирования хронической почечной недостаточности. Однако, своевременное применение иммуносупрессоров и нефропротекторов позволяет замедлить патологический процесс.
Первичная профилактика включает рациональное назначение лекарств, раннюю диагностику и терапию аутоиммунных процессов, избегание контактов с нефротоксическими веществами. Вторичная профилактика предполагает курсы гормональной терапии при обострении основной патологии либо в случае интеркуррентного заболевания. Это необходимо для предупреждения рецидивов нефротического синдрома.
4. Нефротический синдром у детей: определение и принципы терапии/ С.В. Бельмер, А.В. Малкоч// Лечащий врач. — 2004.
Нефротический синдром у детей: особенности развития и тактика лечения
Нефротический синдром у детей – общий термин, обозначающий совокупность внутренних или внешних факторов, которые способствуют разрушению почечной ткани, вызывая развитие органной недостаточности. Разница между вторичной и первичной формами патологии заключается в причине, вызвавшей болезнь. Нефротический синдром диагностируют на основании данных лабораторных исследований, предъявляемых жалоб. При обнаружении характерных признаков нефроурологической патологии важно начать своевременное лечение.
Нефротический синдром у детей – комплекс симптомов, указывающих на недостаточность функции почек
Особенности состояния
Нефротический синдром – обширный симптомокомплекс, развитие которого обусловлено поражением почек и почечных структур различной тяжести. Состояние характеризуется появлением белка в моче, отечностью нижних конечностей и лица, дистрофией слизистых оболочек или кожных покровов. Существуют две основных формы нефротического синдрома:
- первичная, когда патология развивается изолированно (врожденный нефрит);
- вторичная, когда симптомокомплекс становится следствием провоцирующих факторов: инфекции, аутоиммунной патологии, воспалительного процесса, синдрома Альпорта.
Клиницисты выделяют генетическую форму нефротического синдрома, появление которой обусловлено наследственной предрасположенностью. По статистике, почти в 25% нефротический синдром значительно ухудшает функцию почек, осложняет течение основного урологического или нефрологического заболевания. Вторичный патологический синдром клинически обратим, но только при сохранении функции почек до 60–75%.
Причины и факторы развития
Механизм возникновения заключается в повышении проницаемости клубочковых структур почек для белкового компонента на фоне повреждения. Потеря белка с мочой свидетельствует о развитии гипопротеинемии, гипоальбуминемии. Если истинная причина возникновения синдрома у детей остается невыясненной, то диагностируют идиопатический тип болезни. Запустить механизм выхода белка в мочу и разрушения клубочков могут следующие факторы:
- вакцинация, длительное применение средств, так или иначе влияющих на иммунитет;
- длительное или постоянное применение противосудорожных препаратов;
- перенесенные инфекции, особенно органов мочеполовой и мочевыделительной системы;
- гломерулонефрит любой природы;
- туберкулез любой локализации;
- интоксикации различного генеза.
В группе риска – часто болеющие дети, больные с осложненным клиническим анамнезом: аномалиями развития почек и внутренних органов, дисплазиями, гиперплазиями, первичной артериальной гипертензией, кардиологическими патологиями. Частые обострения при пиелонефрите способствуют развитию симптомокомплекса в 45% случаев.
Симптоматический комплекс
Симптоматический комплекс при нефропатиях типичен, однако варьирует в зависимости от основной причины, тяжести поражения почек. Выявляют следующие признаки:
- при анализе мочи – обширная протеинурию, гипопротеинемию ниже 40 г/л, гипоальбуминемию;
- анализе крови – увеличение уровня мочевины и креатинина, повышение холестерина, снижение клиренса креатинина.
Острый нефротический синдром возникает стремительно, объем суточной мочи резко снижается, отмечаются повышение артериального давления, отечность. Хроническое течение может протекать латентно, отражаясь только в данных лабораторных исследований. Другими симптомами нефротического синдрома являются:
- мышечные боли;
- отечность, вплоть до гидроторакса, анасарки, асцита;
- олигурия – уменьшение суточного диуреза.
Функция почек страдает умеренно, интоксикация сопровождается головной болью, рвотой, постоянной жаждой, отсутствием или нарушением аппетита. Присоединение пищеварительных расстройств связано с раздражением слизистых оболочек из-за воздействия остаточного азота. При хронической нефропатии внешний вид детей болезненный, кожные покровы бледные, лицо одутловатое. При осмотре отмечается обложенный язык, пульс несколько замедлен, тоны сердца часто приглушены.
Для нефротического синдрома характерно волнообразное течение с периодическими обострениями и ремиссией.
Диагностические мероприятия
Лечение определяется характером поражения почечных структур
Нефротический синдром является областью исследования нефрологии, а при осложнениях в мочевыделительной системе – урологии. При появлении первых симптомов рекомендуется наблюдение у детского нефролога. Первичное исследование включает в себя:
- анализ мочи – определяют плотность, наличие и количество лейкоцитов, белка, холестеринова, нейтрального жира, эритроцитов;
- анализ крови – определяют скорость оседания эритроцитов, наличие и количество гемоглобина, тромбоцитов, лейкоцитов, креатинина, мочевины.
Для уточнения патологии возможно проведение проб мочи по Зимницкому, Ребергу, Нечипоренко. Идиопатический тип заболевания также включает в себя все клинические критерии патологии. Обязательно проводят инструментальные исследования:
- ультразвуковое исследование почек, органов брюшины (оценивается мочевой пузырь и его функции);
- рентгенконтрастную урографию для оценки выделительной функции почек;
- биопсию.
Последнее исследование подразумевает лапароскопический забор биоптата для гистологического исследования. Метод не применяется при хаотичном почечном кровотоке, когда риски угрожающих жизни осложнений достигают 95%.
По результатам исследований важно выяснить причину поражения почек, дифференцировать состояние от системной красной волчанки, хронического воспаления с тяжелым поражением почечной ткани и гломерул. При идиопатической форме исключают синдром БМИ (болезнь минимальных изменений), IgA-нефропатию. Напоминать течение нефротического синдрома могут мезангиокапиллярный гломерулонефрит, туберкулез почек, васкулиты, аутоиммунные патологии.
Лечение
Лечение нефритов направлено на устранение пускового механизма развития симптомокомплекса, восстановление почечной ткани и предупреждение ее дальнейшего разрушения. Перспективным направлением является медикаментозная терапия. Хирургическое лечение, физиотерапия, народные рецепты неэффективны. Типичная медикаментозная схема предполагает назначение следующих препаратов:
- плазмовосстанавливающие растворы для внутривенного введения. Способствуют улучшению реологических свойств крови, восполнению утраченных альбуминов;
- гормональная терапия для восстановления утраченного белка;
- цитостатики для предупреждения дальнейшего разрушения тканей почек, развития опухолевых процессов, малигнизации клеток;
- диуретики для выведения избыточной жидкости из организма, лечения отеков. Диуретические средства применяются в комплексе антигипертензивной терапии;
- антикоагулянты для улучшения кровотока, разжижения крови.
Острый тип нефропатии нередко требуется сеанса заместительной терапии для облегчения состояния ребенка, очищения крови.
Обязательно назначают препараты кальция и витамин Д для предупреждения размягчения, деформации и истончения костной ткани. Если патологический синдром вызван частыми обострениями инфекционных или воспалительных процессов, то назначаются витаминные комплексы, иммуномодулирующие средства.
Диета и рацион

Гломерулонефрит, пиелонефрит и прочие нефропатии требуют обязательной коррекции рациона
Диета при нефропатиях любой природы является неотъемлемой частью успешного лечения. Пациенты с отечностью, выраженным изменением электролитного и общего состава крови, характерными признаками патологии нуждаются в коррекции питания, лечебном рационе. Существенные ограничения накладывают на жидкость, соль, белок.
При остром течении заболевания полностью исключают соль. Ограничения варьируют в зависимости от данных лабораторных исследований. Протеинурия требует увеличения суточного белка наряду со снижением количества углеводов. При выраженных отеках снижают потребление жидкости.
При нефротическом синдроме в рацион требуется включить следующие продукты и блюда:
- овощные бульоны, супы;
- мясо курицы, индейки, крольчатины;
- желе из ягодных и фруктовых морсов;
- свежие фрукты, овощи, зелень;
- кисломолочные продукты.
Важно соблюдать режим питания. Детей необходимо кормить часто малыми порциями. Пища должны быть приготовлена на пару, методом тушения или варки. Примерное меню на день выглядит так:
- утро – сухарики, чай зеленый или теплый морс, безмолочная каша;
- обед – суп-пюре из тыквы с куриной грудкой, галетное печенье, салат из свеклы;
- полдник – снежок или сладкий кисель, сдобная булочка;
- ужин – тушеные овощи с зеленью, тосты, теплый отвар из ягод шиповника с медом.
Меню дополняют свежими фруктами, паровыми овощами. Диета должна быть сбалансированной, разнообразной. Обязательно исключают агрессивную пищу, копчености, фастфуд, в частности, чипсы, соленые орешки.
Детям резко ограничивают сладости, газированную воду. Заменить кондитерские изделия можно медом, сухофруктами, грецкими орехами. Однако с сухофруктами следует быть осторожным, так как курага и чернослив в больших количествах способствуют нарастанию гиперкальциемии.
Возможные осложнения
При постоянной недостаточности белка в организме значительно снижается иммунитет, обостряются инфекционно-воспалительные процессы, хронические заболевания органов, систем. При стойком нарушении почечной функции нарастает азотемия, возникает артериальная гипертензия. Опасным осложнением является вторичная гипертензия с риском развития сердечной недостаточности и отека легких, хроническая почечная недостаточность.
Профилактика и прогноз
При своевременном лечении патологического синдрома обычно наблюдается положительная динамика по выздоровлению, однако прогноз напрямую зависит от степени поражения почечных тканей, стадии органной недостаточности. Врожденный тип патологии при отсутствии наблюдения приводит к хронической почечной недостаточности (ХПН) в раннем возрасте, прогноз всегда серьезный. Профилактика дальнейших разрушений почечных тканей у детей заключается в следующих мероприятиях:
- правильное питание;
- возрастные физические нагрузки;
- соблюдение диеты, охранительного режима;
- организация режима питания, сна, бодрствования.
Для улучшения клинического прогноза и уменьшения прогрессии ХПН важно вовремя лечить респираторные инфекции, обострения хронических инфекций.
Прогноз течения нефротического синдрома у детей тесно связан с характером провоцирующих факторов. При устранении основного заболевания можно рассчитывать на обратимость патологического симптомокомплекса. При отсутствии лечения почечная недостаточность прогрессирует, что в дальнейшем требует заместительной терапии и трансплантации почек.
Видео


* Представленная информация не может быть использована для самостоятельной постановки диагноза, определения лечения и не заменяет обращение к врачу!
Нефротический синдром у детей: виды, в том числе врождённый, причины возникновения, симптомы, диагностика, лечение и профилактика + фото
При нефротическом синдроме тяжёлая протеинурия приводит к снижению плазменного альбумина и отёкам. Причина состояния неизвестна, но некоторые случаи вторичны по отношению к системным заболеваниям типа пурпуры Шёнлейна-Геноха и другим васкулитам (например, СКВ), инфекционным заболеваниям (например, малярии) или аллергии (например, на укусы пчёл).
Клинические симптомы нефротического синдрома:
• периорбитальные отёки (особенно по утрам) — самый ранний признак;
• отёки мошонки, вульвы, ног и лодыжек;
• асцит;
• одышка из-за плеврального выпота и брюшного растяжения.
Стероидчувствительный нефротический синдром
У 85-90% детей с нефротическим синдромом протеинурия разрешается при проведении терапии глюкокортикоидами (стероидчувствительный нефротический синдром). У этих детей не развивается почечная недостаточность. Данный вариант более характерен для мальчиков, нежели для девочек, для азиатских детей, чем для представителей европеоидной расы. Выявлена слабая связь с атопией. Часто провоцируется инфекциями дыхательных путей. Особенности, наводящие на мысль о стероидчувствительном нефротическом синдроме:
• возраст от 1 до 10 лет;
• отсутствие макрогематурии;
• нормальное АД;
• нормальные уровни комплемента;
• нормальная функции почек.
Методы исследования детей при проявлении нефротического синдрома:
• Белок в моче — с помощью тест-полосок (экспресс-анализ).
• Полный анализ крови и СОЭ.
• Мочевина, электролиты, креатинин, альбумин.
• Уровни фракций комплемента — С3 и С4.
• Титры АСЛО и мазок из зева.
• Микроскопия и культуральное исследование мочи.
• Концентрация натрия в моче.
• Маркёры гепатита В.
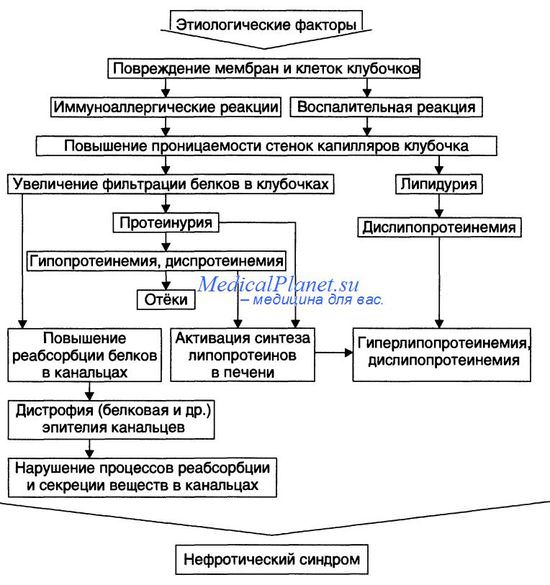
Ведение детей с нефротическим синдромом
Наиболее широко используемый протокол подразумевает первоначальное применение пероральных глюкокортикоидов (60 мг/м2 в день в пересчёте на преднизолон), если нет атипичных симптомов. После 4 нед доза уменьшается до 40 мг/м2 в альтернирующем режиме в течение 4 нед и затем применение глюкокортикоидов прекращается. В среднем белок исчезает из мочи за 11 дней.
Однако имеются современные данные, что продление начального курса стероидов приблизительно до 6 мес с постепенным переходом на альтернирующий режим приёма ведёт к сокращению числа детей, у которых часто развиваются вторичные рецидивы или стероидзависимые формы, и эта схема всё более и более заменяет стандартный протокол.
Дети, которые не отвечают на 4-8-й нед на терапию глюкокортикоидами или имеют атипичные симптомы, могут иметь более тяжёлый диагноз, в связи с чем необходимо проведение биопсии почек. Гистологическая картина почек при стероид-чувствительном нефротическом синдроме обычно нормальная при световой микроскопии, но слияние специализированных эпителиальных клеток (подоцитов), которые обкладывают клубочковые капилляры, выявляется при электронной микроскопии. По этой причине данное состояние называют болезнью минимальных изменений.
У детей с нефротическим синдромом возможны несколько серьёзных осложнений при манифестации или рецидиве.
• Гиповолемия. В течение начальной стадии формирования отёков внутрисосудистый компартмент жидкости может уменьшаться. Ребёнок с гиповолемией, как правило, жалуется на абдоминальную боль и может чувствовать слабость. Возникают периферическая вазоконстрикция и задержка натрия мочи.
Увеличение периферических отёков, оценённых клинически и ежедневным взвешиванием, может причинить дискомфорт и приводить дыхательным нарушениям. Тяжёлые состояния, возможно, нуждаются в лечении с применением внутривенного альбумина. Необходимо следить за использованием коллоидов, поскольку могут возникнуть отёк лёгких и гипертензия от перегрузки объёмом, а также мочегонными средствами, которые могут сами вызвать или ухудшить гиповолемию.
• Тромбоз. Состояние гиперкоагуляции из-за потери антитромбина с мочой, тромбоцитоз, который может быть усилен стероидной терапией, усиленный синтез факторов свёртывания и увеличение вязкости крови вследствие повышенного гематокрита предрасполагают к тромбозу. Возникает, как правило, артериальный тромбоз, который может затронуть мозговое, висцеральное кровообращение и кровоснабжение конечностей с потенциально катастрофическими последствиями.
• Инфекционные осложнения. Дети с рецидивами находятся в группе риска из-за опасности развития инфекции капсулированными бактериями, особенно Pneumococcus. Может развиться перитонит.
• Гиперхолестеринемия (гиперлипидемия). Состояние коррелирует обратно пропорционально относительно содержания альбуминов сыворотки, но причина гиперлипидемии полностью не понятна.
Прогноз нефротического синдрома у детей
Рецидивы идентифицированы родителями при тестировании мочи. Побочные эффекты терапии кортикостероидами можно уменьшить переходом на альтернирующий режим. Если рецидивы возникают часто или требуется высокодозная терапия, желательно привлечение детского нефролога, поскольку необходимо рассмотреть возможность лечения другими препаратами. Левамизол как иммуномодулятор может поддерживать ремиссию. Восьминедельный курс алкилирующими агентами (например, циклофосфамидом или хлорамбуцилом) поддерживает ремиссию у 25-30% детей со стероидозависимыми формами в течение 2 лет.
Циклоспорин поддерживает ремиссию приблизительно у 75% пациентов до тех пор, пока принимается пациентами, но почти всегда возникают рецидивы, когда приём препарата прекращается. На микофенолата мофетил возлагаются большие надежды.
Прогноз гормонорезистентного нефротического синдрома. Эти дети должны быть переданы под наблюдение детского нефролога. Коррекция отёков проводится мочегонной терапией, ограничением соли, ингибиторами АПФ и иногда НПВС, которые могут уменьшить протеинурию.
Прогноз врожденного нефротического синдрома. Врождённый нефротический синдром проявляется в первые 3 мес жизни. Он встречается редко. Наиболее распространённая форма наследуется рецессивно, частота встречаемости гена наиболее высокая в финской популяции. Состояние сопровождается высокой смертностью обычно из-за осложнений в форме гипоальбуминемии, а не почечной недостаточности. Развивающаяся альбуминурия настолько тяжёлая, что для её контроля порой необходима двусторонняя нефрэктомия, что неизбежно вызывает потребности в диализе, который продолжается до тех пор, пока ребёнок не вырастет и не возникнут условия для трансплантации почек.
Нефротический синдром:
• Клинические симптомы — отёк (периорбитальный, мошонки или вульвы, ног и лодыжек), асцит, плевральный выпот.
• Диагноз выставляется на основании массивной протеинурии и низкого уровня альбуминов в плазме.
Стероидочувствительный нефротический синдром:
• Характерные особенности — проявление в возрасте 1-10 лет, отсутствие макрогематурии и АГ, фракции комплемента и функциональные пробы почек в пределах нормы.
• Лечение — пероральные глюкокортикоиды, биопсия почек проводится при отрицательном ответе на терапию и атипичном течении.
• Осложнения — гиповолемия, тромбоз, инфекция (чаще пневмококковая), гиперхолестеринемия (гиперлипидемия).
• Прогноз — может наступить полное выздоровление. В противном случае наблюдаются рецидивы, как частые, так и редкие.
Если ребёнок страдает отёками, проверьте его на протеинурию, чтобы диагностировать нефротический синдром.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Нефротический синдром у детей
Нефротический синдром у детей – это комплекс симптомов и лабораторных показателей или же болезнь, которая проявляется периферическими или генерализованными отеками (в крайней форме это асцит и анасарка). Что касается лабораторных данных при этом диагнозе, фиксируют протеинурию больше 2,5 г/сут или более 50 мг/кг/сут, гипоальбуминемию (менее 40 г/л), гипопротеинемию, гиперлипидемию, диспротеинемию и липидурию.
Осложнения нефторического синдрома у детей
Осложнения при этом заболевании вызваны потерей белков и гиповолемией. Снижается иммунитет, ребенок «подхватывает» инфекции. Может возникнуть железодефицитная анемия, которую нельзя вылечить препаратами железа. Нарушается транспорт по организму холестерина, повышается риск атеросклероза. Может развиться рахитоподобный синдром, потому что организм теряет витамин-Д-связывающий белок. Возникает повышенная кровоточивость, поскольку есть нехватка прокоагулянтов. Повышается количество свободного тироксина в крови.
Что провоцирует / Причины Нефротического синдрома у детей:
В 10 случаях из 100 нефротический синдром у детей – вторичный, то есть вызван определенной причиной (часто это системное заболевание). К НС у детей могут привести такие болезни:
- амилоидоз
- синдроме Альпорта
- геморрагический васкулит
- тромбоз почечной вены
- тромботическая микроангиопатия
Нефротический синдром довольно часто является проявлением первичного гломерулонефрита. Также исследователи говорят о врожденном нефротическом синдроме и семейном НС.
Важно знать, что нефротический синдром у детей может быть и вторичным. Он сопровождает ряд болезней, при которых у ребенка поражены почки:
- ревматоидный артрит
- геморрагический васкулит
- системная красная волчанка
- сахарный диабет
- микроскопический полиангиит и другие
Патогенез (что происходит?) во время Нефротического синдрома у детей:

При нефротическом синдроме развивается гипопротеинемия, потому что с мочой из организма выводятся белки, в основном альбумины (нарушается проницаемость гломерулярного фильтра). Гипопротеинемия становится причиной снижения онкотического давления плазмы. По этой причине жидкость не полностью возвращается в сосудистое русло, начинает задерживаться в тканях. Этим объясняется появление у больного ребенка нефротических отеков. Также важно состояние лимфатических капилляров, поскольку гипергидратация ткани приводит к компенсаторному усилению лимфооттока, вместе с лимфой удаляются тканевые белки. Это приводит к снижению снижает онкотического давления межтканевой жидкости. Данный механизм может до определенного предела препятствовать развитию отека при гипопротеинемии.
Четкая зависимость между уровнем гипопротеинемии и степенью отеков не найдена. Отеки у ребенка могут не появляться, даже если в крови снижен уровень альбуминов. Объяснение может быть во включении компенсаторных механизмов. Если НС у ребенка развивается при первичном гломерулонефрите, его называют идеопатическим нефротическим синдромом. Морфологические изменения заключаются в минимальных, фокально-сегментарном гломерулосклерозе и т.д. При нефротическом синдроме с минимальными изменениями, который обозначается сокращенно как НСМИ, гломерулярная базальная мембрана проницаема преимущественно для низкомолекулярных белковых молекул, потому протеинурия имеет выборочный характер.
Симптомы Нефротического синдрома у детей:
Для нефротического синдрома у детей характерны отеки. Сначала они появляются на лице, потом на веках, далее могут возникнуть в области поясницы и на ногах. Также среди характерных симптомов отмечают бледность кожи, олигурию, связанную с гиповолемией, гиперальдостеронизмом, поражением канальцев. Для НС у детей типичен вторичный гиперальдостеронизм, что становится причиной задержки натрия в детском организме. Это ведет, в свою очередь, к задержке воды, хотя отмечают в крови гипонатриемию.
Гиповолемия в детском возрасте развивается спонтанно, в начале нефротического синдрома, в то время как скорость потери белка выше скорости мобилизации белка из внесосудистых депо. Нефротические отеки имеют генерализированный характер. Сначала они бывают на глазах и лодыжках малыша, потом «двигаются» на торс, достигая степени анасарки и полостных отеков. Отеки характеризуют как мягкие, могут быть ассиметричными. Увеличение печени наблюдают, если отеки при НС выражены сильно.
Неполный нефротический синдром – форма, при которой нет отеков. Смешанный нефротический синдром диагностируют при сочетании НС с гематурией и гипертензией.
Диагностика Нефротического синдрома у детей:
Нефротический синдром диагностируют, если у ребенка отеки и протеинурия, которую можно обнаружить, сдав анализ мочи. Причины заболевания можно выяснить, тщательно собрав анамнез. Если же причину выявить оказывается непросто, могут провести биопсию почек и/или серологические тесты. Диагностическое значение имеет содержание в моче, собранной за сутки, 3 грамм белка. Также по анализу мочи определяют, что в ней есть эритроциты и цилиндры. Исходно присутствует липидурия – в канальцевых клетках есть свободный жир – если нефротический синдром спровоцирован патологией клубочков.
Проведя простую микроскопию, можно обнаружить в моче холестерин, который имеет вид «мальтийского пересечения» под поляризованным светом. Окрашивание Суданом должно использоваться для выявления триглицеридов. При экссудативных заболеваниях и СКВ в больших количествах имеют место лейкоциты.
Для выяснения тяжести и осложнений врачи могут назначить дополнительные тесты. Концентрации креатинина и азота изменяются в зависимости от степени нарушения почечной функции. Содержание альбумина часто менее 25 г/л.
Идиопатический нефротический синдром у детей представлен часто с минимальными изменениями (это было описано выше). Обычно его диагностируют без проведения биопсии, исключения составляют случаи, когда организм не реагирует на пробный курс ГКС (глюкокортикоидов).
Лечение Нефротического синдрома у детей:
В качестве патогенетического лечения нефротического синдрома у детей применяют иммуносупрессивную терапию. Выбирают традиционные, неселективные препараты:
- цитостатики
- глюкокортикоиды
- антиметаболиты
Применяют и селективные иммунодепрессанты:
При иммуносупрессивном лечении ГН применяют такие глюкокортикоиды:
- преднизолон
- преднизол
- медопред
- солу-медрол
- метипред
Нефротический синдром делят на 2 вида в зависимости от реакции на гормональную терапию:
- гормоно(стероидо)чувствительный
- гормоно(стероидо)резистентный
Если у ребенка диагностировали первичный НС, то терапия преднизолоном поможет, заболевание выйдет на стадию ремиссии. Если же на курс препаратов реакции нет, улучшений не наступает, то нужны другие подходы.
Для лечения применяют три режима ГК терапии:
– постоянный пероральный прием преднизолона в дозировке 1–2 мг/кг (делят на 2-4 приема) – назначается сразу после диагностики НС
– альтернативный режим приема (поддерживающая терапия)
суточная доза преднизолона принимается день через день, что поддерживает клинический эффект, но снижает побочные явления.
Среди побочных явлений, возникающих от приема преднизолона:
- эйфория
- повышение аппетита
- психоз
- ожирение
- отеки
- стрии
- миопатия
- гирсутиз
- атрофия кожи
- стероидный диабет
- повышение артериального давления
- и множество других
– пульс-терапия метилпреднизолоном (для достижения очень высоких концентраций ГК в плазме). Внутривенно капельно вводят на протяжении 20-40 минут примерно 30 мг/кг МП один раз за 2 суток.
Цитостатические препараты
Циклофосфамид принимают внутрь или в виде «пульсов». Если назначен прием внутрь, то доза в большинстве случаев составляет 2,0–2,5 мг/кг/сут, курс длится от 8 до 12 недель. Пульс-терапия циклофосфамидом проводится на фоне альтернирующего курса преднизолона при гормонозависимом и гормонорезистентном нефротическом синдроме у ребенка из расчета 12–17 мг/кг внутривенно капельно.
Хлорамбуцил нужно давать ребенку per os в дозе 0,15–0,2 мг/кг в сутки, курс 8-10 недель. На сегодня всё реже применяют азатиоприн и метотрексат, которые являются антиметаболитами.
Цитостатики могут вызвать такие побочные явления:
- лейкопения
- тошнота и рвота
- недостаточность гонад
- геморрагический цистит
- легочный фиброз
- гепатопатия и пр.
Селективные иммунодепрессанты
Применяются такие препараты циклоспорина А:
- сандимун неорал
- сандимун
- биорал
- экорал
Врачи перед назначением таких препаратов должны назначить биопсию почки. Необходим постоянный контроль уровня креатинина в крови и концентрации препарата.
Для лечения могут применяться такие препараты:
- мофетила микофенолат (селсепт)
- такролимус
Они являются новыми селективными иммуносупрессантами. При выявлении стероидорезистентности проводят нефробиопсию.
Принципы лечения первичного ФСГС
Изначально лечение ФСГС осуществляется как терапия идиопатического НС. При соответствующем лечении ПЗ происходит ремиссия, что является хорошим прогностическим признаком. Примерно у 95% процентов больных жизнь сохраняется в течение 10 лет. Когда удается достичь стойкой ремиссии НС, терапия осуществляется как при НСМИ. Но если устанавливается гормонорезистентность, необходимо осуществление нефробиопсии. И только на данном этапе происходит лечение у детей собственно ФСГС, поскольку ранее терапии подвергался идиопатический НС (без морфологического уточнения).
Терапия ФСГС имеет своей целью достижение ремиссии и улучшение прогноза. В случае, если этого не удается достичь, единственной возможностью замедления развития ХПН является снижение протеинурии.
Если показатели протеинурии менее 2 г/сут, в 90% возможна 10-летняя выживаемость больных, тогда как при уровне 2,5–5,0 – лишь около 45%. Если же уровень белка равен или более 14 г/сут, без заместительной терапии больные могут прожить не более 6 лет.
При лечении детей, поскольку преднизолон вводился до проведения биопсии и была доказана гормонорезистентность, терапия проводится алкилирующими агентами, в частности, циклофосфамидом, при альтернирующем режиме приема преднизолона. Возможно введение «пульсов» циклофосфамида или метилпреднизолона.
Наилучшие результаты дает соединение в терапии ФСГС цитостатических (цитотоксических) препаратов и глюкокортикоидов. В этом случае 10-летняя почечная выживаемость больных в среднем 80%, тогда как при лечении только с помощью ГК – примерно 40%, а с помощью ЦС – только 20%. Достижение ремиссии у взрослых пациентов при ФСГС связана с кумулятивной дозой ГК. Если курс приема препаратов не менее 8-9 месяцев, частота наступления ремиссий практически 100%-ая.
Принципы лечения мезангиопролиферативного гломерулонефрита (МзПГН)
Первоначально терапия МзПГН, проявляющегося в виде НС, аналогична лечению идиопатического НС.
Не существует единого способа излечения МзПГН (IgA-нефропатии). Поскольку больные часто являются гормонорезистентными, чаще всего врач назначает цитостатики (в частности, циклофосфамид) и преднизолон, применяя те же схемы. Что и при терапии ФСГС.
Общие рекомендации лечения больных с МзПГН
1. Важнейшее условие правильного и эффективного лечения – осуществление биопсии почки.
2. При быстро развивающейся почечной недостаточности, прогрессирующем нефротическом синдроме, васкулите и нефрите с полулуниями необходимо лечение с помощью кортикостероидов без цитостатиков или в комплексе с ними.
3. Эффективность лечения МзПГН повышается при санировании очагов хронической инфекции. Их уничтожение позволяет сделать рецидивы болезни более редкими. Кроме того, желательна аглиадиновая диета, которая способствует снижению и даже обратному развитию симптомов при целиакии.
4. Для того чтобы у больного ребенка как можно дольше не развивалась почечная недостаточность, необходим строгий контроль гипертензии. Показано ренопротективное лечение с применением блокаторов рецепторов ангиотензина II первого типа в сочетании с диуретиками, а также ингибиторов ангиотензинпревращающего фермента.
Принципы терапии МГН у детей
Прежде всего, больным деткам с нормальной работой почек и при отсутствии нефторического синдрома иммуносупрессивная терапия лечащим врачом не назначается. Но все же они должны постоянно наблюдаться у врача.
Если развивается артериальная гипертензия и обнаружена протеинурия более 1 г/сут, их коррекция проводится с помощью ингибиторов ангиотензинпревращающего фермента. Для нормализации гиперлипидемии показана диета.
Если МГН манифестирует в виде НС или болезнь достигла поздней стадии развития, терапия аналогична лечению идиопатического НС. Если наблюдаются частые рецидивы нефторического синдрома, больной ребенок гормонозависим или резистентен, терапия усиливается с помощью МП, хлорамбуцила или ЦиА (схемы C. Ponticelli, de Santo и др.). Применение комбинаций ЦС и глюкокортикостероидов в дальнейшем приводит к более редким рецидивам. Однако монотерапия ГК так же эффективна для достижения стихания симптомов, как и комбинированный прием указанных препаратов.
МГН, по мнению исследователя C. Ponticelli, – потенциально излечимая болезнь. И это необходимо учитывать при выборе путей лечения заболевания.
Как видно, иммуносупрессивная терапия – основа патогенетического лечения ИНС. Но не менее важны диета, режим, Помимо иммуносупрессивной терапии, не менее важное значение имеют диетические и режимные мероприятия, оздоровление очагов инфекции, лечение побочных недугов, устранение возможных аллергенов и т.п. Но решающим условием достижения стойких долгосрочных ремиссий, которые улучшаю прогноз заболевания, являются ранняя диагностика, назначение, доза и терапия глюкокортикоидами.
Профилактика Нефротического синдрома у детей:
Для профилактики нефротического синдрома следует вовремя лечить инфекционные болезни, не затягивать с походом к врачу. Все рекомендации вашего лечащего врача нужно неукоснительно соблюдать. Если некоторые для вас непонятны или непонятна причина их назначения, лучше переспросить у врача, а не проводить самостоятельную отмену препаратов или уменьшение доз.
Одевайте ребенка по погоде, чтобы не было перегреваний и переохлаждений. Обязательно купите термометр и повесьте за окно, чтобы точно знать температуру на улице, а не надеяться на информацию на погодных сайтах. Во время обострения сезонных аллергий вовремя давайте ребенку антигистаминные препараты (перед приемом нужно проконсультироваться к врачу). По возможности изолируйте ребенка от аллергенов.
К каким докторам следует обращаться если у Вас Нефротический синдром у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Нефротического синдрома у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Нефротический синдром у детей: возможности повлиять на ситуацию

Медицина за более чем две тысячи лет подробно изучила множество различных заболеваний. Одни недуги протекают в острой форме и быстро приводят к выздоровлению. Другие лечатся и существуют в течение жизни с переменным успехом. Открытие микроскопа позволило расшифровать причину инфекционных заболеваний. Исследования генетического кода человека открыли наследственные основы многих болезней. Перспективной отраслью науки в настоящее время является исследование иммунной системы организма. Полученные знания позволяют открыть новые способы лечения таких недугов, как аллергия, бронхиальная астма, ревматоидный артрит. К этому длинному списку принадлежит нефротический синдром у детей — болезнь сложная и многогранная, до сих пор требующая ответов на многие вопросы.
Предпосылки формирования нефротического синдрома у детей
Почки — замечательные, тонко устроенные органы. Их важность для жизни ребёнка подчёркивается тем, что в каждом растущем организме имеются две полноценные структуры. Основная задача почек — избавлять кровь от шлаков и токсинов. Они ежедневно образуются в результате химических превращений в клетках и тканях. Кровь, нуждающаяся в очистке, попадает в почки по широкому артериальному сосуду. Внутри органа он делится на небольшие веточки. Каждая образует собственный сосудистый клубочек.

Нефрон — основная структурная единица почки
Каждый клубочек окружён индивидуальным фильтром. Его отверстия настолько малы, что задерживают все виды клеток крови и крупные белки. Фильтрат содержит смесь полезных и вредных веществ. Итоговая очистка и образование мочи происходит в системе тонких извитых трубок — почечных канальцев. Комплекс из одного клубочка, фильтра и канальцев носит название нефрона. Почка ребёнка содержит множество нефронов. По мере роста они становятся крупнее и способны быстрее образовывать мочу. У детей младшего возраста канальцы более широкие и прямые. Со временем они становятся более тонкими и извитыми.

Почечный фильтр в норме задерживает клетки крови и белки
Нефротический синдром у детей — заболевание почек, при котором с мочой ежедневно теряется большое количество белка. Это обстоятельство влечёт за собой серьёзные изменения состава крови, которые неизбежно сказываются на работе всех органов. Болезнь может развиться у ребёнка любого возраста. Несколько чаще этим недугом страдают мальчики. В зависимости от возраста начала болезни значительно отличается её течение и прогноз.
Что нужно знать о почках — видео
Виды нефротического синдрома
Нефротический синдром не является однородным. По некоторым признакам выделяют его разновидности у детей:
- По характеру заболевания нефротический синдром подразделяется на две основные формы:
- первичный нефротический синдром, который не связан с анатомическими и другими изменениями в почках;
- вторичный тип заболевания. Его началу предшествуют различные изменения в почках.
- По времени появления первых признаков различают два типа нефротического синдрома:
- врождённый. Болезнь проявляется уже в младенческом возрасте, имеет тяжёлое течение и неблагоприятный прогноз:
- синдром «финского типа» ведёт к образованию микроскопических кист;
- синдром «французского типа» преимущественно поражает почечный фильтр;
- потеря белка может происходить на фоне появления рубцов, сдавливающих нефроны;
- приобретённое заболевание часто возникает на фоне уже существующих изменений в почках:
- изменений анатомии почек;
- врождённый. Болезнь проявляется уже в младенческом возрасте, имеет тяжёлое течение и неблагоприятный прогноз:

Нефротический синдром может развиться на фоне анатомических отклонений в строении почек

Опухоль Вильмса — самое распространённое злокачественное новообразование почек у детей
- лёгкая;
- среднетяжёлая;
- тяжёлая.
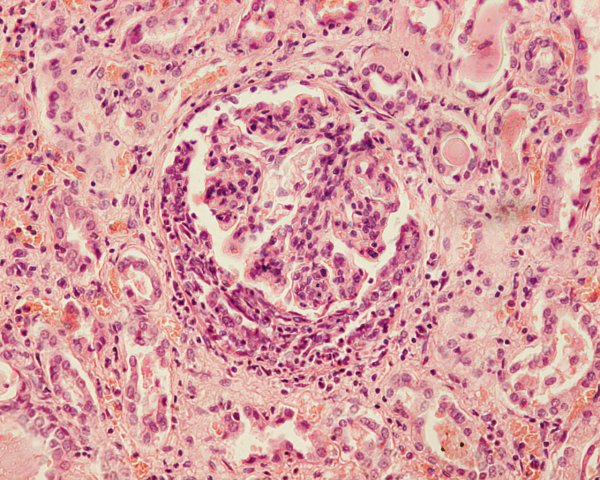
Быстропрогрессирующий нефротический синдром часто носит название злокачественного
- нефротический синдром с сохранённой функцией почек;
- нефротический синдром с почечной недостаточностью.
- гормоночувствительный, симптомы которого быстро исчезают под влиянием лечения;
- гормонозависимый, который реагирует на определённую дозу препарата;
- гормонорезистентный, на течение которого стероиды не влияют.
Причины и факторы риска
Точная причина развития нефротического синдрома у детей в настоящее время не определена. Существует ряд предрасполагающих факторов:
- введение вакцин и других иммунных препаратов;
- длительное употребление некоторых лекарств, в том числе противосудорожных;
- перенесённые инфекционные заболевания — корь, дифтерия, ВИЧ-инфекция, стрептококковая ангина;
- генетическая предрасположенность, полученная по наследству от родителей.

Существует генетическая предрасположенность к возникновению нефротического синдрома у ребёнка
Болезнь начинается с клеток, составляющих почечный фильтр. Отверстия в нём становятся гораздо крупнее необходимого размера. Через них просачиваются крупные белки альбумины, которые в норме присутствуют в кровеносном русле. Они образуются в клетках печени в строго фиксированном количестве. При нефротическом синдроме потеря альбуминов настолько велика, что не может быть компенсирована их образованием.

Белки крови образуются в клетках печени гепатоцитах
Потеря белка влечёт за собой длинную цепь других изменений. В составе крови начинают преобладать жиры (гиперлипидемия). Это обстоятельство негативно сказывается на текучести крови и скорости образования мочи. Кроме того, дефицит альбуминов приводит к тому, что вода из кровеносного русла начинает просачиваться в ткани, образуя отёки разной степени выраженности.
Задержка жидкости в организме, нарушение текучести крови приводит в ряде случаев к повышению артериального давления. Итогом нефротического синдрома часто становится почечная недостаточность. Кровь перестаёт очищаться от шлаков и токсинов, которые в конце концов накапливаются в огромном количестве и приводят к неблагоприятному исходу.
Симптомы нефротического синдрома у детей
Нефротический синдром у детей приводит к появлению целого ряда симптомов, каждый из которых говорит о неблагополучии в организме. И далеко не все указывают именно на заболевание почек. Лишь комплекс симптомов позволяет правильно оценить их вместе и каждый в отдельности.
Симптомы и признаки нефротического синдрома у детей — таблица

Отёк лица и век типичен для нефротического синдрома
Методы установления диагноза
Нефротический синдром у ребёнка — болезнь, которая требует вмешательства специалиста и качественного обследования. На помощь врачу в постановке диагноза придут лабораторные исследования крови и мочи, а также инструментальные методы:
-
общий осмотр — процедура, с которой начинается поиск любого заболевания. При нефротическом синдроме врач обнаружит отёки конечностей, лица, живота, а также выявит признаки скопления жидкости в грудной клетке и сердечной сумке. Кроме того, в обязательном порядке при подозрении на почечную болезнь измеряется кровяное давление. При нефротическом синдроме оно часто повышено;
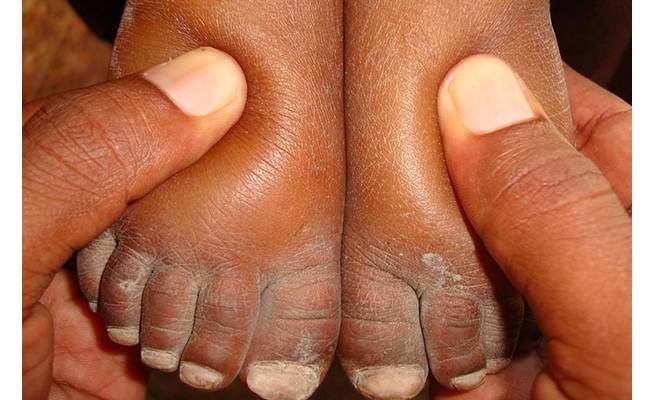
Отёки на ногах — характерная черта гломерулонефрита

При нефротическом синдроме существенно снижено количество белков альбуминов в плазме крови

Цилиндры — белковые слепки почечных канальцев

Ультразвук — основной метод диагностики почечных заболеваний

Гидроторакс — скопление жидкости в грудной полости

При нефротическом синдроме в ткани почек часто обнаруживают скопления жиров (липоидный нефроз)
Дифференциальная диагностика нефротического синдрома проводится со следующими заболеваниями:
- инфекционным воспалением почки пиелонефритом;
- воспалением клубочков гломерулонефритом;
- поражением почек на фоне инфекций и приёма лекарств тубулоинтерстициальным нефритом;
- туберкулёзом почек;
- иммунными заболеваниями: системной красной волчанкой, склеродермией, васкулитом.
Лечение нефротического синдрома у детей
Лечение серьёзного заболевания почек у ребёнка проводится в стационарных условиях под руководством детского врача. Терапия нефротического синдрома обычно носит комплексный характер и включает диету, а также применение медикаментов, в том числе гормонов.
Лекарственные средства
Лекарства — основной метод лечения нефротического синдрома у детей. Назначая препараты, специалист стремится сократить потерю белка, вывести избыток жидкости из организма, а также сохранить работоспособность почек. Дозировки зависят от возраста ребёнка и интенсивности симптомов. Курс лечения подбирается индивидуально для каждого пациента.
Фармакологические средства для лечения нефротического синдрома — таблица
Медикаменты для лечения нефротического синдрома — фотогалерея
Внутривенное введение альбумина позволит компенсировать потерю белка с мочой Преднизолон — стероидный гормон Эндоксан содержит циклофосфамид Лазикс обладает мочегонным действием Гепарин улучшает текучесть крови
Диета
Диета — важная часть лечения нефротического синдрома у ребёнка. Изменения состава крови, отёки, скопление избытка жидкости накладывает на рацион определённые ограничения. В первую очередь необходимо следить за количеством воды, которую ребёнок получает в течение суток. Оно определяется степенью распространённости отёков и нарушений в работе почек. Кроме того, необходимо исключить продукты с большим содержанием натрия и калия. Питание должно быть дробным, особенно у детей с асцитом. Меню ребёнка должно соответствовать возрасту. Для младенцев первого года жизни это грудное молоко, смесь и прикорм. В более старшем возрасте рекомендуется употребление следующих продуктов и блюд:
- овощных супов и гарниров;
- блюд из филе курицы, индейки и кролика;
- кисломолочных продуктов;
- ягодных желе и других десертов;
- свежей зелени;
- свежих фруктов.
Продукты, рекомендованные к употребелению — фотогалерея
Овощной суп не содержит избытка жира и экстрактивных веществ Желательно использовать диетические сорта мяса, например, индейку Йогурт содержит кальций Ягодное желе — идеальный десерт Яблоки и груши — источник витаминов
Необходимо избегать употребления следующих продуктов:
- копчёностей;
- консервов;
- острых специй;
- шоколада и других кондитерских изделий;
- сухофруктов;
- газированных напитков;
- поваренной соли.
Продукты, не рекомендованные к употреблению — фотогалерея
Копчёности содержат много экстрактивных веществ и соли Консервы содержат большое количество соли Шоколад может вызвать аллергические реакции на фоне приёма препаратов Поваренная соль приводит к задержке жидкости в организме Газированные напитки вызывают повышенную жажду
Хирургические и физиотерапевтические методики для лечения нефротического синдрома не применяются. Использование народных средств не доказало свою эффективность.
Осложнения и прогноз
Прогноз лечения нефротического синдрома у детей индивидуален и зависит от формы заболевания. При адекватной терапии большинство симптомов недуга сворачивается, улучшается общее состояние. В тяжёлых случаях возможно развитие осложнений:
- резкого расстройства деятельности сердца — гиповолемического шока;
- воспаления брюшины, покрывающей органы живота, — перитонита;
- выраженного расстройства деятельности почек — почечной недостаточности;

Почечная недостаточность затрагивает все органы и ткани
Профилактика
Поскольку причины нефротического синдрома у детей до конца не изучены, действенных методов профилактики этого заболевания в настоящее время не разработано.
Нефротический синдром у ребёнка — более чем серьёзное заболевание. Этот недуг чаще протекает в течение всей жизни. Гормональное лечение позволяет во многих случаях значительно сгладить изменения, происходящие в детском организме. Однако, даже несмотря на соответствующее лечение, прогноз в ряде случаев остаётся серьёзным.
Нефротический синдром: причины, признаки, диагностика, лечение у детей
Нефротический синдром у детей проявляется в виде отеков и снижения диуреза. Патология развивается на фоне заболеваний сердца, сосудов, онкогематологических и аутоиммунных болезней. Нефротический синдром сложно поддается лечению из-за частых случаев резистентности к медикаментам.

Причины развития нефротического синдрома у детей
У детей чаще всего диагностируют первичную форму нефротического синдрома, которая возникает из-за поражения клубочкового аппарата почек. Нефротический синдром возникает при пиелонефрите, гломерулонефрите.
Причины развития вторичного нефротического синдрома:
- аутоиммунные патологии — синдром Шегрена, системные васкулиты, системная красная волчанка;
- злокачественные новообразования — лимфома Ходжкина, множественная миелома;
- токсическое поражение почек, вызванное бесконтрольным приемом нестероидных противовоспалительных препаратов, некоторых антибиотиков, отравлением ядом змей и насекомых, солями тяжелых металлов;
- нарушение почечного кровотока при тромбозе почечной вены, злокачественной гипертензии, серповидно-клеточной анемии;
- абсцесс легких, септический эндокардит, бронхоэктазам;
- туберкулез, малярия, врожденный сифилис;
- врожденные гломерулопатии при синдроме Альпорта, болезни Фабри.
Клинические проявления
Для нефротического синдрома характерно острое начало. Чаще всего характерные симптомы появляются после переохлаждения, вакцинации, инфекционных патологий, при обострении хронических болезней. Начальные признаки — слабость, сонливость, головная боль, тошнота, отсутствие аппетита, дискомфорт в абдоминальной области. У девочек в подростковом возрасте нарушается менструальный цикл.
Один из основных симптомов — отечность. Сначала утром отекает лицо, а к вечеру голени. Постепенно отеки распространяются по всему телу. Изначально отеки мягкие, симметричные, кожные покровы над ними сухие и теплые. Второй признак — уменьшение суточного количества мочи. Дополнительные проявления — сухость во рту, жажда, понос, вздутие живота, судороги, парестезия. Кожа бледная, сухая и шелушится, волосы и ногти ломкие.
Помимо внешних отеков, возникают и полостные — асцит, гидроторакс, гидроперикард. Что негативно отражается на состоянии ребенка.
Методы диагностики
При появлении признаков нефротического синдрома необходимо обратиться к детскому нефрологу. Диагностика начинается со сбора анамнеза и осмотра.
Врач отмечает сухую, холодную кожу, обложенность языка, отечность, увеличение объема живота. При прослушивании тона сердца приглушенные, перкуторный звук укорочен, дыхание ослабленное, слышны мелкопузырчатые хрипы.
Диагностический комплекс включает:
- Общий, биохимический анализ мочи. Суточная протеинурия более 50 мг/кг, соотношение протеина и креатинина более двух единиц, экскреция альбумина превышает 40 мг на кв. м в час. Плотность мочи повышена, в урине много лейкоцитов, цилиндров, присутствуют кристаллы холестерина, капель жира.
- Дополнительно назначают анализ мочи по Нечипоренко.
- Пробы Реберга проводят для оценки функций почек.
- Биохимический анализ крови. Показатели альбумина, натрия и кальция снижены, уровень холестерина, триглицеридов, креатинина, калия повышен.
- Общий анализ крови. Повышена СОЭ, количество эозинофилов, тромбоцитов. Незначительно снижены показатели гемоглобина, эритроцитов.
- Коагулограмма. Высокий уровень фибриногена.
- ЭхоКГ, ЭКГ. Назначают для выявления гидроперикарда, нарушения сердечного ритма.
- УЗИ почек, УЗДГ почечных сосудов, нефросцинтиграфия.
- Биопсия почек. Пункцию делают детям до года и подросткам старше 12 лет. Полученный биоматериал отправляют на иммунофлюоресцентную, электронную и световую микроскопию.

Методы лечения
При выявлении нефротического синдрома ребенка госпитализируют на 15–20 дней. Назначают медикаментозное лечение и диету.
Группы препаратов для лечения нефротического синдрома:
- коллоидные и кристаллоидные растворы;
- глюкокортикостероиды;
- ингибиторы кальциневрина;
- диуретики;
- ингибиторы АПФ, блокаторы рецепторов ангиотензина;
- препараты витамина D.
Показано питание с высоким содержанием белка — 1,3–1,5 г/кг. Необходимо употреблять полноценные и легкоусвояемые белки — нежирное мясо и рыба, творог, яичный белок. Пищу готовят без соли, из рациона исключают все продукты, которые содержат большое количество соли. Но раз в неделю нужно употреблять 3–4 г соли для предотвращения осложнений бессолевой диеты. Ограничить следует количество сахара. В список запрещенных продуктов входит лук, чеснок, редька.
При хорошей восприимчивости к стероидам выздоровление наблюдается у 95% детей с нефротическим синдромом, функции почек не нарушены. При непереносимости гормональных препаратов велика вероятность развития хронической почечной недостаточности.
Чем опасен нефротический синдром?
При длительном течении болезни уменьшается количество альбуминов. Это приводит к ослаблению иммунитета — ребенок часто болеет респираторными инфекциями, страдает от рецидивирующего синусита, тонзиллита. Из-за снижения уровня трансферрина развивается железодефицитная анемия.
Для маленьких детей опасно снижение уровня белка, который связывает витамин D. Нарушается рост костей, снижается минерализация костной ткани. Иногда при нефротическом синдроме наблюдается дефицит прокоагулянтов, что приводит к повышенной кровоточивости.
Редко нефротический синдром может стать причиной отека мозга, гиповолемического шока.
Первичная профилактика нефротического синдрома заключается в соблюдении правил приема лекарств, раннем выявлении и лечении аутоиммунных патологий, избегании контактов в нефротоксическими веществами. Вторичная профилактика — это курсы стероидной терапии при обострении заболевания.


